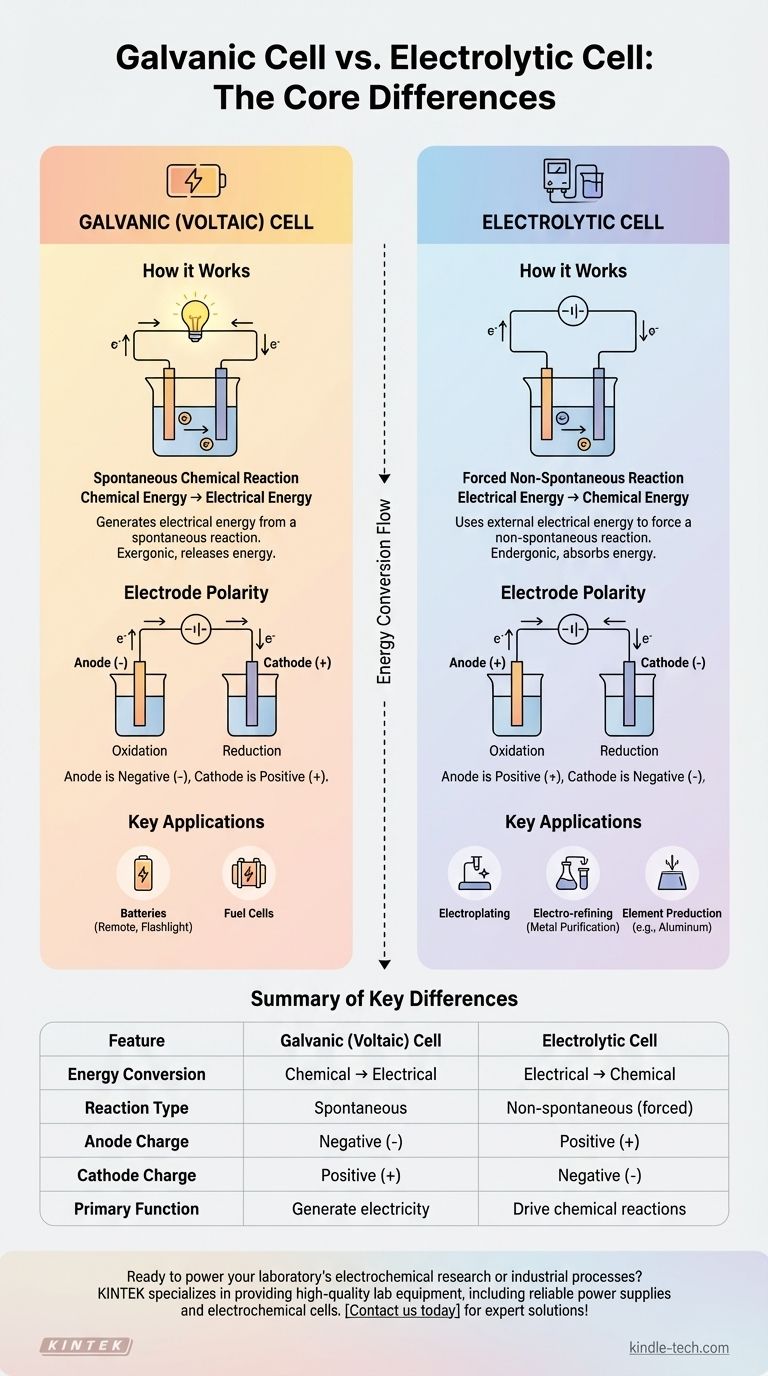
Aunque su pregunta menciona dos celdas electrolíticas, la distinción central en electroquímica es entre una celda electrolítica y una celda galvánica (también conocida como celda voltaica). Una celda galvánica genera energía eléctrica a partir de una reacción química espontánea, como una batería común. Por el contrario, una celda electrolítica utiliza una fuente externa de energía eléctrica para forzar que ocurra una reacción química no espontánea.
La diferencia fundamental radica en la conversión de energía. Una celda galvánica convierte la energía química almacenada en energía eléctrica, mientras que una celda electrolítica hace exactamente lo contrario, convirtiendo la energía eléctrica en energía química para producir sustancias deseadas.

Cómo funcionan las celdas galvánicas (voltaicas)
Una celda galvánica es un sistema autónomo que produce electricidad. Piense en cualquier batería estándar que utilice en un control remoto o una linterna.
Reacciones químicas espontáneas
El motor de una celda galvánica es una reacción redox (reducción-oxidación) espontánea. Esto significa que la reacción química ocurre de forma natural sin ninguna entrada de energía externa, liberando energía en el proceso.
Conversión de energía: de química a eléctrica
La energía liberada por la reacción espontánea empuja los electrones a través de un circuito externo, creando una corriente eléctrica. Transforma eficazmente la energía potencial química almacenada en energía eléctrica utilizable.
Polaridad de los electrodos
En una celda galvánica, el ánodo es el electrodo negativo donde ocurre la oxidación, y el cátodo es el electrodo positivo donde ocurre la reducción. Los electrones fluyen desde el ánodo negativo hacia el cátodo positivo.
Cómo funcionan las celdas electrolíticas
Una celda electrolítica se utiliza para impulsar cambios químicos que no ocurrirían por sí solos. Este proceso se conoce como electrólisis.
Forzar reacciones no espontáneas
Estas celdas están diseñadas para forzar que proceda una reacción no espontánea. Por ejemplo, el agua no se descompone espontáneamente en hidrógeno y oxígeno; requiere energía para forzar su separación.
El papel de una fuente de alimentación externa
Para impulsar esta reacción, una celda electrolítica debe estar conectada a una fuente de alimentación externa, como una batería o una fuente de alimentación de CC. Esta fuente proporciona la energía necesaria para superar la resistencia natural de la reacción.
La función del electrolito
La celda contiene un electrolito, que suele ser una sal fundida o una solución salina. Esta sustancia contiene iones móviles que son atraídos hacia los electrodos, lo que permite que ocurran las reacciones químicas y se complete el circuito eléctrico.
Aplicaciones en la industria
Este proceso es fundamental para muchas aplicaciones industriales, incluida la galvanoplastia (recubrimiento de un objeto con una fina capa de metal), la electrorefinación para purificar metales como el cobre y la producción de elementos puros como el aluminio a partir de la bauxita.
Comprender las diferencias fundamentales
Comparar estas dos celdas lado a lado revela su naturaleza opuesta. Son dos caras de la misma moneda electroquímica.
Flujo de energía y espontaneidad
Una celda galvánica es exergónica, lo que significa que libera energía de una reacción espontánea. Una celda electrolítica es endergónica, lo que significa que absorbe energía para impulsar una reacción no espontánea.
Inversión de la polaridad de los electrodos
Este es un punto crítico de distinción. Si bien la oxidación siempre ocurre en el ánodo y la reducción en el cátodo, sus cargas se invierten.
- En una celda galvánica: El ánodo es negativo (-), el cátodo es positivo (+).
- En una celda electrolítica: El ánodo es positivo (+), el cátodo es negativo (-).
Esta inversión ocurre porque la fuente de alimentación externa en una celda electrolítica dicta el flujo de electrones, anulando la tendencia natural del sistema químico.
Tomar la decisión correcta para su objetivo
Comprender qué celda usar depende completamente de si su objetivo es generar energía o crear un producto químico.
- Si su enfoque principal es generar energía a partir de un proceso químico: Está describiendo una celda galvánica (voltaica), que es el principio detrás de todas las baterías.
- Si su enfoque principal es utilizar energía para crear una sustancia: Necesita una celda electrolítica, que es la base para la galvanoplastia industrial, la refinación y la producción de elementos.
- Si su enfoque principal es comprender la electroquímica básica: Recuerde que las celdas galvánicas liberan energía espontáneamente, mientras que las celdas electrolíticas requieren energía para forzar una reacción.
En última instancia, la dirección de la conversión de energía es el factor más importante que define y separa estas dos celdas electroquímicas fundamentales.
Tabla de resumen:
| Característica | Celda Galvánica (Voltaica) | Celda Electrolítica |
|---|---|---|
| Conversión de energía | Química → Eléctrica | Eléctrica → Química |
| Tipo de reacción | Espontánea | No espontánea (forzada) |
| Carga del ánodo | Negativa (-) | Positiva (+) |
| Carga del cátodo | Positiva (+) | Negativa (-) |
| Función principal | Generar electricidad (ej. baterías) | Impulsar reacciones químicas (ej. galvanoplastia, refinación) |
¿Listo para potenciar la investigación electroquímica o los procesos industriales de su laboratorio? KINTEK se especializa en proporcionar equipos y consumibles de laboratorio de alta calidad, incluidas fuentes de alimentación y celdas electroquímicas fiables adaptadas a sus necesidades específicas. Ya sea que esté desarrollando nuevas tecnologías de baterías u optimizando sistemas de galvanoplastia, nuestra experiencia garantiza que tenga las herramientas adecuadas para el éxito. ¡Contáctenos hoy para analizar cómo podemos apoyar sus proyectos con equipos de precisión y soluciones expertas!
Guía Visual