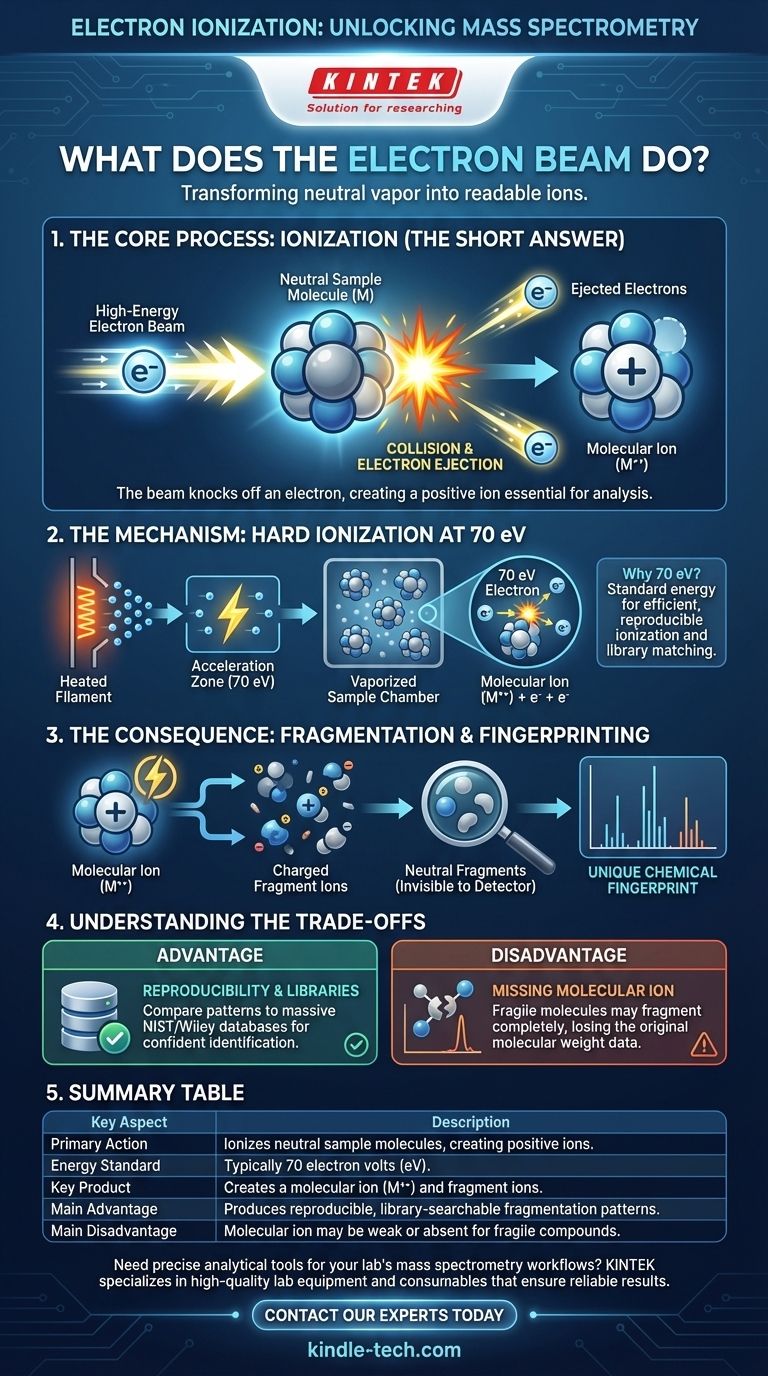
En resumen, el haz de electrones ioniza la muestra. Colisiona con las moléculas neutras en el vapor, expulsando uno de sus propios electrones. Esto transforma las moléculas neutras en iones con carga positiva, un paso crucial que permite que sean controlados y analizados por el espectrómetro de masas.
El propósito fundamental del haz de electrones es impartir una carga positiva a las moléculas de la muestra. Esta conversión de neutro a cargado es lo que hace posible el análisis de masas, ya que solo los iones pueden ser acelerados y separados por campos eléctricos y magnéticos.

El Mecanismo de Ionización por Electrones (EI)
El proceso sobre el que pregunta es una técnica de ionización "dura" conocida como Ionización por Electrones (EI). Es un método fundamental en la espectrometría de masas, particularmente para identificar compuestos orgánicos desconocidos.
El Evento de Colisión
Un filamento calentado, generalmente hecho de tungsteno o renio, libera un flujo de electrones. Estos electrones son luego acelerados a través de una brecha de voltaje, generalmente a una energía estándar de 70 electronvoltios (70 eV). Este haz de alta energía se dirige a través de la muestra vaporizada.
Creación del Ion Molecular
Cuando un electrón de 70 eV golpea una molécula de muestra neutra (M), su energía es lo suficientemente alta como para desalojar uno de los electrones propios de la molécula.
El resultado es un catión radical con carga positiva, conocido como el ion molecular (M+•). El electrón original y el electrón desalojado se eliminan luego del sistema.
Por qué 70 eV es el Estándar
Este nivel de energía específico se utiliza porque está muy por encima de la energía requerida para ionizar la mayoría de las moléculas orgánicas (típicamente 7-15 eV). Esto asegura una ionización eficiente y, fundamentalmente, produce resultados altamente reproducibles que pueden compararse con vastas bibliotecas espectrales para la identificación de compuestos.
La Consecuencia Crítica: Fragmentación
La energía de 70 eV transferida durante la colisión es a menudo mucho mayor de lo que la molécula puede soportar. Esta energía en exceso hace que el ion molecular recién formado se rompa en pedazos más pequeños.
Una Huella Dactilar Predecible
Este proceso, llamado fragmentación, no es aleatorio. Una molécula específica se descompondrá consistentemente de la misma manera, produciendo un patrón característico de iones de fragmentos cargados más pequeños.
Este patrón de fragmentación actúa como una huella dactilar química única. Al analizar las masas de estos fragmentos, los químicos pueden deducir la estructura original de la molécula desconocida.
Lo que Detecta el Espectrómetro de Masas
Es crucial entender que el espectrómetro de masas solo detecta y analiza las partículas cargadas. Esto incluye el ion molecular original (si es lo suficientemente estable como para sobrevivir) y los diversos iones de fragmentos cargados. Cualquier fragmento neutro que se desprenda es invisible para el detector.
Comprender las Compensaciones
Como cualquier técnica analítica, la Ionización por Electrones tiene ventajas y desventajas distintas que son fundamentales de entender.
La Ventaja: Reproducibilidad y Bibliotecas
La principal fortaleza de EI es su reproducibilidad. Debido a que el estándar de 70 eV se usa tan ampliamente, existen bases de datos masivas y consultables (como las bibliotecas NIST y Wiley). Puede comparar el patrón de fragmentación de su muestra desconocida con estas bibliotecas para encontrar una coincidencia, lo que lo convierte en una herramienta poderosa para la identificación.
La Desventaja: El Ion Molecular Faltante
El principal inconveniente de este método de ionización "duro" es que algunas moléculas son demasiado frágiles. El ion molecular puede fragmentarse tan completamente que muy poco, o nada, de él llega al detector. Cuando esto sucede, se pierde la pieza de datos más importante: el peso molecular del compuesto original.
Cómo Afecta Esto a Su Análisis
Comprender este proceso le permite interpretar sus resultados correctamente y elegir el método adecuado para su objetivo.
- Si su enfoque principal es identificar un compuesto desconocido común: El rico patrón de fragmentación producido por EI es su herramienta más poderosa para una búsqueda de biblioteca segura.
- Si su enfoque principal es determinar el peso molecular de una molécula nueva o frágil: Tenga en cuenta que el pico del ion molecular puede ser débil o estar ausente con EI, y puede ser necesaria una técnica de ionización "más suave".
En última instancia, el haz de electrones transforma una molécula neutra invisible en una firma química legible e identificable.
Tabla Resumen:
| Aspecto Clave | Descripción |
|---|---|
| Acción Principal | Ioniza moléculas de muestra neutras, creando iones positivos. |
| Estándar de Energía | Típicamente 70 electronvoltios (eV). |
| Producto Clave | Crea un ion molecular (M+•) e iones de fragmentos. |
| Ventaja Principal | Produce patrones de fragmentación reproducibles y consultables en bibliotecas. |
| Desventaja Principal | El ion molecular puede ser débil o estar ausente para compuestos frágiles. |
¿Necesita herramientas analíticas precisas para los flujos de trabajo de espectrometría de masas de su laboratorio? KINTEK se especializa en equipos de laboratorio y consumibles de alta calidad que garantizan resultados fiables. Desde fuentes de ionización robustas hasta los consumibles que mantienen sus instrumentos en funcionamiento, apoyamos las necesidades de su laboratorio para una identificación precisa de compuestos. Contacte a nuestros expertos hoy para discutir cómo podemos mejorar sus capacidades analíticas.
Guía Visual