En esencia, el diseño de un biorreactor es un ejercicio de biología aplicada. Primero debe comprender profundamente las necesidades de las células o microorganismos que desea cultivar. Solo entonces podrá diseñar un recipiente físico y un sistema de control que cree el entorno perfecto para que prosperen y generen el producto deseado.
El error más común en el diseño de biorreactores es centrarse primero en el hardware. El diseño óptimo siempre fluye desde la biología hacia afuera, haciendo coincidir las características físicas del recipiente y las capacidades de control con los requisitos metabólicos precisos y la sensibilidad al cizallamiento de su línea celular específica.

La base: defina su proceso biológico
Antes de que se gire un solo tornillo, todo el diseño está dictado por el organismo vivo en el centro del proceso. Su tarea principal es definir sus necesidades.
Caracterizar el cultivo celular
El tipo de célula es el factor más importante. ¿Es un cultivo microbiano robusto como bacterias o levaduras, o una línea celular de mamíferos frágil y sensible?
Las células microbianas (p. ej., E. coli, S. cerevisiae) a menudo pueden soportar una agitación alta y tienen tasas de crecimiento rápidas, lo que exige una alta transferencia de oxígeno y una eliminación eficiente del calor.
Las células de mamíferos (p. ej., células CHO) son mucho más grandes, carecen de pared celular y son muy sensibles al estrés por cizallamiento. Requieren una mezcla suave y un entorno controlado con mayor precisión.
Comprender los requisitos metabólicos
Debe cuantificar lo que sus células consumen y lo que producen. Las preguntas clave incluyen:
- ¿Aeróbico o anaeróbico? Esto determina toda la estrategia de manejo de gases. Los procesos aeróbicos necesitan un suministro eficiente de oxígeno, mientras que los anaeróbicos deben excluirlo.
- ¿Cuáles son los nutrientes clave? Esto dicta la formulación del medio de cultivo y la estrategia de alimentación (por lotes, por lotes alimentados o perfusión).
- ¿Qué productos de desecho se acumulan? Los subproductos como el lactato o el amoníaco pueden volverse tóxicos e inhibir el crecimiento, lo que requiere un monitoreo y control cuidadosos.
Aclarar la expresión del producto
¿Dónde está su producto objetivo? ¿Se secreta en el medio de cultivo, lo que facilita su recolección?
¿O es un producto intracelular, lo que significa que las células deben recolectarse y lisarse (romperse) para recuperarlo? Esta decisión impacta fundamentalmente los pasos de procesamiento posteriores.
Principios básicos de ingeniería
Una vez definidas las necesidades biológicas, puede traducirlas en especificaciones de ingeniería para el sistema del reactor.
Geometría y material del recipiente
El recipiente en sí es el contenedor principal. Las dos opciones de material dominantes son el acero inoxidable y el plástico de un solo uso.
La relación de aspecto del recipiente (altura-diámetro) influye en la eficiencia de la mezcla y la formación de espuma. Un recipiente más alto y delgado puede mejorar la transferencia de gas, pero puede crear zonas de mezcla, mientras que un recipiente más corto y ancho proporciona una mezcla más uniforme.
Agitación y transferencia de masa
El objetivo de la agitación es crear un ambiente homogéneo, asegurando que las células tengan acceso uniforme a nutrientes y oxígeno mientras se previenen gradientes térmicos.
El impulsor (la "hélice") es clave. Una turbina Rushton es excelente para la dispersión de gases y la transferencia de masa alta en cultivos microbianos robustos. Un impulsor de palas inclinadas o de estilo marino proporciona un flujo axial más suave, lo cual es fundamental para las células de mamíferos sensibles al cizallamiento.
La eficacia del suministro de oxígeno se mide por el coeficiente de transferencia de masa (kLa). Su diseño debe lograr un kLa que satisfaga la tasa de consumo de oxígeno (OUR) de las células.
Aireación e intercambio de gases
Este sistema suministra oxígeno y elimina el CO2 residual. Un pulverizador, típicamente un anillo o frita porosa en la parte inferior del recipiente, libera burbujas de gas en el medio.
El tamaño de las burbujas importa. Los micro-pulverizadores crean burbujas muy finas con una gran superficie para una mejor transferencia de oxígeno, pero también pueden generar más espuma. El caudal de gas y la composición (p. ej., enriquecimiento con O2 puro) son parámetros de control críticos.
Esterilización y operación aséptica
El sistema debe ser estéril para evitar la contaminación. Los reactores de acero inoxidable utilizan procedimientos de limpieza in situ (CIP) y esterilización in situ (SIP).
Los biorreactores de un solo uso (SUB) vienen preesterilizados por irradiación gamma, lo que elimina la necesidad de estos complejos pasos de utilidad y garantiza la esterilidad desde el primer momento. Todo el diseño debe mantener una barrera aséptica.
Comprender las compensaciones
Cada elección de diseño implica un compromiso. Comprender estas compensaciones es el sello distintivo de un ingeniero experimentado.
Sistemas de acero inoxidable vs. de un solo uso
El acero inoxidable ofrece máxima durabilidad y personalización. Representa un alto gasto de capital, pero puede tener un costo a largo plazo por lote más bajo para una producción dedicada a gran escala. Sin embargo, requiere una infraestructura significativa para la limpieza y esterilización, lo que lleva a tiempos de respuesta más largos.
Los biorreactores de un solo uso (SUB) ofrecen una flexibilidad y velocidad inigualables. Eliminan la validación de la limpieza y reducen drásticamente el riesgo de contaminación cruzada. Esto los hace ideales para instalaciones multiproducto y fabricación clínica, a pesar de un costo por lote más alto debido a los componentes desechables.
Alta agitación vs. bajo estrés por cizallamiento
Para la fermentación industrial, el objetivo suele ser maximizar la agitación para lograr el kLa más alto posible para un cultivo microbiano denso. El hardware está diseñado para una mezcla agresiva.
Para la producción de proteínas terapéuticas en células de mamíferos, este enfoque es destructivo. El diseño debe minimizar el estrés por cizallamiento. Esto significa usar impulsores de bajo cizallamiento, optimizar su posición y controlar la velocidad de rotación (RPM) con precisión, a menudo complementando el control de oxígeno mediante el flujo de gas en lugar de la agitación.
Escalabilidad: del laboratorio a la producción
Un diseño que funciona a 2 litros no funcionará automáticamente a 2.000 litros. A medida que aumenta el volumen, la relación superficie-volumen disminuye, lo que dificulta mucho la eliminación del calor.
Para garantizar que un proceso sea escalable, los diseñadores a menudo intentan mantener ciertos parámetros constantes, como la potencia por unidad de volumen (P/V) o la velocidad de la punta del impulsor. Este modelado debe considerarse durante la fase de diseño inicial para evitar fallas en el proceso a mayor escala.
Tomar la decisión correcta para su objetivo
Su diseño final es un reflejo directo de su objetivo principal.
- Si su enfoque principal es la investigación y el desarrollo rápido de procesos: Elija un sistema de sobremesa de un solo uso flexible y preesterilizado para maximizar el rendimiento experimental y minimizar el tiempo de respuesta.
- Si su enfoque principal es producir un producto terapéutico comercial con células de mamíferos: Priorice un sistema de un solo uso con agitación de bajo cizallamiento, amplia integración de sensores y una ruta de diseño escalable y bien documentada.
- Si su enfoque principal es la fermentación industrial a gran escala (p. ej., biocombustibles, enzimas): Diseñe un reactor de acero inoxidable robusto y rentable optimizado para una alta transferencia de masa, enfriamiento eficiente y producción dedicada a largo plazo.
Un biorreactor bien diseñado no es solo un equipo; es un ecosistema diseñado con precisión y adaptado a la vida que contiene.
Tabla resumen:
| Consideración de diseño | Preguntas clave | Impacto en el diseño |
|---|---|---|
| Tipo de célula | ¿Microbiana vs. de mamífero? | Intensidad de agitación, sensibilidad al cizallamiento |
| Metabolismo | ¿Aeróbico o Anaeróbico? | Estrategia de manejo de gases, suministro de oxígeno |
| Material del recipiente | ¿Acero inoxidable vs. un solo uso? | Costo de capital, flexibilidad, necesidades de esterilización |
| Escala | ¿I+D de sobremesa o producción a gran escala? | Escalabilidad, transferencia de calor, eficiencia de mezcla |
¿Listo para construir el biorreactor ideal para su aplicación específica? El equipo de laboratorio adecuado es fundamental para el éxito. KINTEK se especializa en equipos y consumibles de laboratorio de alta calidad, satisfaciendo diversas necesidades de laboratorio. Nuestros expertos pueden ayudarle a seleccionar el sistema de biorreactor perfecto para asegurar que sus células prosperen y su proceso escale de manera eficiente. Contacte a nuestro equipo hoy para discutir su proyecto y descubrir cómo podemos apoyar sus objetivos de investigación y producción.
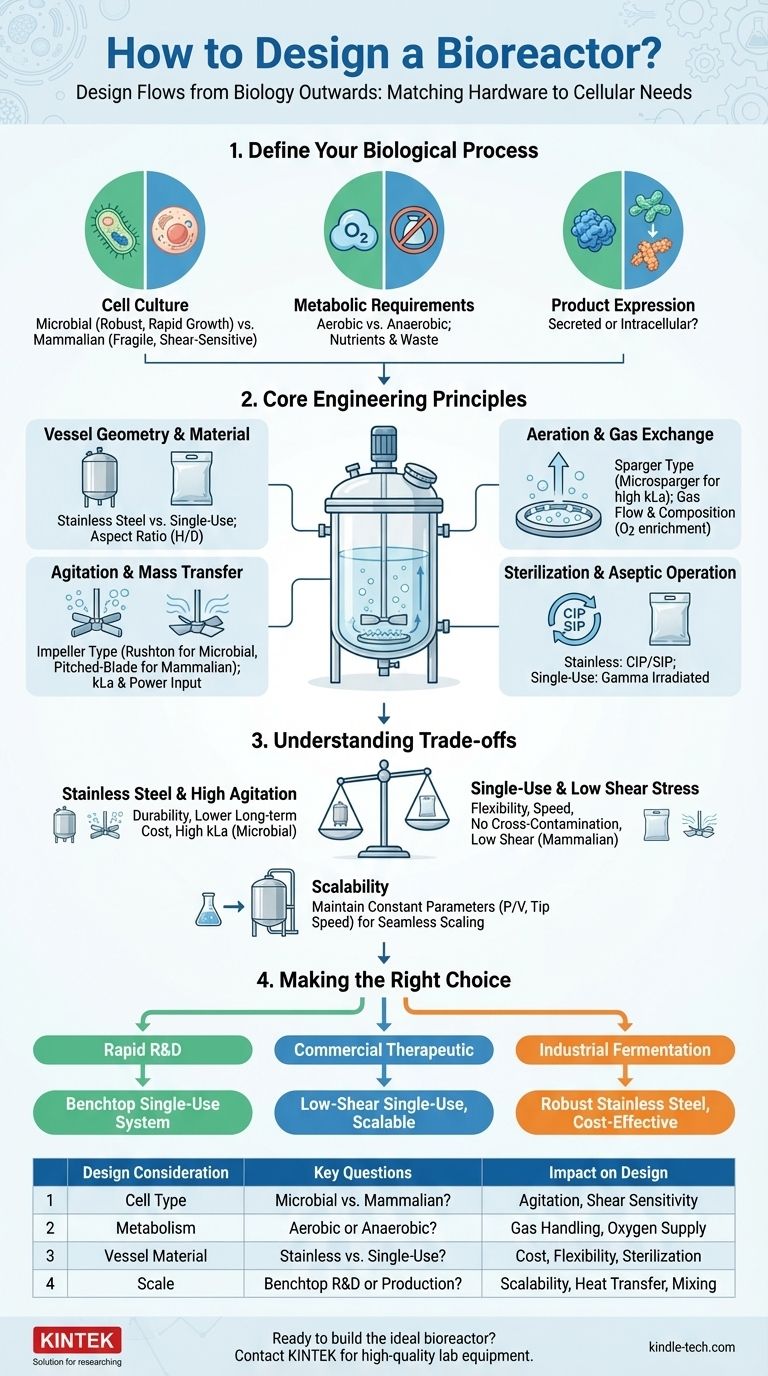
Guía Visual
Productos relacionados
- Reactores de Laboratorio Personalizables de Alta Temperatura y Alta Presión para Diversas Aplicaciones Científicas
- Reactor Visual de Alta Presión para Observación In Situ
- Reactores personalizables de alta presión para aplicaciones científicas e industriales avanzadas
- Reactor de Presión de Laboratorio Autoclave de Alta Presión de Acero Inoxidable
- Reactor Autoclave de Laboratorio de Alta Presión para Síntesis Hidrotermal
La gente también pregunta
- ¿Por qué el argón es mejor que el nitrógeno para atmósferas inertes? Asegure Reactividad y Estabilidad Absolutas
- ¿Cómo influye un sistema automático de control de temperatura en el magnesio de alta pureza? Estabilización Térmica de Precisión
- ¿Cómo garantizan los reactores de alta presión y alta temperatura el tratamiento eficaz de las aguas residuales lignocelulósicas en WAO?
- ¿Cómo afecta la presión inicial de oxígeno a la oxidación húmeda de lodos farmacéuticos? Domina la profundidad de tu oxidación
- ¿Cómo garantiza un sistema de calentamiento con control de temperatura de alta precisión la cinética de corrosión precisa? Expert Lab Solutions





