En un entorno de laboratorio, la eliminación de un disolvente por evaporación implica aplicar energía, generalmente en forma de calor, y/o reducir la presión ambiental. Esto proporciona a las moléculas del disolvente suficiente energía para escapar a la fase gaseosa, dejando atrás los componentes menos volátiles de su mezcla, como el producto deseado. Este proceso se gestiona activamente mediante equipos específicos para controlar la velocidad y la temperatura.
El desafío central de la eliminación de disolventes no es solo la evaporación, sino la evaporación controlada. Su objetivo es eliminar el disolvente lo más rápido posible sin degradar o perder la muestra que intenta aislar. El mejor método siempre depende de las propiedades del disolvente y de la sensibilidad de la muestra.

Los principios fundamentales de la evaporación
Para elegir el método correcto, primero debe comprender los cuatro factores que puede manipular para controlar la velocidad de evaporación. Estos principios son la base de cada técnica.
El papel de la temperatura
Aumentar la temperatura de un disolvente aumenta directamente la energía cinética de sus moléculas. Esto facilita que superen las fuerzas que las mantienen en la fase líquida y escapen como gas. Más calor significa una evaporación más rápida.
El papel de la presión
Reducir la presión sobre un líquido disminuye su punto de ebullición. Este es el principio más importante para manejar muestras sensibles. Al colocar una muestra bajo vacío, puede hacer que el disolvente hierva y se evapore a una temperatura mucho más baja y segura, protegiendo su compuesto de la degradación térmica.
El papel del área superficial
La evaporación solo ocurre en la superficie del líquido. Al aumentar el área superficial, expone más moléculas de disolvente a la fase gaseosa, acelerando drásticamente el proceso. Esta es la razón por la que un charco se evapora más rápido que la misma cantidad de agua en una taza profunda.
El papel del flujo de gas
Cuando un disolvente se evapora, crea una capa de vapor justo por encima de la superficie del líquido, lo que puede provocar la recondensación. Al soplar un chorro constante de gas inerte (como nitrógeno) sobre la superficie, elimina constantemente este vapor, lo que fomenta que más líquido se evapore para restablecer el equilibrio.
Métodos comunes de evaporación en laboratorio
Estos principios se aplican utilizando varios equipos de laboratorio estándar, cada uno adecuado para diferentes escalas y tipos de muestras.
Evaporación simple en campana extractora
Este es el método más básico. La muestra se coloca en un recipiente ancho y poco profundo (como un plato de evaporación o un vidrio de reloj) dentro de una campana extractora. El flujo de aire de la campana proporciona un suave flujo de gas para eliminar los vapores.
Este método solo es adecuado para volúmenes muy pequeños de disolventes no tóxicos y muy volátiles y para muestras que no son sensibles al aire o a la exposición prolongada.
Calentamiento en placa calefactora
Una forma sencilla de acelerar la evaporación es calentar suavemente la muestra en una placa calefactora dentro de una campana extractora. Esto aplica directamente el principio de aumentar la temperatura.
Aunque es rápido, este método ofrece un control deficiente de la temperatura y crea un alto riesgo de sobrecalentamiento o "bumping" (ebullición violenta), lo que puede provocar la pérdida y degradación de la muestra.
Evaporación por soplado de nitrógeno
También conocida como N-Evap, esta técnica utiliza un colector para dirigir múltiples chorros finos de gas nitrógeno sobre la superficie de las muestras en viales o una microplaca. A menudo incluye un calentamiento suave desde un bloque o baño de agua inferior.
Esto es muy eficaz para concentrar múltiples muestras de pequeño volumen simultáneamente y es común en la preparación de muestras para química analítica.
Evaporación rotatoria ("Rotovap")
El evaporador rotatorio es el caballo de batalla del laboratorio de química sintética. Combina todos los principios para una eliminación de disolvente eficiente y suave.
- Presión reducida: Una bomba de vacío reduce el punto de ebullición.
- Área superficial aumentada: El matraz se hace girar continuamente, cubriendo las paredes internas con una fina película de la muestra.
- Calentamiento suave: El matraz giratorio se coloca en un baño de agua para un calentamiento estable y controlado.
Este método es ideal para compuestos sensibles al calor y para eliminar disolventes de volúmenes que oscilan típicamente entre 25 ml y varios litros.
Evaporación centrífuga ("SpeedVac")
Un evaporador centrífugo (a menudo llamado SpeedVac) somete las muestras a un vacío profundo mientras las hace girar en una centrífuga. La fuerza centrífuga evita el bumping y se aplica un calor suave mediante radiación infrarroja.
Este es el estándar de oro para concentrar de forma segura muchas muestras pequeñas, valiosas o sensibles, como ADN, ARN o péptidos, sin ningún riesgo de contaminación cruzada o pérdida.
Comprensión de las compensaciones y los riesgos
Elegir un método requiere equilibrar la velocidad con los problemas potenciales. Ser consciente de estas compensaciones es fundamental para el éxito.
Degradación de la muestra
El riesgo principal es la degradación térmica. Muchos compuestos orgánicos y casi todas las moléculas biológicas pueden ser destruidos por el calor excesivo. Esta es la razón por la cual los métodos que utilizan presión reducida, como la evaporación rotatoria, son tan esenciales.
Bumping y pérdida de muestra
Cuando un líquido se calienta al vacío sin agitación, puede sobrecalentarse y luego hervir violentamente en una única erupción grande. Este fenómeno, llamado bumping, puede hacer que pierda una porción significativa de su muestra en el sistema de vacío. La rotación (en un rotovap) o la fuerza centrífuga (en un SpeedVac) se utilizan específicamente para prevenir esto.
Eliminación incompleta del disolvente
Los disolventes con puntos de ebullición altos, como DMSO o DMF, pueden ser difíciles de eliminar por completo. Incluso bajo un fuerte vacío, pueden quedar cantidades residuales, contaminando su producto final. Esto a veces se puede solucionar añadiendo un disolvente más volátil (como tolueno) y volviendo a evaporar, un proceso conocido como secado azeotrópico.
Tomar la decisión correcta para su muestra
Su decisión debe guiarse por las características de su muestra y su objetivo final.
- Si su muestra es térmicamente estable y el disolvente es volátil: La simple calefacción en una campana extractora o el soplado con nitrógeno pueden ser suficientes y rápidos.
- Si su muestra es térmicamente sensible o está en un volumen superior a 20 ml: Un evaporador rotatorio es la opción estándar y más fiable.
- Si tiene muchas muestras biológicas pequeñas y muy sensibles: Un evaporador centrífugo ofrece el mayor nivel de protección y eficiencia.
- Si su objetivo es aislar un producto con la máxima pureza: Elija siempre un método con vacío para utilizar la temperatura más baja posible, minimizando la formación de subproductos térmicos.
Al adaptar la técnica a las necesidades de su muestra, se asegura una eliminación eficiente del disolvente mientras maximiza la integridad y el rendimiento de su producto final.
Tabla de resumen:
| Método | Mejor para | Principio(s) clave |
|---|---|---|
| Evaporación simple | Pequeños volúmenes de disolventes no tóxicos y volátiles | Área superficial, Flujo de gas |
| Calentamiento en placa calefactora | Evaporación rápida de muestras térmicamente estables | Temperatura |
| Soplado de nitrógeno (N-Evap) | Concentración de múltiples muestras de pequeño volumen | Flujo de gas, Temperatura |
| Evaporación rotatoria (Rotovap) | Compuestos sensibles al calor; volúmenes de 25 ml a litros | Presión, Área superficial, Temperatura |
| Evaporación centrífuga (SpeedVac) | Muestras biológicas pequeñas, valiosas o sensibles | Presión, Fuerza centrífuga |
¿Necesita optimizar su proceso de evaporación de disolventes?
Elegir el equipo adecuado es fundamental para proteger sus muestras sensibles y maximizar el rendimiento. KINTEK se especializa en proporcionar equipos de laboratorio y consumibles fiables adaptados a las necesidades únicas de su laboratorio.
Ya sea que necesite un evaporador rotatorio suave para sus flujos de trabajo de química sintética o un evaporador centrífugo de alto rendimiento para muestras biológicas valiosas, tenemos la solución.
Permita que nuestros expertos le ayuden a mejorar la eficiencia de su laboratorio y la integridad de la muestra.
Contacte con KINTEK hoy mismo para encontrar el sistema de evaporación perfecto para su aplicación.
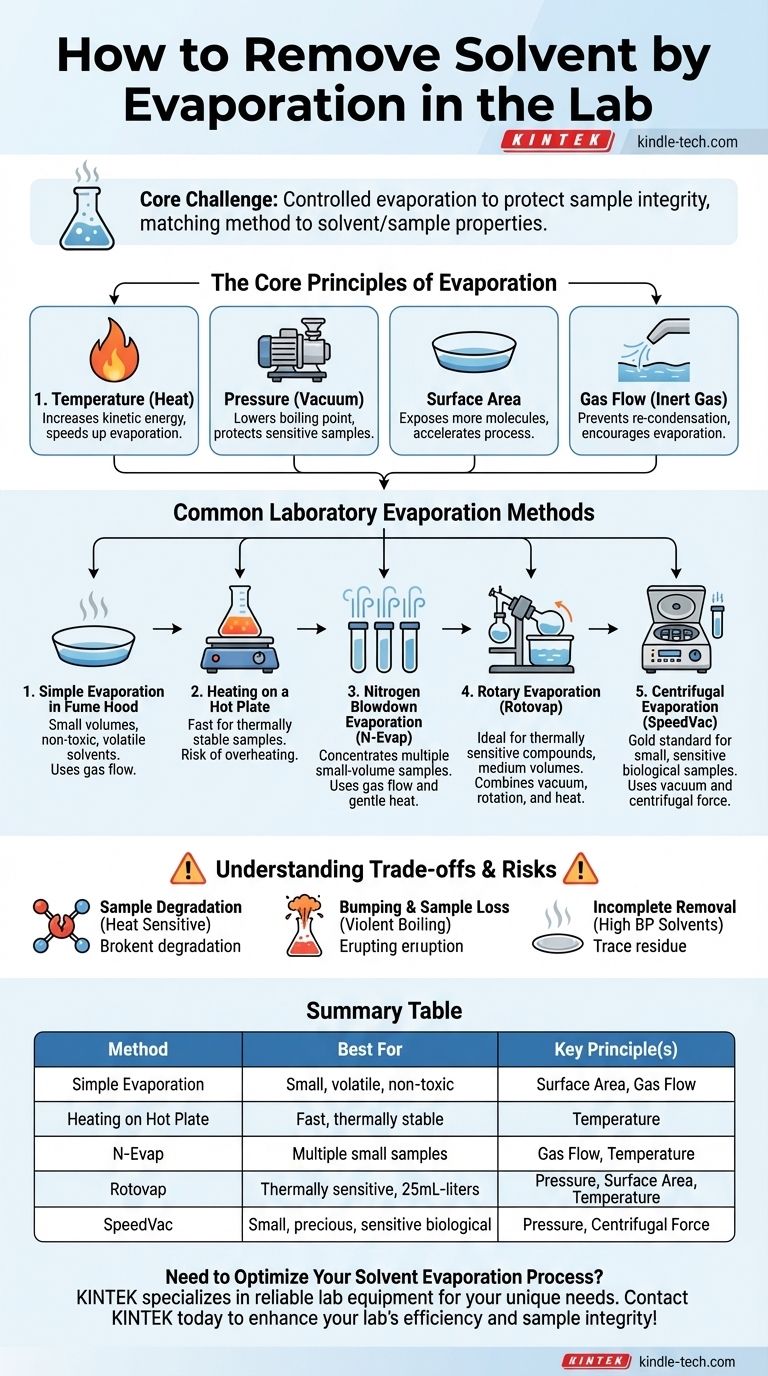
Guía Visual
Productos relacionados
- Equipo de horno de tubo para deposición química de vapor asistida por plasma (PECVD) rotatorio inclinado
- Horno tubular de equipo PECVD de deposición química de vapor mejorada por plasma rotatorio inclinado
- Horno de Tubo Rotatorio de Laboratorio con Inclinación al Vacío
- Horno de tubo rotatorio dividido con múltiples zonas de calentamiento
- Horno de tubo rotatorio de funcionamiento continuo sellado al vacío Horno de tubo giratorio
La gente también pregunta
- ¿Cómo funciona el proceso PECVD? Lograr películas delgadas de alta calidad a baja temperatura
- ¿Cuál es el proceso de PECVD en semiconductores? Habilitando la deposición de películas delgadas a baja temperatura
- ¿Cómo facilita la PECVD las películas nanocompuestas de Ru-C? Síntesis de películas delgadas de precisión a baja temperatura
- ¿Cómo funciona la deposición química de vapor asistida por plasma? Permite la deposición de películas delgadas a baja temperatura
- ¿Cuáles son las ventajas principales del PE-CVD en el encapsulamiento de OLED? Proteja las capas sensibles con deposición de película a baja temperatura



















