En cualquier sistema electroquímico, el propósito de un electrodo de referencia es proporcionar un potencial estable, constante y bien conocido. Actúa como una línea base fija, o punto cero, contra el cual se puede medir el potencial de un segundo electrodo, el electrodo de trabajo. Al completar el circuito eléctrico, hace posible una medición significativa.
No se puede medir el potencial de un solo electrodo de forma aislada; el potencial es siempre una diferencia entre dos puntos. El electrodo de referencia proporciona una mitad confiable e inmutable del sistema, asegurando que cualquier cambio que mida se deba únicamente a la reacción química que está estudiando en el electrodo de trabajo.

La base de la medición electroquímica
Para comprender el electrodo de referencia, primero debe entender que cada medición electroquímica requiere dos electrodos para formar una celda completa. El electrodo de referencia es uno de estos componentes esenciales.
Proporcionar una línea base estable
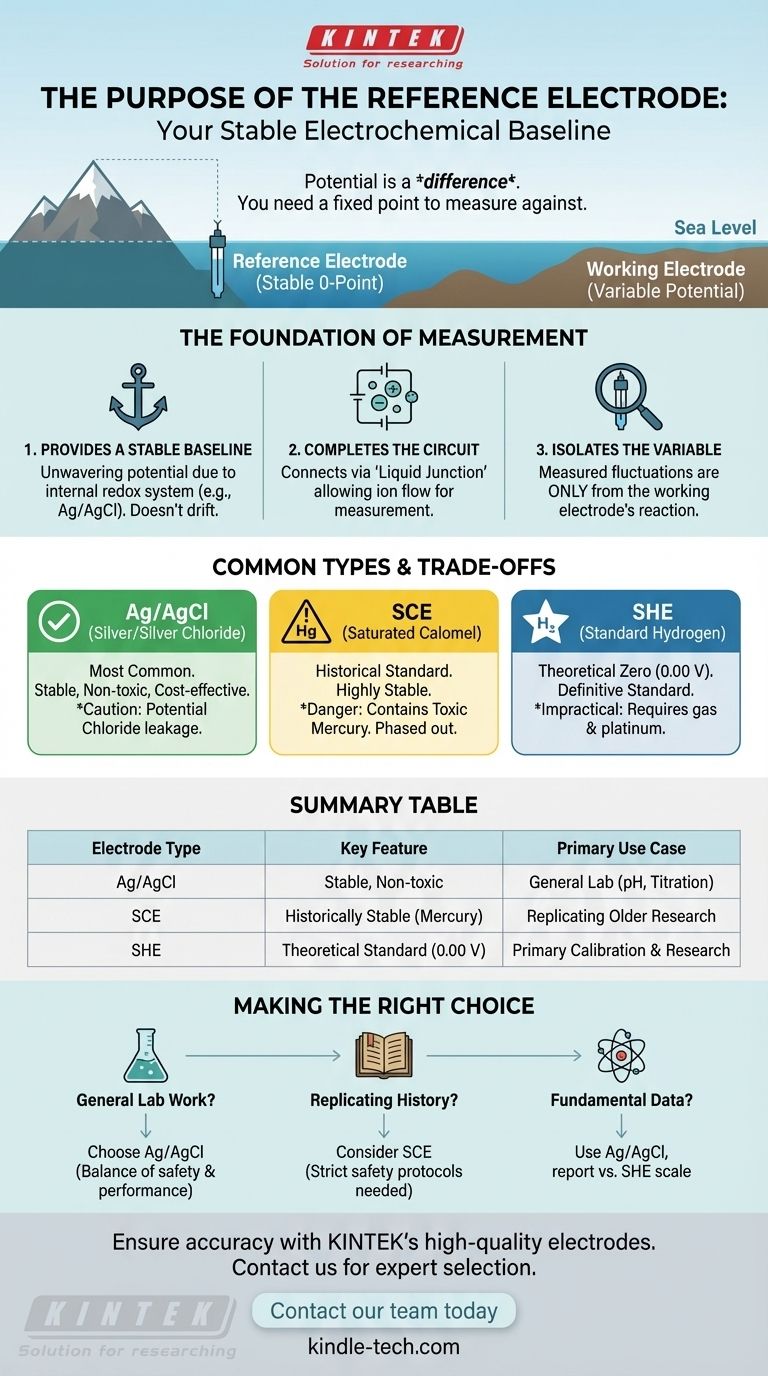
El potencial es un valor relativo, muy parecido a la altura de una montaña medida con respecto al nivel del mar. El electrodo de referencia actúa como el "nivel del mar" inquebrantable para su medición.
Su química interna está cuidadosamente diseñada utilizando un sistema redox (como plata y cloruro de plata) con soluciones saturadas o tamponadas. Esto asegura que su propio potencial no se desvíe ni cambie durante el experimento.
Completar el circuito eléctrico
Una línea base teórica es inútil sin una conexión física. El electrodo de referencia hace contacto con la solución de muestra a través de un componente llamado unión líquida.
Esta unión permite el flujo de iones, completando el circuito eléctrico entre el electrodo de referencia y el de trabajo. Sin esta conexión, no se podría tomar ninguna medición.
Aislar la variable de interés
Al proporcionar un potencial constante, el electrodo de referencia permite que el potencial total medido de la celda refleje solo lo que está sucediendo en el electrodo de trabajo.
Por lo tanto, cualquier fluctuación detectada es atribuible directamente a la concentración del analito o a la reacción que se está estudiando, que es el objetivo de toda la medición.
Tipos comunes y sus compensaciones
Aunque todos los electrodos de referencia sirven para el mismo propósito, no están hechos de la misma manera. La elección del electrodo implica compensaciones prácticas en estabilidad, costo y seguridad.
Plata/Cloruro de Plata (Ag/AgCl)
Este es el electrodo de referencia más utilizado en la actualidad. Es conocido por ser relativamente económico, altamente estable y no tóxico.
Su principal inconveniente es la posibilidad de que la solución interna del puente salino (cloruro de potasio) se filtre en la muestra, lo que puede ser un problema en aplicaciones sensibles a los iones cloruro.
Electrodo de Calomel Saturado (ECS)
El ECS es un electrodo históricamente significativo, famoso por su excepcional estabilidad y fiabilidad. Una vez fue un estándar de laboratorio.
Sin embargo, contiene mercurio, que es altamente tóxico. Debido a preocupaciones de seguridad y desafíos de eliminación, su uso ha sido en gran parte eliminado en favor del electrodo Ag/AgCl.
Electrodo Estándar de Hidrógeno (EEH)
El EEH es el referente teórico definitivo contra el cual se definen todos los demás potenciales de electrodo. Su potencial se establece exactamente en 0.00 voltios por convención.
A pesar de su importancia como estándar, el EEH es extremadamente impráctico para el uso diario. Requiere un suministro constante de gas hidrógeno inflamable y un electrodo de platino especialmente preparado, lo que lo hace adecuado solo para la calibración primaria y la investigación.
Tomar la decisión correcta para su objetivo
Su elección de electrodo de referencia generalmente se guía por los requisitos de compatibilidad, precisión y seguridad de su aplicación.
- Si su enfoque principal es el trabajo general de laboratorio (p. ej., pH, titulación): El electrodo de Plata/Cloruro de Plata (Ag/AgCl) es la opción estándar por su excelente equilibrio entre rendimiento, seguridad y costo.
- Si su enfoque principal es replicar investigaciones antiguas: Es posible que deba utilizar un Electrodo de Calomel Saturado (ECS) para mantener la coherencia con los datos históricos, pero debe cumplir con protocolos de seguridad estrictos.
- Si su enfoque principal es establecer datos electroquímicos fundamentales: Utilizará un electrodo práctico como el Ag/AgCl, pero informará sus resultados relativos a la escala del Electrodo Estándar de Hidrógeno (EEH) para una comparación universal.
En última instancia, el electrodo de referencia es una herramienta simple pero crítica que elimina la ambigüedad, permitiéndole concentrarse en la química que importa.
Tabla de resumen:
| Tipo de electrodo | Característica clave | Caso de uso principal |
|---|---|---|
| Plata/Cloruro de Plata (Ag/AgCl) | Estable, no tóxico, rentable | Trabajo general de laboratorio (pH, titulación) |
| Calomel Saturado (ECS) | Históricamente estable, contiene mercurio | Replicación de investigaciones antiguas (con protocolos de seguridad) |
| Hidrógeno Estándar (EEH) | Estándar teórico (0.00 V) | Calibración primaria e investigación fundamental |
Asegure la precisión y fiabilidad de sus experimentos electroquímicos con el electrodo de referencia adecuado.
KINTEK se especializa en equipos y consumibles de laboratorio de alta calidad, incluida una gama de electrodos de referencia confiables adaptados a las necesidades del laboratorio. Nuestros expertos pueden ayudarle a seleccionar el electrodo ideal para su aplicación específica, garantizando mediciones precisas y estables.
¡Contacte a nuestro equipo hoy para discutir sus requisitos y mejorar las capacidades analíticas de su laboratorio!
Guía Visual
Productos relacionados
- Electrodo de Referencia Calomel Plata Cloruro Mercurio Sulfato para Uso en Laboratorio
- Electrodo de Referencia de Sulfato de Cobre para Uso en Laboratorio
- Electrodo Electroquímico de Disco Metálico
- Electrodo de Hoja de Oro Electrodos de Oro para Electroquímica
- Electrodo de lámina de platino para aplicaciones de laboratorio de baterías
La gente también pregunta
- ¿Qué tipo de electrodo se puede utilizar como punto de referencia? Seleccione el adecuado para mediciones precisas
- ¿Qué es el electrodo de referencia en potenciometría? La clave para mediciones estables y precisas
- ¿Qué electrodo se utiliza como electrodo de referencia para medir potenciales de semicelda? Comprendiendo el Estándar Universal
- ¿Qué electrodo se utiliza como referencia de tierra? Domine la clave para mediciones electroquímicas precisas
- ¿Por qué es fundamental la selección de un electrodo de referencia de alta calidad en la síntesis electroquímica? | KINTEK


















