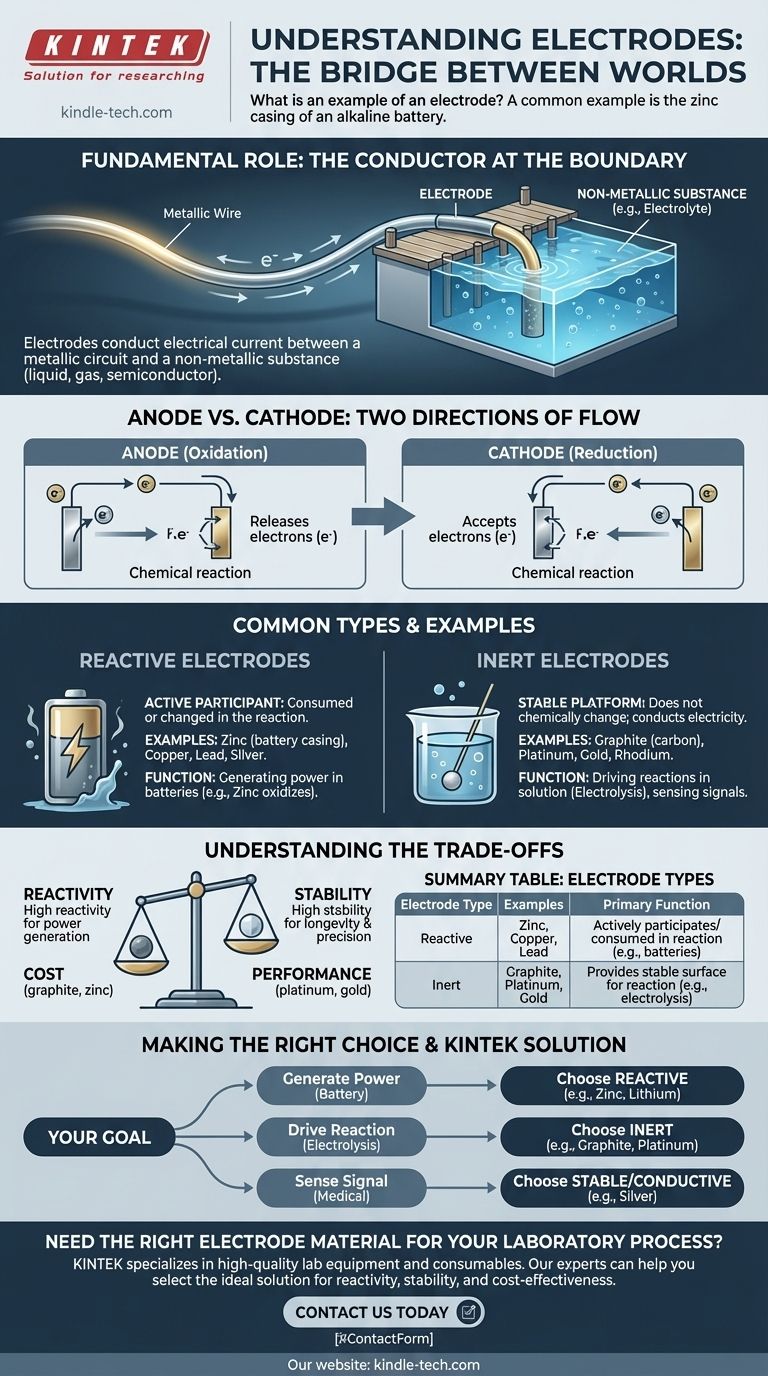
Un ejemplo común de electrodo es la carcasa de zinc de una batería alcalina o la parte superior de cobre de una batería de 9 voltios. Estos materiales actúan como conductores eléctricos que hacen contacto con la pasta química no metálica (el electrolito) dentro de la batería, permitiendo que fluya una corriente eléctrica y alimente su dispositivo.
Un electrodo es fundamentalmente un puente. Su función es conducir corriente eléctrica entre un cable metálico estándar y una sustancia no metálica, como un líquido, gas o semiconductor, lo que permite una amplia gama de procesos químicos y electrónicos.

¿Cuál es el papel fundamental de un electrodo?
Un electrodo sirve como el punto de contacto crucial donde un circuito eléctrico se encuentra con un componente no metálico. Sin este puente, muchas tecnologías serían imposibles.
El conductor en el límite
Piense en un electrodo como un muelle para la electricidad. Un cable es como un camino que lleva la electricidad al borde de un lago (la sustancia no metálica, como un electrolito). El electrodo es el muelle que permite que la electricidad entre o salga del agua.
Esta parte no metálica puede ser un electrolito líquido en una batería, un semiconductor en un diodo o incluso el cuerpo humano en un dispositivo médico.
Ánodo vs. Cátodo: Las dos direcciones del flujo
En sistemas electroquímicos como las baterías, los electrodos reciben nombres específicos según la dirección de la reacción.
- Un ánodo es el electrodo donde ocurre la oxidación, lo que significa que libera electrones al circuito.
- Un cátodo es el electrodo donde ocurre la reducción, lo que significa que acepta electrones del circuito.
Tipos y ejemplos comunes
Los electrodos no son todos iguales; su material se elige en función de si deben participar en una reacción o simplemente observarla.
Electrodos reactivos
Un electrodo reactivo es un participante activo en una reacción química. Se consume o cambia durante el proceso.
La carcasa de zinc de una batería es un ejemplo perfecto. A medida que la batería se descarga, el metal de zinc se oxida y se disuelve lentamente en el electrolito, liberando los electrones que alimentan su dispositivo. Otros electrodos reactivos comunes incluyen cobre, plomo y plata.
Electrodos inertes
Un electrodo inerte actúa como una plataforma estable y no participante para que ocurra una reacción. Conduce electricidad pero no cambia químicamente.
El grafito (una forma de carbono) es un electrodo inerte ampliamente utilizado porque es un excelente conductor y es relativamente económico. El platino, el oro y el rodio también se utilizan por su extrema resistencia a la reacción, aunque son mucho más costosos.
Comprendiendo las compensaciones
La elección del material del electrodo es una decisión de ingeniería crítica basada en la función y el entorno previstos.
Reactividad vs. Estabilidad
La principal compensación es entre reactividad y estabilidad. Para una batería de un solo uso, usted quiere un electrodo reactivo que pueda consumirse para generar energía.
Sin embargo, para un proceso como la electrólisis (usar electricidad para dividir el agua), necesita un electrodo inerte como el platino o el grafito. Usar un electrodo reactivo como el zinc haría que el propio electrodo reaccionara con el agua en lugar de dividirla.
Costo vs. Rendimiento
Los metales altamente inertes como el oro y el platino ofrecen un rendimiento y una longevidad superiores, ya que resisten la corrosión y las reacciones secundarias no deseadas.
Sin embargo, su alto costo los hace inadecuados para muchas aplicaciones. El grafito ofrece un buen equilibrio entre inercia y conductividad a una fracción del precio, lo que lo hace ideal para procesos industriales a gran escala.
Tomando la decisión correcta para su objetivo
Al observar el material y su aplicación, puede comprender rápidamente el propósito de un electrodo dado.
- Si su objetivo principal es generar energía en una batería: Los electrodos estarán hechos de materiales reactivos como zinc, litio o plomo, elegidos específicamente para ser consumidos en una reacción química.
- Si su objetivo principal es impulsar una reacción en una solución (electrólisis): Los electrodos serán materiales inertes como grafito o platino que pueden conducir corriente sin interferir.
- Si su objetivo principal es detectar una señal eléctrica: Los electrodos (como en los dispositivos médicos) estarán hechos de materiales conductores y estables como la plata que pueden transmitir con precisión pequeñas corrientes de una fuente no metálica como el cuerpo.
En última instancia, ver un electrodo como el puente entre los mundos metálico y no metálico es clave para comprender su función en cualquier dispositivo.
Tabla resumen:
| Tipo de electrodo | Ejemplos comunes | Función principal |
|---|---|---|
| Reactivo | Zinc, Cobre, Plomo | Participa activamente y es consumido por una reacción química (p. ej., en baterías). |
| Inerte | Grafito, Platino, Oro | Proporciona una superficie estable para una reacción sin ser consumido (p. ej., en electrólisis). |
¿Necesita el material de electrodo adecuado para su proceso de laboratorio? Elegir el electrodo correcto es fundamental para el éxito y la eficiencia de sus experimentos, ya sea que esté desarrollando nuevas tecnologías de baterías o realizando una electrólisis precisa. KINTEK se especializa en equipos y consumibles de laboratorio de alta calidad, incluida una amplia gama de materiales para electrodos. Nuestros expertos pueden ayudarlo a seleccionar la solución ideal en cuanto a reactividad, estabilidad y rentabilidad. Contáctenos hoy para discutir sus necesidades específicas y permítanos ser su socio en la innovación.
Guía Visual
Productos relacionados
- Electrodo de Referencia Calomel Plata Cloruro Mercurio Sulfato para Uso en Laboratorio
- Electrodo Electroquímico de Disco Metálico
- Electrodo de disco giratorio (disco de anillo) RRDE / compatible con PINE, ALS japonés, Metrohm suizo de carbono vítreo platino
- Electrodo de disco de platino giratorio para aplicaciones electroquímicas
- Electrodo de lámina de platino para aplicaciones de laboratorio de baterías
La gente también pregunta
- ¿Qué es el electrodo de referencia en potenciometría? La clave para mediciones estables y precisas
- ¿Qué electrodo se utiliza como electrodo de referencia para medir potenciales de semicelda? Comprendiendo el Estándar Universal
- ¿Qué tipo de electrodo se puede utilizar como punto de referencia? Seleccione el adecuado para mediciones precisas
- ¿Cómo se correlaciona la selección de electrodos de referencia, como Ag/AgCl o Hg/HgO, con el pH del electrolito en las pruebas de reacción de evolución de hidrógeno (HER)?
- ¿Por qué es fundamental la selección de un electrodo de referencia de alta calidad en la síntesis electroquímica? | KINTEK



















