Requisitos para el uso de electrodos de referencia
Electrodo no polarizado ideal
Un electrodo ideal no polarizado es la piedra angular de las mediciones electroquímicas, ya que proporciona un punto de referencia estable y fiable.Este tipo de electrodo se caracteriza por su excelente reversibilidad, que garantiza que el potencial del electrodo permanezca constante independientemente de la dirección del flujo de corriente.Un potencial estable es crucial, ya que minimiza las fluctuaciones y los errores en las mediciones, mejorando así la precisión y la fiabilidad de los datos obtenidos.
Además, la reproducibilidad del potencial de un electrodo no polarizado ideal es primordial.Esto significa que el electrodo debe producir sistemáticamente el mismo potencial en condiciones idénticas, eliminando las discrepancias en experimentos repetidos.Esta reproducibilidad es esencial para el rigor científico y para garantizar que los resultados experimentales puedan compararse y reproducirse de forma fiable.
Para ilustrar estas cualidades, considere la siguiente tabla en la que se comparan las características de los electrodos de referencia ideales y no ideales:
| Característica | Electrodo de referencia ideal | Electrodo de referencia no ideal |
|---|---|---|
| Reversibilidad del electrodo | Alta | Bajo |
| Estabilidad potencial | Alta | Variable |
| Reproducibilidad potencial | Alta | Bajo |
En resumen, un electrodo no polarizado ideal debe presentar una alta reversibilidad del electrodo, un potencial estable y una excelente reproducibilidad del potencial para funcionar eficazmente como referencia en estudios electroquímicos.
Coeficiente de temperatura y mantenimiento
El coeficiente de temperatura de un electrodo de referencia es un parámetro crítico que influye en su rendimiento y fiabilidad.Lo ideal es que el electrodo presente un coeficiente de temperatura mínimo, que garantice que su potencial permanezca estable en condiciones ambientales variables.Esta estabilidad es crucial para obtener mediciones precisas en experimentos electroquímicos, en los que incluso pequeñas fluctuaciones de potencial pueden dar lugar a errores significativos.
Además de un coeficiente de temperatura pequeño, el electrodo debe ser fácil de usar en términos de fabricación, funcionamiento y mantenimiento.La facilidad de fabricación garantiza una calidad y disponibilidad constantes, mientras que el uso sencillo simplifica la configuración experimental y reduce la probabilidad de errores operativos.Los requisitos de mantenimiento deben ser mínimos, lo que permite un uso a largo plazo sin calibraciones ni sustituciones frecuentes.
| Aspecto | Características ideales | Importancia |
|---|---|---|
| Coeficiente de temperatura | Pequeño | Garantiza un potencial estable a distintas temperaturas |
| Fabricación | Fácil de fabricar | Garantiza una calidad y disponibilidad constantes |
| Utilización | Sencillo e intuitivo | Simplifica la configuración experimental y reduce los errores |
| Mantenimiento | Mínimo | Permite un uso a largo plazo sin intervenciones frecuentes |
Centrándose en estos aspectos, los investigadores pueden seleccionar y mantener electrodos de referencia que proporcionen datos fiables y precisos, contribuyendo al éxito de sus estudios electroquímicos.
Condiciones de uso de los distintos electrodos de referencia
Clasificación en función del pH
A la hora de seleccionar un electrodo de referencia para experimentos electroquímicos, el pH del electrolito es un factor crítico.Los distintos electrodos de referencia están diseñados específicamente para funcionar de forma óptima en condiciones de pH variables, garantizando mediciones precisas y estables.
Condiciones ácidas
Para ambientes con pH bajo, electrodos de calomelano .Estos electrodos son fiables en entornos ácidos debido a su estabilidad y al hecho de que no reaccionan con las soluciones ácidas.El electrodo de calomelano está formado por mercurio en contacto con una pasta de cloruro de mercurio (I) (calomelano) y una solución de cloruro potásico, que proporciona un potencial estable.

Condiciones neutras
En entornos de pH neutro los electrodos de cloruro de plata son los preferidos.Este tipo de electrodo está compuesto por un hilo de plata recubierto de cloruro de plata, que se sumerge en una solución de cloruro potásico o cloruro sódico.El electrodo de cloruro de plata ofrece una excelente estabilidad y un bajo coeficiente de temperatura, lo que lo hace adecuado para una amplia gama de aplicaciones.
Condiciones alcalinas
Para entornos con pH elevado, electrodos de óxido de mercurio-mercurio se utilizan.Estos electrodos están hechos de mercurio en contacto con una pasta de óxido de mercurio y solución de hidróxido de potasio.El electrodo de mercurio-óxido de mercurio es estable en condiciones alcalinas y proporciona un potencial constante, lo que resulta crucial para realizar mediciones precisas en dichos entornos.
| Tipo de electrodo | Rango óptimo de pH | Componentes |
|---|---|---|
| Electrodo de Calomel | Ácido (pH bajo) | Mercurio, pasta de cloruro de mercurio (I), solución de cloruro de potasio |
| Electrodo de cloruro de plata | Neutro (pH medio) | Alambre de plata recubierto con solución de cloruro de plata, cloruro de potasio o cloruro de sodio |
| Electrodo de mercurio-óxido de mercurio | Alcalino (pH alto) | Mercurio, pasta de óxido de mercurio, solución de hidróxido de potasio |
Comprender los requisitos específicos de pH para cada tipo de electrodo de referencia garantiza la elección del electrodo más adecuado, mejorando así la precisión y fiabilidad de las mediciones electroquímicas.
Casos especiales y electrolitos orgánicos
En situaciones específicas, como las que implican ácido sulfúrico o soluciones de sulfato, se emplean electrodos de sulfato mercúrico de mercurio debido a su compatibilidad con estos entornos agresivos.Estos electrodos son especialmente eficaces para mantener potenciales estables y garantizar mediciones precisas en condiciones tan agresivas.
En el ámbito de la tecnología de baterías, los electrodos de hidróxido de cadmio son los más utilizados.Estos electrodos se eligen por su capacidad para soportar las exigencias cíclicas del funcionamiento de las baterías, proporcionando un rendimiento fiable durante periodos prolongados.
Para aplicaciones con electrolitos orgánicos, los electrodos de plata y ferroceno suelen ser los preferidos.Los electrodos de plata se valoran por su estabilidad y baja reactividad con compuestos orgánicos, mientras que los electrodos de ferroceno ofrecen ventajas únicas en cuanto a sus propiedades redox y compatibilidad con medios orgánicos.
| Tipo de electrolito | Electrodo preferido | Ventajas clave |
|---|---|---|
| Soluciones de ácido sulfúrico | Sulfato mercúrico de mercurio | Compatibilidad con entornos agresivos, potencial estable |
| Industria de baterías | Hidróxido de cadmio | Resistencia en operaciones cíclicas de baterías, rendimiento fiable |
| Electrolitos orgánicos | Plata y ferroceno | Estabilidad con compuestos orgánicos, propiedades redox únicas |
Esta tabla resume los electrodos preferidos para diferentes tipos de electrolitos, destacando sus ventajas clave en diversas aplicaciones.
Por qué diferentes electrodos de referencia se aplican a diferentes condiciones
Reacción del electrodo y ecuación de Nernst
Los distintos electrodos se adaptan a condiciones específicas en función de sus reacciones electroquímicas únicas y de los potenciales de electrodo de equilibrio estándar resultantes, que se calculan meticulosamente mediante la ecuación de Nernst.Esta ecuación, que debe su nombre al químico alemán Walther Nernst, es fundamental en electroquímica, ya que relaciona el potencial de reducción de una reacción electroquímica con el potencial de electrodo estándar y las actividades de las especies que reaccionan.
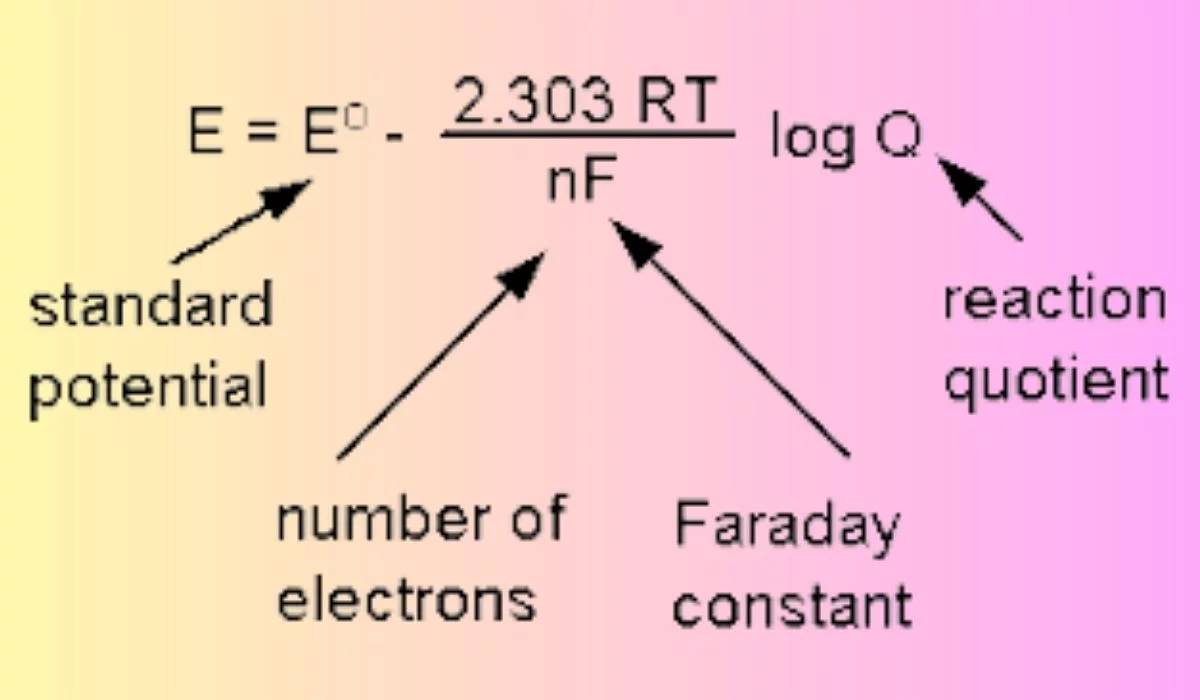
Por ejemplo, el potencial de electrodo de equilibrio estándar de un electrodo de cloruro de plata, utilizado a menudo en entornos neutros, está influido por la concentración de iones de cloruro y la presión parcial del gas hidrógeno.Por el contrario, un electrodo de calomelano, favorecido en condiciones ácidas, funciona bajo principios termodinámicos diferentes, garantizando la estabilidad y la precisión en el entorno designado.
| Tipo de electrodo | Condiciones adecuadas | Reacción clave | Potencial de equilibrio estándar (V) |
|---|---|---|---|
| Cloruro de plata | Neutro | AgCl + e- → Ag + Cl- | 0.2223 |
| Calomel | Ácido | Hg₂Cl₂ + 2e- → 2Hg + 2Cl- | 0.2682 |
| Óxido de mercurio-mercurio | Alcalino | HgO + H₂O + 2e- → Hg + 2OH- | 0.0977 |
La selección de un electrodo adecuado es crucial, ya que influye directamente en la precisión y fiabilidad de las mediciones electroquímicas.La idoneidad de cada electrodo viene determinada por su capacidad para mantener un potencial estable en condiciones variables, garantizando que la ecuación de Nernst prediga con exactitud el comportamiento del electrodo.Esta precisión es esencial para aplicaciones que van desde la monitorización medioambiental a la tecnología de baterías, donde incluso pequeñas desviaciones pueden dar lugar a errores significativos.
En resumen, la ecuación de Nernst no sólo cuantifica la relación entre el potencial del electrodo y las condiciones de reacción, sino que también subraya la importancia de elegir el electrodo adecuado para aplicaciones específicas.Esto garantiza que los experimentos electroquímicos produzcan resultados precisos y reproducibles, en línea con los objetivos más amplios de la investigación científica y la práctica industrial.
Estabilidad y desventajas
El electrodo de cloruro de plata es un buen ejemplo de cómo las condiciones específicas pueden afectar a la estabilidad y precisión de los electrodos de referencia.En condiciones alcalinas, el uso prolongado de este electrodo puede provocar la formación de óxido de plata.Esta reacción no sólo compromete la estabilidad del electrodo, sino que también disminuye su precisión, afectando así a la fiabilidad de las mediciones realizadas.
En ambientes alcalinos, la reacción química puede resumirse de la siguiente manera:
- Cloruro de plata (AgCl) + Hidróxido (OH-) → Óxido de plata (Ag₂O) + Cloruro (Cl-).
Esta transformación altera significativamente el potencial del electrodo, haciéndolo menos predecible y más propenso a errores.La inestabilidad introducida por la formación de óxido de plata requiere una cuidadosa consideración a la hora de seleccionar y utilizar electrodos de referencia en tales condiciones.
Para mitigar estos inconvenientes, a menudo se recomienda emplear un sistema de doble puente salino.Este método ayuda a mantener la estabilidad del electrodo de cloruro de plata en condiciones alcalinas, garantizando lecturas más precisas y fiables.
Mitigación de los inconvenientes con puentes salinos
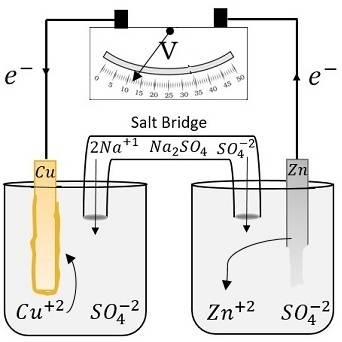
En condiciones alcalinas, los electrodos de cloruro de plata pueden tener problemas de estabilidad debido a la formación de óxido de plata con el tiempo, lo que afecta a la precisión y fiabilidad de las mediciones.Para contrarrestar estos inconvenientes, el empleo de un sistema de doble puente salino es una estrategia eficaz.
Un sistema de doble puente salino implica el uso de dos puentes salinos separados, cada uno lleno de un electrolito apropiado.Esta configuración ayuda a aislar el electrodo de referencia de la solución de prueba, reduciendo así el riesgo de contaminación y minimizando la interacción que podría conducir a la formación de óxido de plata.Al crear una zona tampón, el sistema de doble puente salino garantiza que el electrodo de referencia permanezca estable, incluso en entornos alcalinos difíciles.
Este método no sólo preserva la integridad del electrodo de cloruro de plata, sino que también mejora la precisión general de las mediciones electroquímicas.El doble aislamiento proporcionado por los puentes salinos actúa como una barrera protectora, permitiendo una recogida de datos más consistente y fiable en condiciones alcalinas.
Productos relacionados
- Electrodo de Referencia Calomel Plata Cloruro Mercurio Sulfato para Uso en Laboratorio
- Electrodo de Referencia de Sulfato de Cobre para Uso en Laboratorio
- Electrodo Electroquímico de Disco Metálico
- Electrodo Electrolítico de Grafito en Disco y Varilla de Grafito
- Electrodo electroquímico de carbono vítreo
Artículos relacionados
- Una guía para principiantes para comprender los electrodos de referencia en electroquímica
- Electrodos de referencia comunes en estudios electroquímicos
- Diseño y aplicación de electrodos de referencia en baterías de litio
- Guía completa de electrodos de referencia: Tipos, aplicaciones y criterios de selección
- Cómo elegir el electrodo de referencia adecuado para su aplicación



















