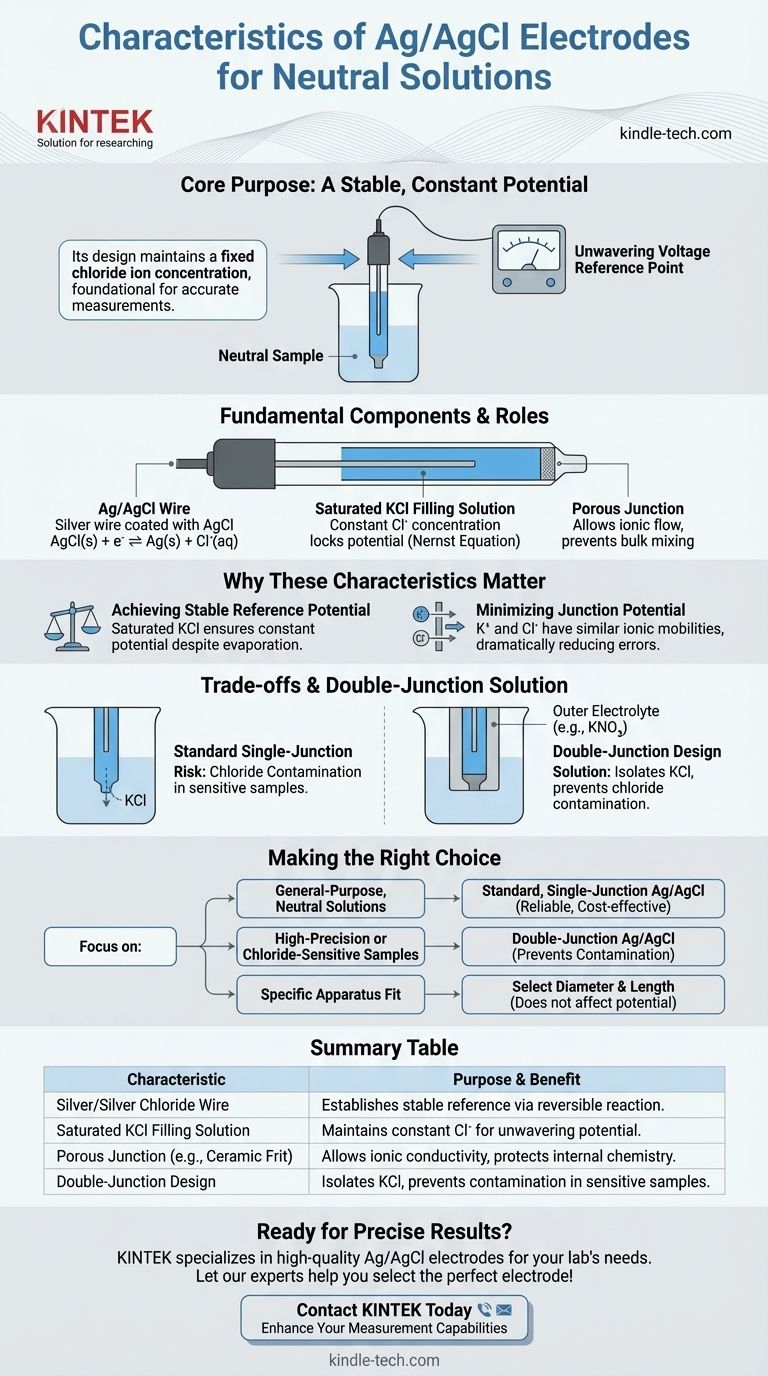
En esencia, un electrodo de plata/cloruro de plata (Ag/AgCl) diseñado para soluciones neutras es un electrodo de referencia que proporciona un potencial estable y constante. Su característica clave es el uso de un hilo de plata recubierto de cloruro de plata, que se sumerge en una solución saturada de cloruro de potasio (KCl) para mantener una concentración fija de iones cloruro.
El propósito de un electrodo de Ag/AgCl no es reaccionar con su muestra, sino proporcionar un punto de referencia de voltaje inquebrantable y conocido. Su diseño, centrado en una solución saturada de KCl, asegura esta estabilidad, que es la base para cualquier medición electroquímica precisa.

Los componentes fundamentales y su función
Para comprender el rendimiento del electrodo, primero debe comprender su construcción. Cada parte cumple una función precisa para garantizar un potencial estable.
El elemento plata/cloruro de plata
El corazón del electrodo es un hilo de plata pura recubierto con una capa de cloruro de plata (AgCl). Este elemento es donde ocurre la reacción electroquímica fundamental.
El potencial se establece por el equilibrio entre la plata/cloruro de plata sólida y los iones cloruro (Cl⁻) en la solución de llenado: AgCl(s) + e⁻ ⇌ Ag(s) + Cl⁻(aq).
La solución de llenado de KCl saturado
Para su uso en soluciones neutras, el electrodo se llena con una solución saturada de cloruro de potasio (KCl). Esta es la característica más crítica para la estabilidad.
Debido a que la solución está saturada, la concentración de iones cloruro se mantiene constante a un nivel alto y conocido. Según la ecuación de Nernst, esta concentración constante de cloruro fija el potencial del electrodo, convirtiéndolo en una referencia confiable.
La unión porosa
Una frita porosa, típicamente hecha de cerámica o cuarzo, separa la solución de llenado interna de la solución de muestra externa.
Esta unión permite que los iones fluyan entre el electrodo y la muestra, completando el circuito eléctrico. Sin embargo, evita la mezcla a granel de las dos soluciones, protegiendo la química interna del electrodo de referencia.
Por qué estas características son importantes para su medición
Los componentes específicos de un electrodo de Ag/AgCl se eligen deliberadamente para resolver problemas comunes en electroquímica, asegurando que sus resultados sean precisos y reproducibles.
Lograr un potencial de referencia estable
El propósito completo de un electrodo de referencia es tener un potencial que no cambie durante su experimento.
Al usar una solución saturada de KCl, la concentración de cloruro permanece constante incluso si una pequeña cantidad de agua se evapora o difunde. Esta concentración constante asegura un potencial de referencia sólido como una roca contra el cual puede medir su electrodo de trabajo.
Minimizar el potencial de unión
Una fuente importante de error en las mediciones electroquímicas es el potencial de unión líquida. Este es un pequeño voltaje que se desarrolla en la interfaz entre la solución de llenado y la solución de su muestra debido a las diferencias en las tasas de difusión iónica.
El cloruro de potasio (KCl) se usa específicamente porque las movilidades iónicas del ion potasio (K⁺) y el ion cloruro (Cl⁻) son casi idénticas. Esta similitud hace que se difundan a través de la unión casi a la misma velocidad, lo que minimiza drásticamente el potencial de unión y mejora la precisión de la medición.
Comprendiendo las compensaciones y variaciones
Aunque el electrodo estándar de Ag/AgCl es un caballo de batalla, no es universalmente perfecto. Comprender sus limitaciones es clave para evitar errores de medición.
El riesgo de contaminación por cloruro
La principal compensación es que una pequeña cantidad de la solución de llenado de KCl se filtrará inevitablemente desde la unión porosa hacia su muestra.
Para la mayoría de las soluciones neutras, esto no es un problema. Sin embargo, si su experimento es sensible a los iones cloruro, por ejemplo, si está midiendo bajas concentraciones de cloruro o trabajando con muestras que precipitan con cloruro (como el nitrato de plata), esta fuga introducirá errores significativos.
El papel del electrodo de doble unión
Para resolver el problema de la contaminación por cloruro, se utiliza un electrodo de doble unión. Este diseño presenta una segunda cámara exterior que aísla la solución de KCl de la muestra.
Esta cámara exterior se puede llenar con un electrolito no interferente, como nitrato de potasio (KNO₃) o sulfato de sodio (Na₂SO₄). Proporciona el puente iónico a la muestra sin introducir iones cloruro, preservando la integridad de su muestra.
Consideraciones de diseño físico
Los electrodos están disponibles en varios diámetros (por ejemplo, 4 mm, 6 mm, 10 mm) y longitudes. Estas características físicas no afectan el potencial del electrodo, pero se eligen en función de las limitaciones de su celda electroquímica, el volumen de su muestra y la durabilidad requerida.
Tomar la decisión correcta para su objetivo
Seleccionar el electrodo correcto es un paso crítico para adquirir datos confiables. Su elección depende directamente de la naturaleza química de su muestra.
- Si su enfoque principal son las mediciones de propósito general en soluciones neutras: Un electrodo estándar de Ag/AgCl de unión simple con KCl saturado es la opción confiable y rentable.
- Si su enfoque principal son las mediciones de alta precisión o muestras sensibles al cloruro: Debe usar un electrodo de Ag/AgCl de doble unión para evitar la contaminación de la muestra y garantizar la precisión de los datos.
- Si su enfoque principal es encajar en un aparato específico: Seleccione el diámetro y la longitud del electrodo que coincidan físicamente con el diseño de su celda electroquímica.
Comprender cómo estos componentes crean una referencia estable es la clave para generar resultados electroquímicos confiables y reproducibles.
Tabla resumen:
| Característica | Propósito y Beneficio |
|---|---|
| Hilo de plata/cloruro de plata | Elemento central; establece un potencial de referencia estable mediante una reacción reversible. |
| Solución de llenado de KCl saturado | Mantiene una concentración constante de iones cloruro para un potencial inquebrantable, incluso con una evaporación menor. |
| Unión porosa (por ejemplo, frita cerámica) | Permite la conductividad iónica mientras evita la mezcla a granel de soluciones, protegiendo la química interna. |
| Diseño de doble unión (variación) | Aísla el KCl de la muestra utilizando un electrolito intermedio para evitar la contaminación por cloruro en muestras sensibles. |
¿Listo para lograr resultados electroquímicos precisos y confiables?
El electrodo de referencia adecuado es fundamental para el éxito de su laboratorio. KINTEK se especializa en equipos de laboratorio de alta calidad, incluida una gama de electrodos de Ag/AgCl diseñados para la precisión y durabilidad en soluciones neutras. Ya sea que necesite un modelo estándar de unión simple para uso general o un electrodo de doble unión para aplicaciones sensibles al cloruro, tenemos la solución para satisfacer las necesidades específicas de su laboratorio.
Deje que nuestros expertos le ayuden a seleccionar el electrodo perfecto para sus experimentos. ¡Contacte a KINTEK hoy mismo para discutir sus requisitos y mejorar sus capacidades de medición!
Guía Visual
Productos relacionados
- Electrodo de Referencia Calomel Plata Cloruro Mercurio Sulfato para Uso en Laboratorio
- Electrodo de Referencia de Sulfato de Cobre para Uso en Laboratorio
- Electrodo de Disco de Oro
- Electrodo de Hoja de Oro Electrodos de Oro para Electroquímica
- Electrodo Electrolítico de Grafito en Disco y Varilla de Grafito
La gente también pregunta
- ¿Qué es el electrodo de referencia en potenciometría? La clave para mediciones estables y precisas
- ¿Qué electrodo se utiliza como referencia? Una guía para mediciones electroquímicas precisas
- ¿Cuál es la función de un electrodo de referencia? Domina la precisión en la reconstrucción de reactores de tres electrodos
- ¿Por qué es fundamental la selección de un electrodo de referencia de alta calidad en la síntesis electroquímica? | KINTEK
- ¿Qué electrodo se utiliza como electrodo de referencia para medir potenciales de semicelda? Comprendiendo el Estándar Universal










