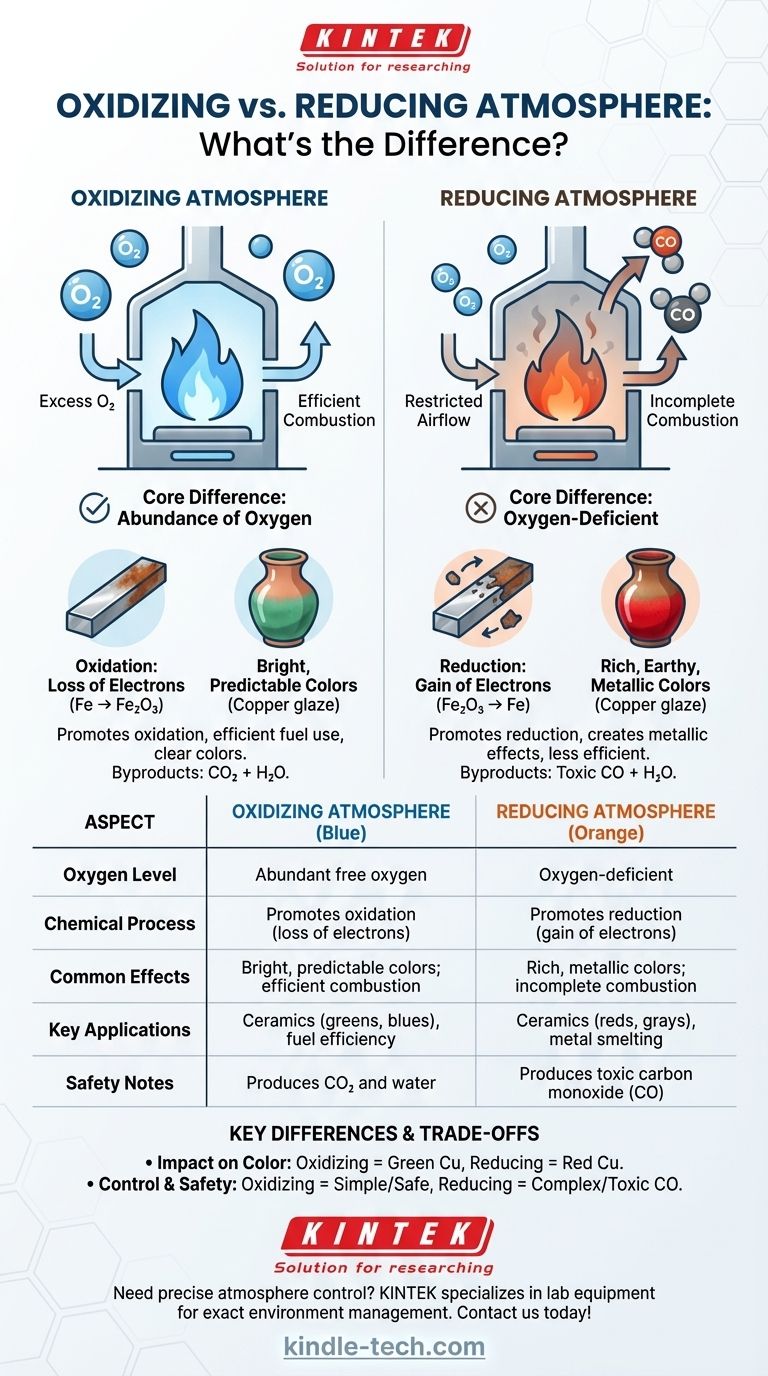
En esencia, la diferencia entre una atmósfera oxidante y una reductora es la disponibilidad de oxígeno. Una atmósfera oxidante tiene una abundancia de oxígeno libre, lo que promueve reacciones químicas como la combustión y la corrosión. Una atmósfera reductora es deficiente en oxígeno y activamente despoja a los materiales de átomos de oxígeno, invirtiendo el proceso de oxidación.
La elección entre una atmósfera oxidante o reductora es un mecanismo de control fundamental en la ciencia de los materiales y la química. No se trata solo del entorno; es una herramienta utilizada para cambiar deliberadamente el estado químico y las propiedades físicas de un material.
¿Qué es una atmósfera oxidante?
Una atmósfera oxidante es el estado "predeterminado" en el que vivimos, definido por la presencia de exceso de oxígeno. En aplicaciones de alta temperatura como hornos o estufas, se mantiene asegurando un suministro constante y amplio de aire fresco.
El papel del exceso de oxígeno
La característica clave es que hay más oxígeno disponible del necesario para quemar completamente cualquier combustible presente. Este excedente de oxígeno es químicamente activo y está listo para reaccionar con otros materiales.
El proceso químico: Oxidación
La oxidación es una reacción química en la que una sustancia pierde electrones. Aunque otros elementos pueden causar esto, en este contexto, casi siempre implica que una sustancia se une con el oxígeno. Este es el mismo proceso fundamental que causa la oxidación del hierro o que un fuego arda limpiamente.
Efectos y aplicaciones comunes
En un fuego oxidante, el combustible se quema de manera eficiente y completa, produciendo el máximo calor con poca o ninguna hollín. En cerámica, produce colores claros, brillantes y a menudo predecibles de esmaltes y cuerpos de arcilla (por ejemplo, el hierro produce tonos tostados y rojos, el cobre produce verdes y azules).
¿Qué es una atmósfera reductora?
Una atmósfera reductora es un ambiente con escasez de oxígeno. Se crea deliberadamente en un horno o estufa restringiendo la entrada de aire o introduciendo más combustible del que el aire disponible puede quemar.
El papel del combustible sin quemar
Con oxígeno insuficiente para una combustión completa, el combustible sin quemar libera compuestos como el monóxido de carbono (CO) y el hidrógeno. Estos compuestos son químicamente inestables y buscan agresivamente átomos de oxígeno para unirse a ellos.
El proceso químico: Reducción
La reducción es lo opuesto a la oxidación; es una reacción química en la que una sustancia gana electrones. En este entorno, el monóxido de carbono "roba" activamente átomos de oxígeno de los óxidos metálicos dentro de la arcilla o los esmaltes, reduciéndolos a un estado más metálico.
Efectos y aplicaciones comunes
Un fuego reductor es a menudo más frío y más humeante, una señal de combustión incompleta. Es esencial para procesos como la fundición de metal a partir de mineral. En cerámica, crea colores terrosos y metálicos ricos, complejos y a menudo impredecibles (por ejemplo, el hierro produce azules y grises profundos, el cobre produce rojos vibrantes).
Comprendiendo las diferencias clave y las compensaciones
La decisión de usar una atmósfera u otra está impulsada enteramente por el resultado deseado, pero conlleva importantes compensaciones.
Impacto en el color y las propiedades del material
Esta es la diferencia más visible. Un esmalte que contiene óxido de cobre se volverá verde en una atmósfera oxidante. El mismo esmalte, cuando se cuece en una atmósfera reductora, verá su oxígeno eliminado, reduciendo el cobre a su forma metálica y creando un rojo brillante.
Control y eficiencia
Lograr una atmósfera oxidante es simple: proporcionar mucho aire. Crear una atmósfera reductora requiere una gestión activa, como cerrar un amortiguador para privar al fuego de oxígeno. Esto hace que el proceso sea menos eficiente en cuanto a combustible, ya que no se extrae toda la energía potencial del combustible.
Seguridad y subproductos
Los fuegos oxidantes producen principalmente dióxido de carbono (CO₂) y agua. Los fuegos reductores, debido a la combustión incompleta, producen cantidades significativas de monóxido de carbono (CO), un gas incoloro, inodoro y altamente tóxico. Una ventilación adecuada es absolutamente crítica al crear una atmósfera reductora.
Cómo elegir la atmósfera adecuada
Su elección depende enteramente de su material y su objetivo. La atmósfera no es una condición de fondo; es un ingrediente activo en el proceso químico.
- Si su enfoque principal son los colores brillantes y estables y la eficiencia del combustible: Utilice una atmósfera oxidante asegurando un flujo de aire constante y amplio a su horno o estufa.
- Si su enfoque principal son los efectos ricos, terrosos o metálicos en cerámica: Utilice una atmósfera reductora restringiendo cuidadosamente el flujo de aire a temperaturas específicas para forzar la reducción química de los óxidos metálicos.
- Si su enfoque principal es la fundición de mineral o la prevención de la formación de incrustaciones superficiales en el acero: Utilice una atmósfera fuertemente reductora para despojar el oxígeno del mineral o evitar que se forme en la superficie del metal.
Dominar la interacción entre el oxígeno y el calor le brinda un control preciso sobre la forma y función final de su material.

Tabla resumen:
| Aspecto | Atmósfera Oxidante | Atmósfera Reductora |
|---|---|---|
| Nivel de Oxígeno | Oxígeno libre abundante | Deficiente en oxígeno |
| Proceso Químico | Promueve la oxidación (pérdida de electrones) | Promueve la reducción (ganancia de electrones) |
| Efectos Comunes | Colores brillantes y predecibles; combustión eficiente | Colores ricos y metálicos; combustión incompleta |
| Aplicaciones Clave | Cerámica (verdes, azules), eficiencia de combustible | Cerámica (rojos, grises), fundición de metales |
| Notas de Seguridad | Produce CO₂ y agua | Produce monóxido de carbono (CO) tóxico |
¿Necesita un control preciso de la atmósfera para los procesos de su laboratorio? KINTEK se especializa en equipos y consumibles de laboratorio, ofreciendo hornos y estufas que proporcionan un control exacto sobre ambientes oxidantes o reductores. Ya sea que esté desarrollando nuevos materiales, probando cerámicas o realizando experimentos a alta temperatura, nuestras soluciones garantizan resultados precisos y repetibles. Contáctenos hoy para discutir cómo podemos mejorar las capacidades de su laboratorio.
Guía Visual