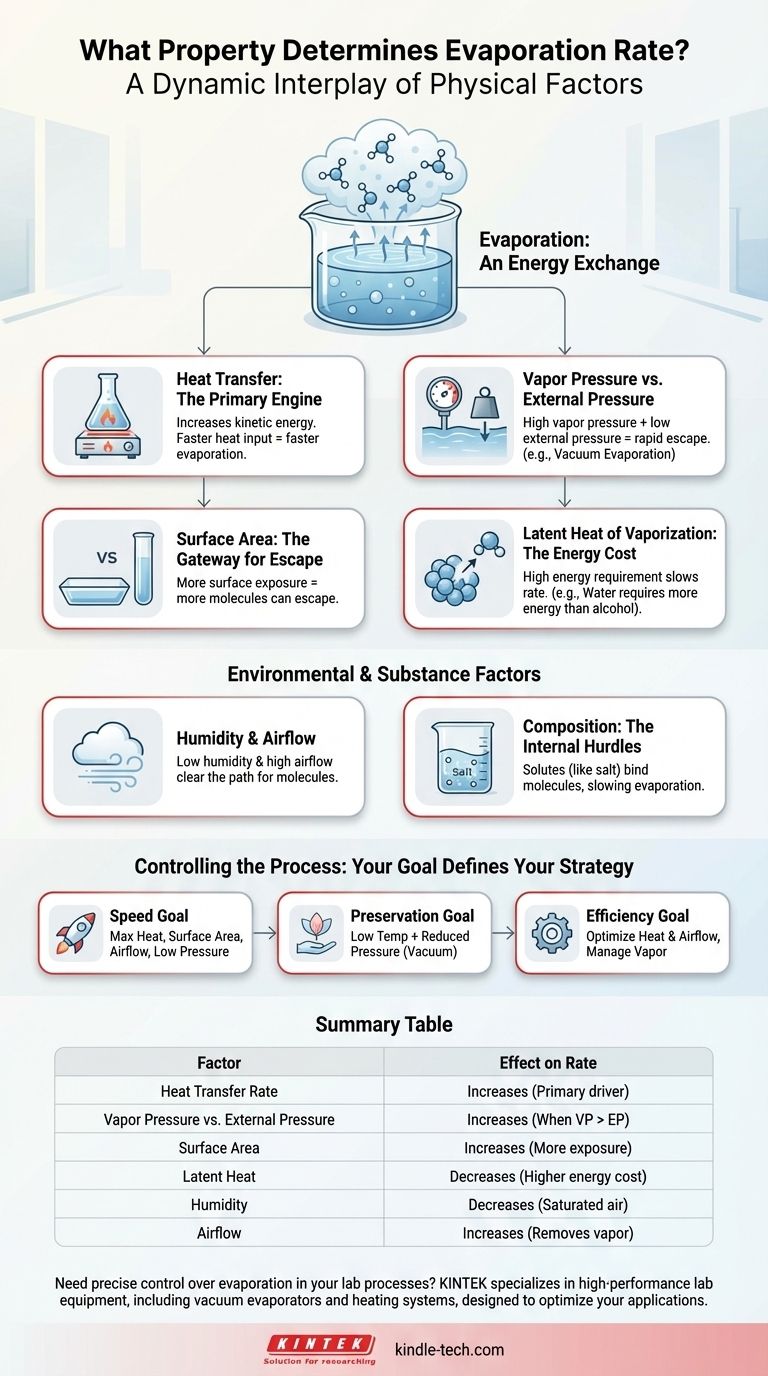
La evaporación no se rige por una sola propiedad, sino por una interacción dinámica de varios factores físicos clave. La tasa está fundamentalmente determinada por la velocidad de transferencia de calor al líquido, la presión sobre su superficie y la energía intrínseca requerida para que el líquido se convierta en gas.
El principio central es un intercambio de energía: la evaporación se acelera cuando se añade energía a un líquido más rápidamente de lo que el entorno circundante puede resistir el escape de sus moléculas. Comprender cómo manipular el calor, la presión y el área de superficie le da control directo sobre este proceso.

Los impulsores principales de la evaporación
Para comprender verdaderamente la tasa de evaporación, debemos observar las fuerzas físicas en juego. Estos factores actúan en conjunto para fomentar o dificultar el escape de moléculas de la superficie de un líquido.
Transferencia de calor: El motor principal
El impulsor más significativo es la velocidad a la que se suministra energía térmica al líquido. El calor aumenta la energía cinética de las moléculas del líquido.
Cuando una molécula gana suficiente energía cinética para superar las fuerzas intermoleculares que la unen a sus vecinas, escapa de la superficie como gas. Por lo tanto, una mayor tasa de transferencia de calor se traduce directamente en una tasa de evaporación más rápida.
Presión de vapor y presión externa: La batalla en la superficie
Cada líquido ejerce una presión de vapor, que es la fuerza de sus moléculas que empujan para escapar a la fase gaseosa. Esto se contrarresta con la presión externa (generalmente la presión atmosférica) que empuja hacia abajo sobre la superficie del líquido.
La evaporación ocurre rápidamente cuando la presión de vapor es alta en relación con la presión externa. Por eso el agua se evapora más rápido en altitudes elevadas donde la presión atmosférica es menor.
Calor latente de vaporización: El costo energético
El calor latente de vaporización es la cantidad específica de energía requerida para convertir una unidad de una sustancia de líquido a gas sin cambiar su temperatura.
Las sustancias con un alto calor latente de vaporización, como el agua, requieren más energía para evaporar cada kilogramo. Esto actúa como un freno en la tasa de evaporación en comparación con líquidos como el alcohol, que tienen un costo energético menor.
Área de superficie: La puerta de escape
La evaporación es un fenómeno de superficie. Solo las moléculas en o cerca de la superficie pueden escapar.
Al aumentar el área de superficie —por ejemplo, extendiendo un charco de agua— se exponen más moléculas al aire, creando más oportunidades para que escapen. Esto aumenta drásticamente la tasa de evaporación general.
Factores ambientales y específicos de la sustancia
Más allá de la física básica, el entorno inmediato y la composición del líquido añaden otra capa de control.
Humedad y flujo de aire: Despejando el camino
La cantidad de vapor ya presente en el aire circundante, conocida como humedad, afecta la tasa neta de evaporación. Si el aire ya está saturado, hay menos "espacio" para nuevas moléculas de agua, lo que ralentiza el proceso.
El flujo de aire (viento) arrastra la capa de aire húmedo directamente sobre la superficie del líquido, reemplazándola con aire más seco. Esto mantiene un gradiente de concentración pronunciado y fomenta que más moléculas escapen.
Composición de la sustancia: Los obstáculos internos
La presencia de solutos, como sal o azúcar en el agua, puede ralentizar la evaporación. Estas partículas disueltas forman enlaces con las moléculas de agua, lo que requiere más energía para romperlas.
Por eso el agua de mar se evapora más lentamente que el agua dulce en condiciones idénticas. Las propiedades de la sustancia en sí, y cualquier cambio que experimente, son un factor crítico.
Comprendiendo las compensaciones
La manipulación de estos factores a menudo implica equilibrar prioridades contrapuestas, especialmente en aplicaciones industriales o culinarias.
La relación entre presión y temperatura
Reducir la presión disminuye el punto de ebullición de un líquido. Esta poderosa relación permite una evaporación rápida a temperaturas mucho más bajas de lo que se requeriría de otro modo.
Esta técnica, conocida como evaporación al vacío, es esencial para concentrar sustancias sensibles al calor, como la leche o los zumos de frutas, sin quemarlas ni degradarlas.
El límite de la entrada de calor
Si bien añadir calor es la forma más rápida de aumentar la evaporación, a menudo existe una temperatura máxima permitida.
Exceder este límite puede causar reacciones químicas no deseadas, quemaduras o descomposición del producto. El objetivo suele ser encontrar la tasa de transferencia de calor más alta posible que no comprometa la integridad de la sustancia.
Cómo controlar la evaporación para su objetivo
Su estrategia para gestionar la evaporación depende completamente del resultado deseado.
- Si su enfoque principal es la velocidad: Maximice la tasa de entrada de calor, aumente el área de superficie, asegure un flujo de aire constante y, si es posible, reduzca la presión ambiental.
- Si su enfoque principal es preservar la sustancia: Utilice una temperatura más baja combinada con presión reducida para lograr la evaporación sin daños por calor.
- Si su enfoque principal es la eficiencia energética: Concéntrese en optimizar la transferencia de calor y gestionar el flujo de aire para eliminar el vapor saturado, evitando el desperdicio de energía.
En última instancia, controlar la evaporación es un proceso de gestión del flujo de energía dentro y fuera de un sistema.
Tabla resumen:
| Factor | Efecto en la tasa de evaporación | Principio clave |
|---|---|---|
| Tasa de transferencia de calor | Aumenta | Impulsor principal; añade energía cinética a las moléculas. |
| Presión de vapor vs. Presión externa | Aumenta cuando la presión de vapor > presión externa | Las moléculas escapan más fácilmente cuando la presión externa es menor. |
| Área de superficie | Aumenta | Más moléculas expuestas en la superficie, permitiendo el escape. |
| Calor latente de vaporización | Disminuye para sustancias con alto calor latente | Mayor costo energético por molécula ralentiza la tasa. |
| Humedad | Disminuye | El aire saturado reduce el gradiente de concentración para el escape. |
| Flujo de aire | Aumenta | Elimina el vapor saturado, manteniendo un gradiente de concentración pronunciado. |
¿Necesita un control preciso sobre la evaporación en sus procesos de laboratorio? KINTEK se especializa en equipos de laboratorio de alto rendimiento, incluidos evaporadores al vacío y sistemas de calefacción diseñados para optimizar la transferencia de calor, la presión y el área de superficie para sus aplicaciones específicas, ya sea que esté concentrando muestras sensibles al calor o maximizando el rendimiento. Deje que nuestros expertos le ayuden a seleccionar la solución adecuada para mejorar la eficiencia y preservar la integridad de la muestra. ¡Contacte a KINTEK hoy mismo para discutir sus necesidades de evaporación en el laboratorio!
Guía Visual