La Ilusión de la Perilla
Existe la tentación en el trabajo de laboratorio de ver el control como un simple acto mecánico. Giras un dial, la aguja se mueve y la máquina obedece.
En electroquímica, esta visión es peligrosa.
Una celda electrolítica no es simplemente una máquina; es un entorno caótico donde intentas forzar a la naturaleza a retroceder. Estás usando energía para impulsar reacciones no espontáneas. Para hacerlo con éxito, no puedes simplemente "encenderla".
Debes actuar como un arquitecto del entorno atómico.
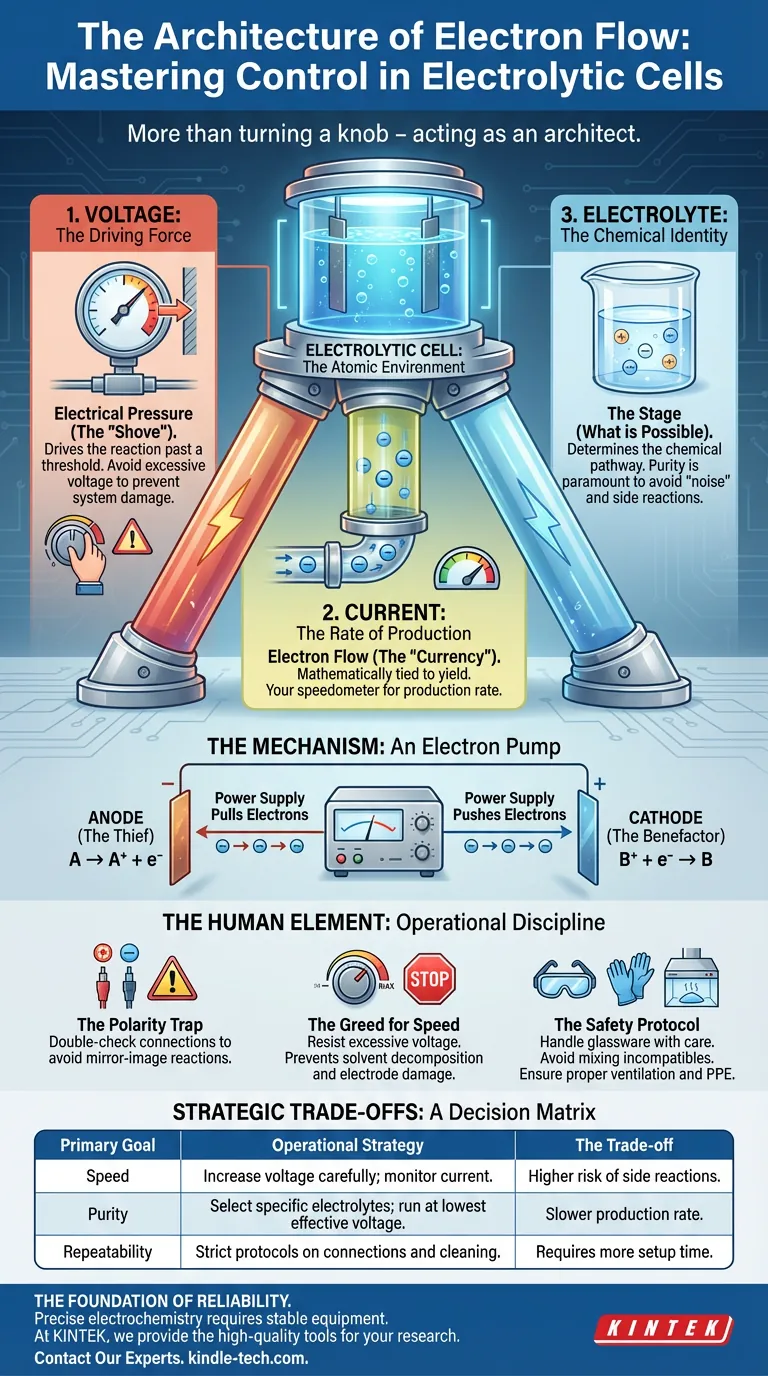
El control en este contexto es un trípode. Descansa sobre tres pilares innegociables: Voltaje, Corriente y Composición. Si ignoras uno, la estructura colapsa.
Las Tres Palancas de Influencia
Para dominar la salida de tu celda, debes comprender el papel distinto de cada variable. Están interconectadas, pero no son lo mismo.
1. Voltaje: La Fuerza Motriz
Piensa en el voltaje como presión eléctrica. Es el empujón necesario para que la reacción comience.
Sin suficiente voltaje, no sucede nada. La barrera para la reacción sigue siendo demasiado alta. Sin embargo, más no siempre es mejor. Aumentar el voltaje aumenta la velocidad, pero solo hasta un umbral. Más allá de ese punto, ya no estás impulsando la reacción, estás dañando el sistema.
2. Corriente: La Velocidad de Producción
La corriente es el flujo de electrones. En la economía de la celda electrolítica, los electrones son la moneda.
La cantidad de producto que creas está matemáticamente ligada a la corriente. Si deseas un mayor rendimiento, necesitas más carga pasando por el sistema con el tiempo. La corriente es tu velocímetro.
3. Electrolito: La Identidad Química
El electrolito es el escenario donde ocurre la obra. Determina qué reacción es químicamente posible.
Si el voltaje y la corriente son el motor, el electrolito es el destino. La pureza aquí es primordial. Un electrolito contaminado introduce "ruido" en el sistema, lo que lleva a reacciones secundarias que arruinan el producto final.
El Mecanismo: Una Bomba de Electrones
Para controlar la celda, debes visualizar lo que está sucediendo en los electrodos. La fuente de alimentación externa actúa como una bomba, creando un desequilibrio que la naturaleza desesperadamente quiere corregir.
- En el Ánodo (El Ladrón): La fuente de alimentación extrae electrones. Esto obliga a las especies del electrolito a perder electrones (oxidación).
- En el Cátodo (El Benefactor): La fuente de alimentación empuja electrones hacia adentro. Esto obliga a las especies a ganar electrones (reducción).
Tu trabajo es regular esta bomba para que el intercambio ocurra exactamente como se planeó, sin abrumar la capacidad química de la solución.
El Elemento Humano: Disciplina Operacional
La variable más grande en cualquier experimento es el operador. El conocimiento teórico falla cuando se encuentra con negligencia práctica.
En cirugía, una lista de verificación salva vidas. En el laboratorio, un protocolo salva experimentos.
La Trampa de la Polaridad
Invertir el ánodo y el cátodo es un error simple con consecuencias profundas. Crea una reacción imagen especular, produciendo las sustancias incorrectas en los polos incorrectos. Verifique sus conexiones dos veces.
La Codicia por la Velocidad
Existe un impulso psicológico para aumentar el voltaje y terminar más rápido. Resístelo.
Un voltaje excesivo a menudo conduce a la descomposición del disolvente (generalmente agua) o a la degradación de la superficie del electrodo. Cambias la pureza por la velocidad, y generalmente, pierdes ambas.
El Protocolo de Seguridad
La química es implacable con la complacencia.
- Vidrio de laboratorio: Manipule la celda con cuidado. Los rasguños de los cepillos metálicos debilitan la integridad estructural.
- Mezclas: Nunca mezcle ácidos y bases durante la limpieza. La reacción exotérmica resultante puede hacer estallar el recipiente.
- Protección: Los electrolitos corrosivos y los gases tóxicos exigen una ventilación adecuada (campanas de extracción) y EPP.
Compensaciones Estratégicas
La perfección es imposible. La optimización es el objetivo. Su estrategia de control debe cambiar según su objetivo específico.
Utilice esta matriz de decisión para guiar su configuración:
| Objetivo Principal | Estrategia Operacional | La Compensación |
|---|---|---|
| Velocidad | Aumente el voltaje cuidadosamente; monitoree la corriente. | Mayor riesgo de reacciones secundarias. |
| Pureza | Seleccione electrolitos específicos; opere al voltaje efectivo más bajo. | Tasa de producción más lenta. |
| Repetibilidad | Protocolos estrictos sobre conexiones y limpieza. | Requiere más tiempo de configuración. |
La Base de la Fiabilidad
No puedes controlar una reacción si no puedes confiar en tus herramientas.
La electroquímica precisa requiere equipos que proporcionen voltaje estable, corriente constante y materiales duraderos que resistan entornos corrosivos sin contaminar sus resultados.
En KINTEK, entendemos el romance del ingeniero con la precisión. Nos especializamos en proporcionar equipos de laboratorio y consumibles de alta calidad que sirven como el socio silencioso en su investigación. Cuando el hardware es confiable, usted es libre de concentrarse en la ciencia.
Guía Visual
Productos relacionados
- Celda electrolítica de PTFE Celda electroquímica sellada y no sellada resistente a la corrosión
- Celda electroquímica electrolítica super sellada
- Célula electrolítica electroquímica de cinco puertos
- Celda Electrolítica Tipo H Triple Celda Electroquímica
- Celda de gas de difusión electrolítica electroquímica Celda de reacción de flujo de líquido
Artículos relacionados
- El Arte de lo No Espontáneo: Precisión en Circuitos Electrolíticos
- La Arquitectura de la Certeza: Dominando el Control en Celdas Electrolíticas Multifuncionales
- El Ancla de la Verdad: Por Qué la Estabilidad Física Define el Éxito Electroquímico
- Diseño y normas de las células electrolíticas
- La Geometría Silenciosa del Voltaje: Respetando los Límites de la Electrólisis




















