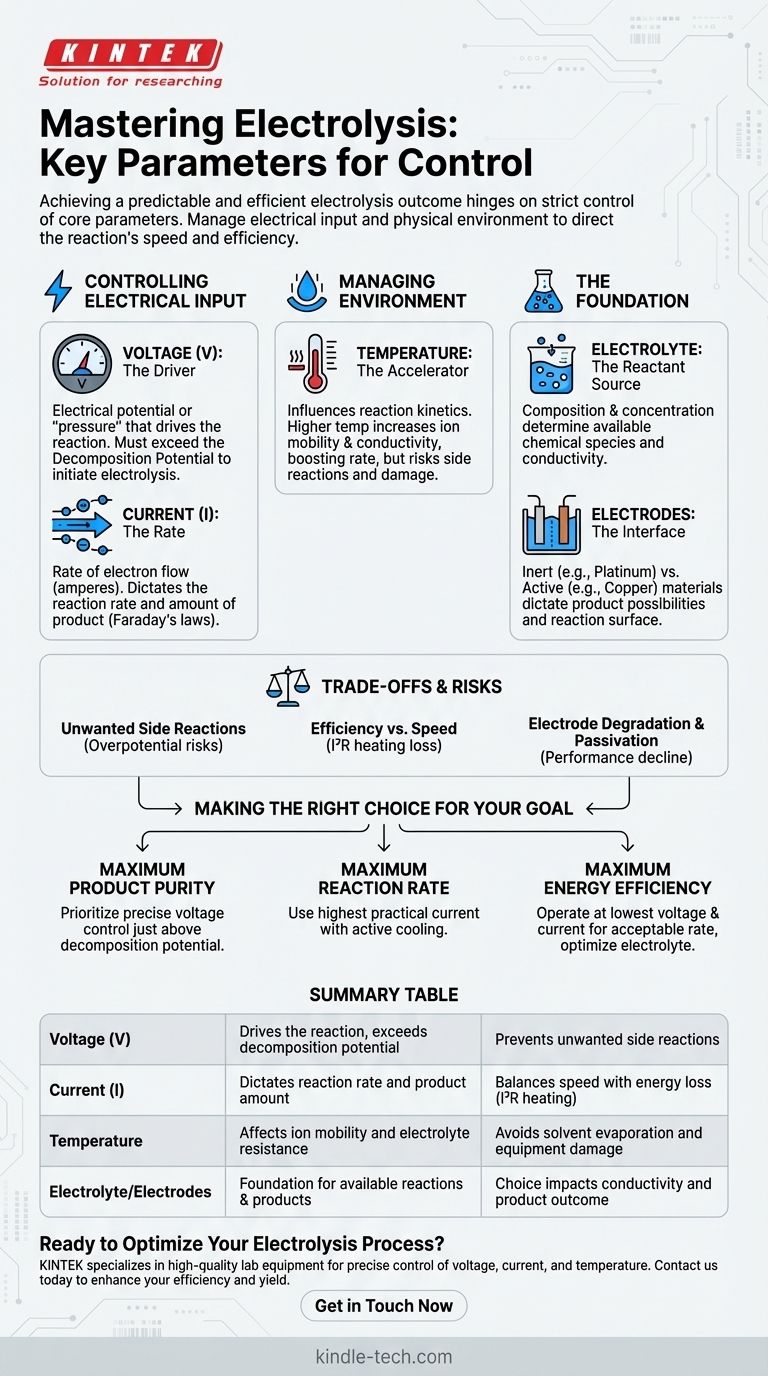
En cualquier configuración de electrólisis, lograr un resultado predecible y eficiente depende del control estricto de varios parámetros fundamentales. Para asegurar que la reacción proceda según lo previsto, debe gestionar con precisión la entrada eléctrica —específicamente el voltaje y la corriente—, así como el entorno físico, principalmente la temperatura del electrolito. Estas tres variables son las palancas principales para controlar la velocidad y la eficiencia de la reacción.
El desafío principal de la electrólisis no es simplemente iniciar una reacción, sino dirigirla. Si bien controlar el voltaje, la corriente y la temperatura es la tarea inmediata, el verdadero dominio proviene de comprender cómo estos parámetros, junto con la elección del electrolito y los electrodos, dictan los productos finales y la eficiencia general.

Los Pilares del Control Electrolítico
Una electrólisis exitosa es un acto de equilibrio. Cada parámetro influye en los demás y tiene un impacto directo en el resultado final. Comprender sus roles individuales es el primer paso hacia el dominio del proceso.
Control de la Entrada Eléctrica: Voltaje y Corriente
El suministro eléctrico es el motor de su reacción. El voltaje (V) es el potencial eléctrico o la "presión" que impulsa la reacción. Debe ser suficiente para superar el potencial de descomposición del electrolito, que es el voltaje mínimo requerido para que comience la electrólisis.
La corriente (I), medida en amperios, es la tasa de flujo de electrones. Según las leyes de Faraday de la electrólisis, la cantidad de sustancia química producida es directamente proporcional a la cantidad de corriente que pasa a través del sistema a lo largo del tiempo. En resumen, la corriente dicta la velocidad de reacción.
Gestión del Entorno de Reacción: Temperatura
La temperatura influye en la cinética de la reacción. Aumentar la temperatura generalmente reduce la viscosidad de la solución y aumenta la movilidad de los iones, lo que a su vez disminuye la resistencia eléctrica del electrolito.
Esto permite una mayor velocidad de reacción a un voltaje dado. Sin embargo, el calor excesivo puede causar reacciones secundarias no deseadas, provocar la evaporación del solvente o incluso dañar el equipo.
La Base: Electrolito y Electrodos
Aunque no son variables de proceso dinámicas de la misma manera que la temperatura o la corriente, la elección inicial del electrolito y los electrodos es el acto de control más fundamental que usted tiene.
La composición y concentración del electrolito determinan qué especies químicas están disponibles para reaccionar. Las concentraciones más altas suelen aumentar la conductividad, pero también pueden alterar qué reacciones se favorecen en los electrodos.
El material del electrodo determina si el electrodo simplemente proporciona una superficie para la reacción (electrodos inertes como el platino o el grafito) o participa directamente en ella (electrodos activos como el cobre o el zinc), cambiando fundamentalmente los posibles productos.
Comprendiendo las Ventajas y Desventajas y los Riesgos
Controlar la electrólisis no se trata solo de ajustar diales; se trata de navegar por compromisos y evitar errores comunes que pueden arruinar sus resultados.
El Riesgo de Reacciones Secundarias No Deseadas
Aplicar un voltaje significativamente más alto que el potencial de descomposición es un error común. Este "sobrepotencial" puede proporcionar suficiente energía para desencadenar reacciones no deseadas, como la electrólisis del agua misma, lo que reduce la eficiencia de corriente para su producto objetivo.
Eficiencia vs. Velocidad
Existe una constante compensación entre la velocidad y la eficiencia energética. Impulsar una alta velocidad de reacción aumentando la corriente también aumenta las pérdidas de calor resistivo (calentamiento I²R). Esto desperdicia energía y requiere un control de temperatura más robusto, lo que añade complejidad y costo.
Degradación y Pasivación de Electrodos
Incluso los electrodos considerados "inertes" pueden degradarse bajo condiciones extremas de voltaje o densidad de corriente. Más críticamente, la superficie de un electrodo puede recubrirse con una capa aislante de producto —un fenómeno llamado pasivación— que puede ralentizar o detener por completo el proceso de electrólisis.
Tomando la Decisión Correcta para Su Objetivo
La estrategia de control óptima depende completamente de lo que quiera lograr. Use su objetivo principal para guiar cómo gestiona los parámetros clave.
- Si su enfoque principal es la máxima pureza del producto: Priorice el control preciso del voltaje para mantenerse justo por encima del potencial de descomposición para su reacción objetivo, evitando reacciones secundarias.
- Si su enfoque principal es la máxima velocidad de reacción: Utilice la corriente práctica más alta que su sistema pueda manejar mientras implementa un sistema de enfriamiento activo para gestionar el aumento de temperatura resultante.
- Si su enfoque principal es la máxima eficiencia energética: Opere con el voltaje y la corriente más bajos posibles que aún produzcan una tasa aceptable, y optimice la concentración del electrolito para minimizar la resistencia.
Dominar estos parámetros transforma la electrólisis de una simple demostración en una herramienta de fabricación química precisa y predecible.
Tabla Resumen:
| Parámetro | Función Principal | Consideración Clave |
|---|---|---|
| Voltaje (V) | Impulsa la reacción, debe exceder el potencial de descomposición | Evita reacciones secundarias no deseadas |
| Corriente (I) | Dicta la velocidad de reacción y la cantidad de producto | Equilibra la velocidad con la pérdida de energía (calentamiento I²R) |
| Temperatura | Afecta la movilidad de los iones y la resistencia del electrolito | Evita la evaporación del solvente y el daño al equipo |
| Electrolito/Electrodos | Base para las reacciones y productos disponibles | La elección impacta la conductividad y el resultado del producto |
¿Listo para Optimizar Su Proceso de Electrólisis?
Lograr un control preciso sobre el voltaje, la corriente y la temperatura es fundamental para obtener resultados eficientes y predecibles. Ya sea que su objetivo sea la máxima pureza del producto, una alta velocidad de reacción o una eficiencia energética óptima, el equipo de laboratorio adecuado es esencial.
KINTEK se especializa en equipos y consumibles de laboratorio de alta calidad, satisfaciendo todas sus necesidades de laboratorio. Desde fuentes de alimentación precisas hasta sistemas de control de temperatura, le proporcionamos las herramientas confiables que necesita para dominar sus parámetros de electrólisis.
Contáctenos hoy para discutir cómo nuestras soluciones pueden mejorar la eficiencia y el rendimiento de su proceso. Construyamos juntos un laboratorio más controlado y productivo.
Guía Visual
Productos relacionados
- Celdas personalizables de electrólisis PEM para diversas aplicaciones de investigación
- Célula electroquímica de electrólisis espectral de capa fina
- Celda de gas de difusión electrolítica electroquímica Celda de reacción de flujo de líquido
- Celda electroquímica electrolítica de cuarzo para experimentos electroquímicos
- Celda electrolítica de PTFE Celda electroquímica sellada y no sellada resistente a la corrosión
La gente también pregunta
- ¿Cuáles son las precauciones para calentar o esterilizar una celda de electrólisis? Evite dañar los componentes sensibles
- ¿Cuáles son los riesgos de un control de voltaje inadecuado en una celda de electrólisis? Evite daños costosos e ineficiencia
- ¿Cuáles son las configuraciones de apertura para las versiones no selladas y selladas de la celda de electrólisis? Optimice su configuración electroquímica
- ¿Cuál es el procedimiento de limpieza inmediato posterior al uso de una celda de electrólisis? Evite la acumulación de residuos para obtener resultados precisos
- ¿Cómo se conoce también a una celda de electrólisis? Entendiendo las celdas electrolíticas vs. galvánicas



















