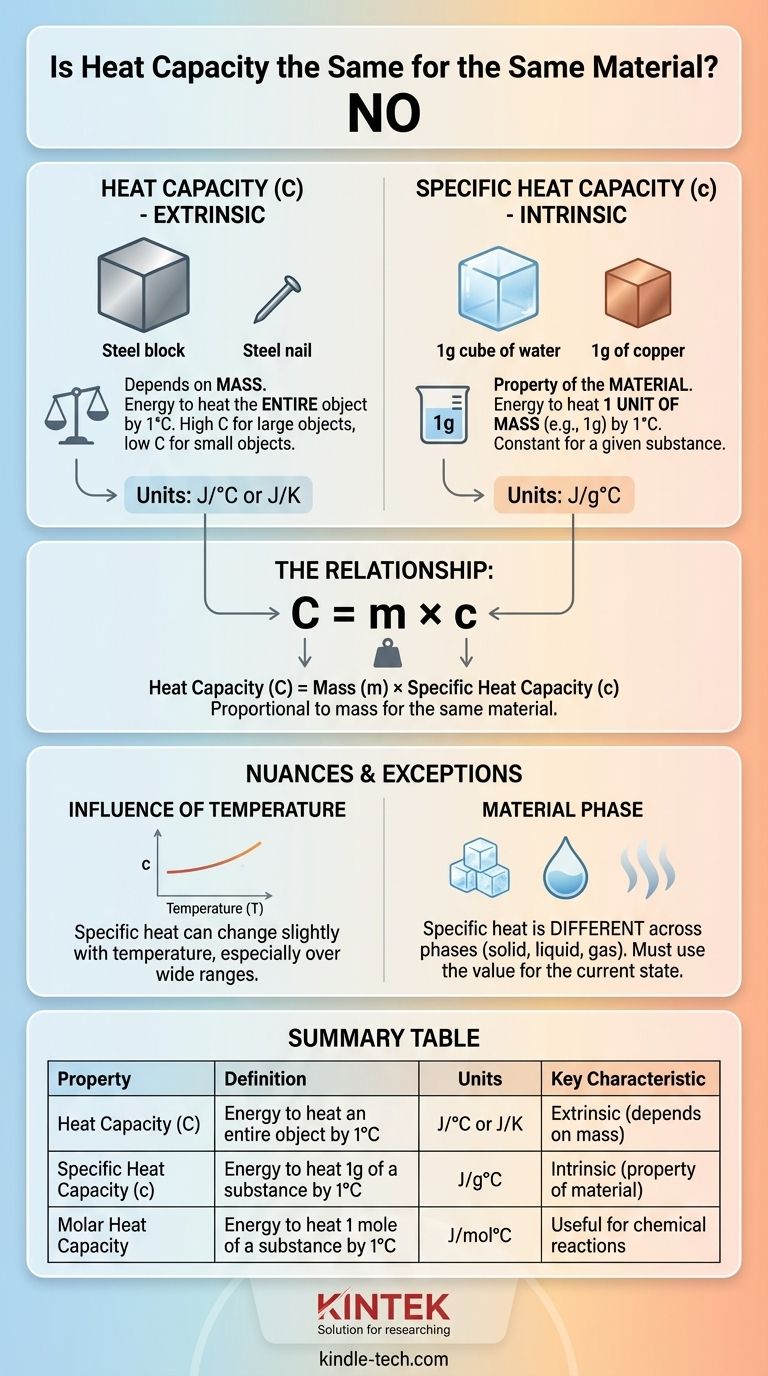
En resumen, no. La capacidad calorífica de un objeto no es la misma para el mismo material si la cantidad de material es diferente. La capacidad calorífica depende directamente de la masa de un objeto, por lo que un bloque grande de acero tendrá una capacidad calorífica mucho mayor que un pequeño clavo de acero. La propiedad en la que estás pensando, que es constante para un material, se llama calor específico.
La distinción fundamental es esta: la capacidad calorífica es una propiedad extrínseca de un objeto específico (cuánta energía se necesita para calentar todo el objeto), mientras que el calor específico es una propiedad intrínseca de una sustancia (cuánta energía se necesita para calentar una cantidad determinada, como un gramo). Confundir una con la otra es una fuente común de confusión.

Definiendo los conceptos clave: Capacidad calorífica vs. Calor específico
Para resolver problemas que involucran energía térmica, primero debes ser preciso con tus términos. La diferencia entre "capacidad calorífica" y "calor específico" es fundamental.
¿Qué es la capacidad calorífica (C)?
La capacidad calorífica es la cantidad de energía térmica requerida para elevar la temperatura de un objeto entero en un grado (Celsius o Kelvin).
Piensa en ello como la inercia térmica de un objeto en particular. Una piscina grande requiere una cantidad masiva de energía para calentarse un grado, por lo que tiene una alta capacidad calorífica. Una taza pequeña de agua requiere mucha menos energía, por lo que tiene una baja capacidad calorífica.
Debido a que depende del tamaño del objeto, la capacidad calorífica es una propiedad extrínseca. Su unidad es típicamente Joules por grado Celsius (J/°C) o Joules por Kelvin (J/K).
¿Qué es el calor específico (c)?
El calor específico es la cantidad de energía térmica requerida para elevar la temperatura de una unidad de masa (como un gramo o un kilogramo) de una sustancia en un grado.
Este es el valor que se encuentra en las tablas de referencia para los materiales. Permite una comparación justa entre sustancias. Por ejemplo, el agua tiene un calor específico muy alto (4.184 J/g°C), mientras que el cobre tiene uno bajo (0.385 J/g°C).
Esto significa que se necesita mucha más energía para calentar un gramo de agua que para calentar un gramo de cobre. Debido a que está estandarizado por unidad de masa, el calor específico es una propiedad intrínseca de una sustancia.
La relación matemática
La conexión entre estas dos propiedades es simple y directa. La capacidad calorífica de un objeto es su masa multiplicada por el calor específico del material.
Capacidad calorífica (C) = masa (m) × calor específico (c)
Esta fórmula muestra claramente que si tienes dos objetos hechos del mismo material (mismo c), el que tenga mayor masa (m) tendrá una capacidad calorífica (C) proporcionalmente mayor.
Comprendiendo los matices y las excepciones
Si bien el calor específico se considera una constante para un material dado, esta suposición tiene límites importantes en aplicaciones de ingeniería y científicas del mundo real.
La influencia de la temperatura
Para la mayoría de los cálculos cotidianos, el calor específico se trata como constante. Sin embargo, en realidad, el calor específico de un material puede cambiar ligeramente con la temperatura.
En campos de alta precisión como la aeroespacial o la ciencia de materiales, los ingenieros deben tener en cuenta cómo cambia el calor específico de un material a medida que se calienta o enfría en un amplio rango.
El papel crítico de la fase del material
El calor específico de una sustancia no es el mismo en sus diferentes fases (sólido, líquido, gas).
El ejemplo más común es el agua. El calor específico del hielo sólido es diferente al del agua líquida, que también es diferente al del vapor gaseoso. Al realizar cálculos, debes usar el valor correspondiente al estado actual del material.
Capacidad calorífica molar: una perspectiva diferente
En química, a menudo es más útil medir la cantidad de una sustancia en moles en lugar de en masa.
La capacidad calorífica molar es la energía requerida para elevar un mol de una sustancia en un grado. Esto es particularmente útil al analizar reacciones químicas, donde el número de moléculas es el factor clave.
Cómo aplicar este conocimiento correctamente
Elegir el término correcto depende completamente de lo que intentes describir o calcular.
- Si tu enfoque principal es un objeto específico: Usa la capacidad calorífica (C) para comprender la energía total necesaria para calentar ese objeto completo, como un bloque de motor, un disipador de calor o una olla de cocina.
- Si tu enfoque principal es una sustancia o material: Usa el calor específico (c) para comparar las propiedades térmicas inherentes de diferentes materiales, como elegir entre aluminio y cobre para una aplicación particular.
- Si tu enfoque principal es una reacción química: Considera usar la capacidad calorífica molar, ya que relaciona los cambios de energía directamente con el número de moléculas involucradas en el proceso.
Distinguir entre la propiedad de un objeto y la propiedad de una sustancia es la clave para dominar los cálculos térmicos.
Tabla resumen:
| Propiedad | Definición | Unidades | Característica clave |
|---|---|---|---|
| Capacidad calorífica (C) | Energía para calentar un objeto entero en 1°C | J/°C o J/K | Extrínseca (depende de la masa) |
| Calor específico (c) | Energía para calentar 1g de una sustancia en 1°C | J/g°C | Intrínseca (propiedad del material) |
| Capacidad calorífica molar | Energía para calentar 1 mol de una sustancia en 1°C | J/mol°C | Útil para reacciones químicas |
El análisis térmico preciso es fundamental para el éxito de tu laboratorio.
Comprender las propiedades térmicas precisas de tus materiales es fundamental para una investigación, desarrollo y control de calidad fiables. Ya sea que estés caracterizando nuevos materiales, optimizando un proceso térmico o seleccionando el equipo adecuado, los datos precisos de capacidad calorífica son innegociables.
KINTEK se especializa en proporcionar el equipo de laboratorio y los consumibles de alta calidad que necesitas para realizar estas mediciones críticas con confianza. Desde calorímetros hasta sistemas de control de temperatura, nuestras soluciones están diseñadas para ofrecer la precisión y fiabilidad que exigen los laboratorios.
Deja que KINTEK sea tu socio en precisión. Contacta a nuestros expertos hoy para discutir tu aplicación específica y descubrir cómo nuestros productos pueden mejorar tus capacidades de análisis térmico.
Guía Visual