En esencia, un electrodo es un puente. Es un conductor eléctrico utilizado para hacer contacto con una parte no metálica de un circuito, permitiendo que la corriente fluya entre ellos. Por ejemplo, los terminales positivo y negativo de cualquier batería son los puntos de conexión externos para dos electrodos internos sumergidos en una solución química.
La función esencial de un electrodo no es solo conducir electricidad, sino servir como la interfaz física donde la energía eléctrica se convierte en energía química (y viceversa) al liberar o aceptar electrones.

El papel fundamental de un electrodo
La función principal de un electrodo es resolver un problema fundamental: cómo hacer que la electricidad fluya a través de un material que no es un simple cable metálico.
Uniendo dos mundos
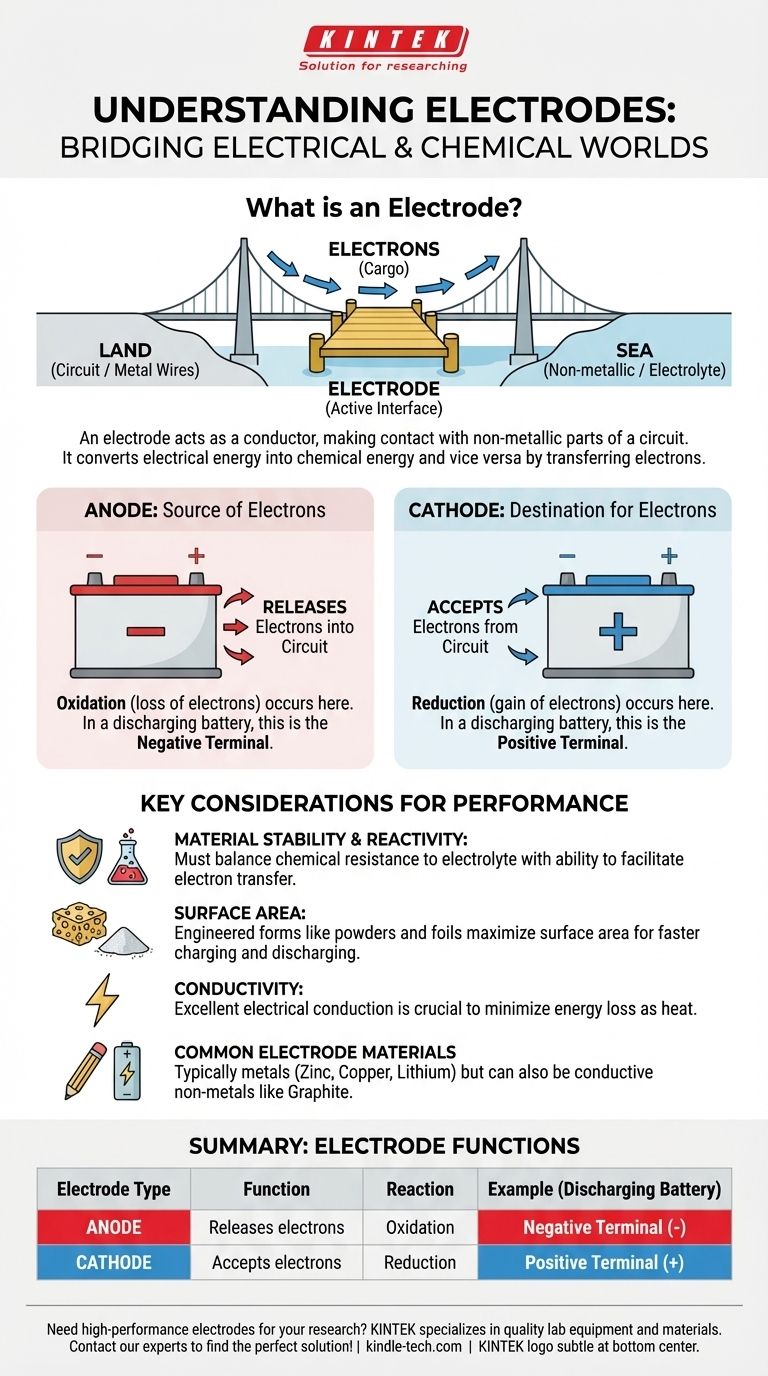
Piensa en un electrodo como un muelle especializado. Los cables metálicos en un circuito son la "tierra", y una sustancia no metálica como un electrolito líquido en una batería es el "mar". El electrodo es el muelle donde los electrones (la "carga") se transfieren entre la tierra y el mar.
Estas sustancias no metálicas pueden incluir electrolitos (en baterías), semiconductores (en transistores), gases (en letreros de neón) o incluso el vacío (en antiguas válvulas de vacío).
Un sitio para reacciones químicas
En muchas aplicaciones, especialmente baterías, los electrodos no son conductores pasivos. Son participantes activos en reacciones químicas.
La superficie de un electrodo es donde tiene lugar la oxidación (la pérdida de electrones) o la reducción (la ganancia de electrones). Esta reacción química controlada es lo que permite a una batería almacenar y liberar energía.
Materiales comunes de los electrodos
Aunque típicamente están hechos de metales como zinc, cobre o litio, los electrodos no son exclusivamente metálicos. Cualquier buen conductor eléctrico puede servir.
Por ejemplo, el grafito (una forma de carbono) es un material de electrodo muy común utilizado en baterías y electrólisis industrial porque es un excelente conductor y es químicamente estable.
Ánodos y cátodos: los dos tipos clave
En cualquier sistema con dos electrodos, se les dan nombres específicos basados en la reacción química que ocurre en su superficie. Estas etiquetas son cruciales para entender cómo funcionan las celdas electroquímicas.
El ánodo: la fuente de electrones
El ánodo se define como el electrodo donde ocurre la oxidación. En términos simples, es el electrodo que libera electrones al circuito.
En una batería que está alimentando un dispositivo (descargándose), el ánodo es el terminal negativo.
El cátodo: el destino de los electrones
El cátodo es el electrodo donde ocurre la reducción. Es el electrodo que acepta los electrones que vienen del circuito.
En una batería que se está descargando, el cátodo es el terminal positivo.
Comprendiendo las consideraciones clave
Elegir un material para el electrodo es una decisión de diseño crítica que implica equilibrar varios factores contrapuestos.
Estabilidad y reactividad del material
Un electrodo debe ser químicamente lo suficientemente estable como para sobrevivir en su entorno, que a menudo es un electrolito corrosivo. Si se degrada demasiado rápido, el dispositivo fallará.
Al mismo tiempo, debe ser lo suficientemente reactivo como para facilitar la transferencia de electrones deseada. Este equilibrio entre estabilidad y reactividad es clave para el rendimiento.
Área de superficie y rendimiento
La velocidad de una reacción química a menudo está limitada por el área de superficie disponible. Debido a esto, muchos electrodos modernos no son bloques sólidos de metal.
En cambio, se diseñan a partir de polvos, láminas o espumas para crear una enorme área de superficie en un pequeño volumen. Esto aumenta la potencia de salida del dispositivo, permitiéndole cargarse y descargarse más rápidamente.
La conductividad no es negociable
Por encima de todo, el material debe ser un excelente conductor eléctrico. Cualquier resistencia en el propio electrodo desperdicia energía en forma de calor, reduciendo la eficiencia general del dispositivo.
Tomar la decisión correcta para su objetivo
Los términos ánodo y cátodo están ligados a la dirección del flujo de electrones, por lo que su ubicación física depende del contexto.
- Si está mirando una batería: El terminal positivo (+) es la conexión externa para el cátodo, y el terminal negativo (-) es la conexión para el ánodo.
- Si está estudiando electrólisis (usando electricidad para impulsar una reacción): El electrodo conectado al lado positivo de la fuente de alimentación es el ánodo, y el conectado al lado negativo es el cátodo.
- Si está trabajando con un dispositivo semiconductor: Los electrodos son los contactos metálicos nombrados (por ejemplo, fuente, drenaje, puerta) que le permiten controlar el flujo de corriente a través del silicio.
Comprender el papel de un electrodo es el primer paso para dominar cómo la tecnología moderna almacena, libera y controla la energía eléctrica.
Tabla resumen:
| Tipo de electrodo | Función | Reacción | Ejemplo (Batería descargándose) |
|---|---|---|---|
| Ánodo | Libera electrones al circuito | Oxidación (pérdida de electrones) | Terminal Negativo (-) |
| Cátodo | Acepta electrones del circuito | Reducción (ganancia de electrones) | Terminal Positivo (+) |
¿Necesita electrodos de alto rendimiento o equipos de laboratorio para su investigación? Elegir el material de electrodo adecuado es fundamental para la eficiencia y la longevidad de sus dispositivos. KINTEK se especializa en proporcionar equipos y consumibles de laboratorio de alta calidad, incluidos materiales de electrodo estables y conductores, para impulsar sus innovaciones. Contacte a nuestros expertos hoy para discutir su aplicación específica y encontrar la solución perfecta para sus necesidades de laboratorio.
Guía Visual
Productos relacionados
- Electrodo de Referencia Calomel Plata Cloruro Mercurio Sulfato para Uso en Laboratorio
- Electrodo Electroquímico de Disco Metálico
- Electrodo de disco giratorio (disco de anillo) RRDE / compatible con PINE, ALS japonés, Metrohm suizo de carbono vítreo platino
- Electrodo de disco de platino giratorio para aplicaciones electroquímicas
- Electrodo de lámina de platino para aplicaciones de laboratorio de baterías
La gente también pregunta
- ¿Qué electrodo se utiliza como referencia de tierra? Domine la clave para mediciones electroquímicas precisas
- ¿Por qué es fundamental la selección de un electrodo de referencia de alta calidad en la síntesis electroquímica? | KINTEK
- ¿Qué es el electrodo de referencia en potenciometría? La clave para mediciones estables y precisas
- ¿Cuál es el mantenimiento recomendado para la solución de relleno de un electrodo de referencia? Una guía para lecturas estables y precisas
- ¿Cuál es el propósito del electrodo de referencia? Lograr mediciones electroquímicas estables y precisas



















