En resumen, una atmósfera reductora es un entorno gaseoso controlado donde el oxígeno ha sido eliminado intencionalmente y reemplazado por gases que previenen la oxidación y promueven activamente la reducción química. Este tipo de atmósfera es rica en "agentes reductores" como el hidrógeno (H₂), el monóxido de carbono (CO) o el sulfuro de hidrógeno (H₂S), que están químicamente ansiosos por donar electrones y eliminar el oxígeno de otros materiales.
Una atmósfera reductora no se trata simplemente de la ausencia de oxígeno; es un entorno químico activo diseñado para forzar una reacción específica. Funciona creando un excedente de electrones, obligando a los materiales dentro de ella a ganar esos electrones y volver a un estado menos oxidado.

La química fundamental en juego
Para comprender verdaderamente una atmósfera reductora, primero debe comprender el principio químico fundamental en el que se basa: la oxidación y la reducción. Son dos caras de la misma moneda, un proceso a menudo denominado "redox".
Comprender la oxidación y la reducción
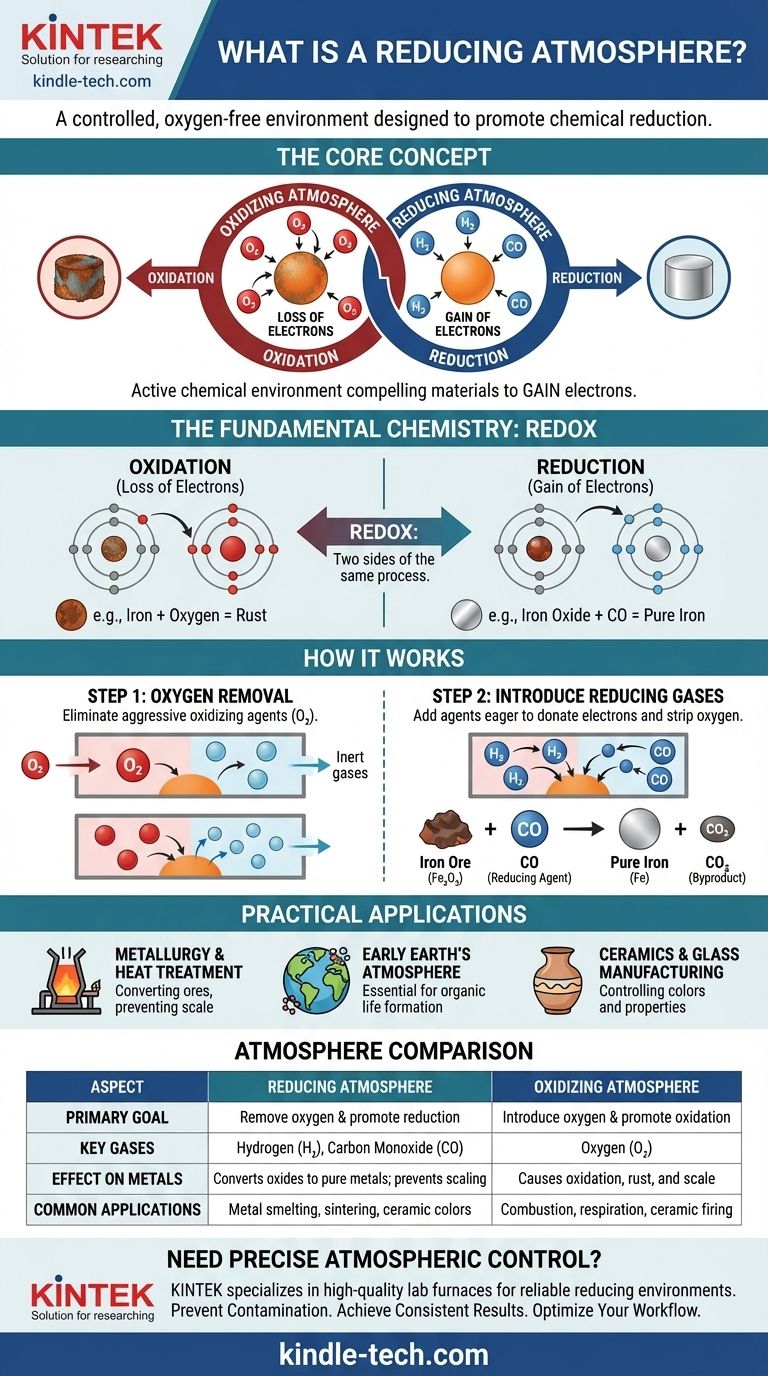
La oxidación es la pérdida de electrones. Un ejemplo clásico es el óxido del hierro. El oxígeno en el aire extrae electrones de los átomos de hierro, formando óxido de hierro (herrumbre). El hierro se "oxida".
La reducción es la ganancia de electrones. Es lo opuesto químico de la oxidación. Una atmósfera reductora facilita este proceso al crear un entorno donde los átomos se ven obligados a aceptar electrones.
Piense en ello como una guerra de tira y afloja química por los electrones. Un agente oxidante, como el oxígeno, es fuerte y arrastra electrones lejos de otros materiales. Un agente reductor, como el hidrógeno, es generoso y dona electrones a otros materiales.
El papel de la eliminación de oxígeno
El primer y más crítico paso para crear una atmósfera reductora es la eliminación del oxígeno libre (O₂) y otros gases oxidantes.
El oxígeno es un agente oxidante muy agresivo. Su presencia hace casi imposible realizar una reacción de reducción, ya que implacablemente extraerá electrones de cualquier fuente disponible. Eliminarlo previene que ocurra esta oxidación no deseada.
La función de los gases reductores
Simplemente eliminar el oxígeno crea una atmósfera neutra o inerte. Para convertirla en una atmósfera reductora, se introducen gases específicos.
Estos gases, generalmente hidrógeno (H₂) o monóxido de carbono (CO), actúan como potentes agentes reductores. Tienen una mayor afinidad por el oxígeno que muchos otros elementos, lo que significa que "robarán" activamente átomos de oxígeno de compuestos como los óxidos metálicos.
Por ejemplo, cuando el mineral de hierro (óxido de hierro, Fe₂O₃) se calienta en un horno con monóxido de carbono, el CO elimina el oxígeno del hierro, dejando atrás hierro puro líquido y creando dióxido de carbono (CO₂) como subproducto. El mineral de hierro ha sido "reducido" a hierro.
Aplicaciones prácticas y contexto
Las atmósferas reductoras no son solo un concepto teórico; son una herramienta crítica en muchos procesos industriales y científicos donde se requiere un control químico preciso.
Metalurgia y tratamiento térmico
Esta es la aplicación más común. Los altos hornos utilizan una atmósfera reductora rica en monóxido de carbono para transformar minerales metálicos en metales puros. También se utiliza en el recocido y la sinterización para prevenir la formación de óxidos (cascarilla) en la superficie de los metales durante el procesamiento a alta temperatura.
La atmósfera de la Tierra primitiva
Los científicos teorizan que la atmósfera primordial de la Tierra era reductora, contenía metano, amoníaco y vapor de agua, pero prácticamente nada de oxígeno libre. Este entorno fue esencial para la formación de las moléculas orgánicas complejas que finalmente dieron lugar a la vida.
Fabricación de cerámica y vidrio
La atmósfera dentro de un horno tiene un profundo efecto en el producto final. Se puede utilizar una atmósfera reductora para crear colores y propiedades específicas en esmaltes cerámicos y vidrio al cambiar el estado de oxidación de los óxidos metálicos utilizados como colorantes. Por ejemplo, el óxido de cobre produce verde en un fuego oxidante, pero un rojo intenso en uno reductor.
Comprender las compensaciones: Oxidante frente a reductor
Lo opuesto a una atmósfera reductora es una atmósfera oxidante, que es rica en oxígeno. La atmósfera actual de nuestro planeta es un excelente ejemplo.
La atmósfera oxidante
Una atmósfera oxidante promueve la pérdida de electrones. Es esencial para procesos como la combustión (quemado) y la respiración celular (respiración), pero es destructiva en otros contextos, causando corrosión, deterioro y degradación.
Por qué el control atmosférico es fundamental
La elección entre una atmósfera reductora, inerte u oxidante está determinada enteramente por el resultado deseado. Usar la incorrecta no solo es ineficiente; puede ser catastrófico para un proceso.
Intentar fundir metal en un ambiente rico en oxígeno fracasaría, produciendo en su lugar más óxidos y cascarilla. Por el contrario, cocer una cerámica que requiere oxidación en una atmósfera reductora daría como resultado colores incorrectos e impredecibles.
Cómo aplicar este conocimiento
Comprender el propósito de una atmósfera específica se reduce a identificar la transformación química deseada.
- Si el objetivo principal es prevenir la degradación: Se utiliza una atmósfera inerte o reductora para eliminar el oxígeno, el principal agente de corrosión y deslustre.
- Si el objetivo principal es transformar un material de un óxido a su forma pura: Se requiere una atmósfera reductora para despojar activamente a los átomos de oxígeno del material (por ejemplo, convertir mineral en metal).
- Si el objetivo principal es controlar las propiedades finales de un compuesto: El equilibrio entre oxidación y reducción se utiliza para manipular el estado electrónico de los elementos, controlando así resultados como el color en cerámicas o la conductividad en semiconductores.
En última instancia, saber si una atmósfera está diseñada para donar o aceptar electrones es la clave para predecir y controlar los resultados químicos.
Tabla de resumen:
| Aspecto | Atmósfera Reductora | Atmósfera Oxidante |
|---|---|---|
| Objetivo Principal | Eliminar el oxígeno y promover la reducción (ganancia de electrones) | Introducir oxígeno y promover la oxidación (pérdida de electrones) |
| Gases Clave | Hidrógeno (H₂), Monóxido de Carbono (CO) | Oxígeno (O₂) |
| Efecto en Metales | Convierte óxidos metálicos en metales puros; previene la formación de cascarilla | Causa oxidación, lo que lleva a herrumbre y cascarilla |
| Aplicaciones Comunes | Fundición de metales, recocido, sinterización, esmaltes cerámicos específicos | Combustión, respiración, cocción de ciertas cerámicas |
¿Necesita un control atmosférico preciso para sus procesos de laboratorio?
Ya sea que esté sinterizando metales, desarrollando esmaltes cerámicos especializados o realizando investigaciones que requieran un entorno libre de oxígeno, el equipo adecuado es fundamental. KINTEK se especializa en proporcionar hornos y reactores de laboratorio de alta calidad diseñados para un control atmosférico preciso, incluida la creación de entornos reductores confiables.
Le ayudamos a:
- Prevenir la Contaminación: Asegúrese de que sus materiales no se degraden por una oxidación no deseada.
- Lograr Resultados Consistentes: Obtenga las transformaciones químicas precisas que necesita, lote tras lote.
- Optimizar su Flujo de Trabajo: Con equipos diseñados para confiabilidad y facilidad de uso.
¿Listo para mejorar las capacidades de su laboratorio? Contacte a KINTEK hoy para discutir sus necesidades específicas de laboratorio y cómo nuestras soluciones pueden impulsar su éxito.
Guía Visual
Productos relacionados
- Horno de atmósfera controlada de 1200℃, horno de atmósfera inerte de nitrógeno
- Horno de Atmósfera Controlada de 1700 ℃ Horno de Atmósfera Inerte de Nitrógeno
- Horno de atmósfera controlada de 1400 ℃ con nitrógeno y atmósfera inerte
- Horno de Atmósfera de Hidrógeno y Nitrógeno Controlado
- Horno de atmósfera controlada con cinta de malla
La gente también pregunta
- ¿Cuál es la necesidad de hornos de atmósfera controlada para la corrosión por gas? Asegure un modelado preciso de fallas de materiales
- ¿Cuál es el papel de la atmósfera del horno? Domine el control metalúrgico preciso para su tratamiento térmico
- ¿Qué es un horno de atmósfera controlada? Logre pureza y precisión en el procesamiento a alta temperatura
- ¿Cuál es la necesidad de un horno de atmósfera controlada para la investigación de la corrosión? Replicando Riesgos Industriales Realistas
- ¿Cuáles son los dos propósitos principales del uso de una atmósfera controlada? Protección maestra vs. Modificación de materiales















