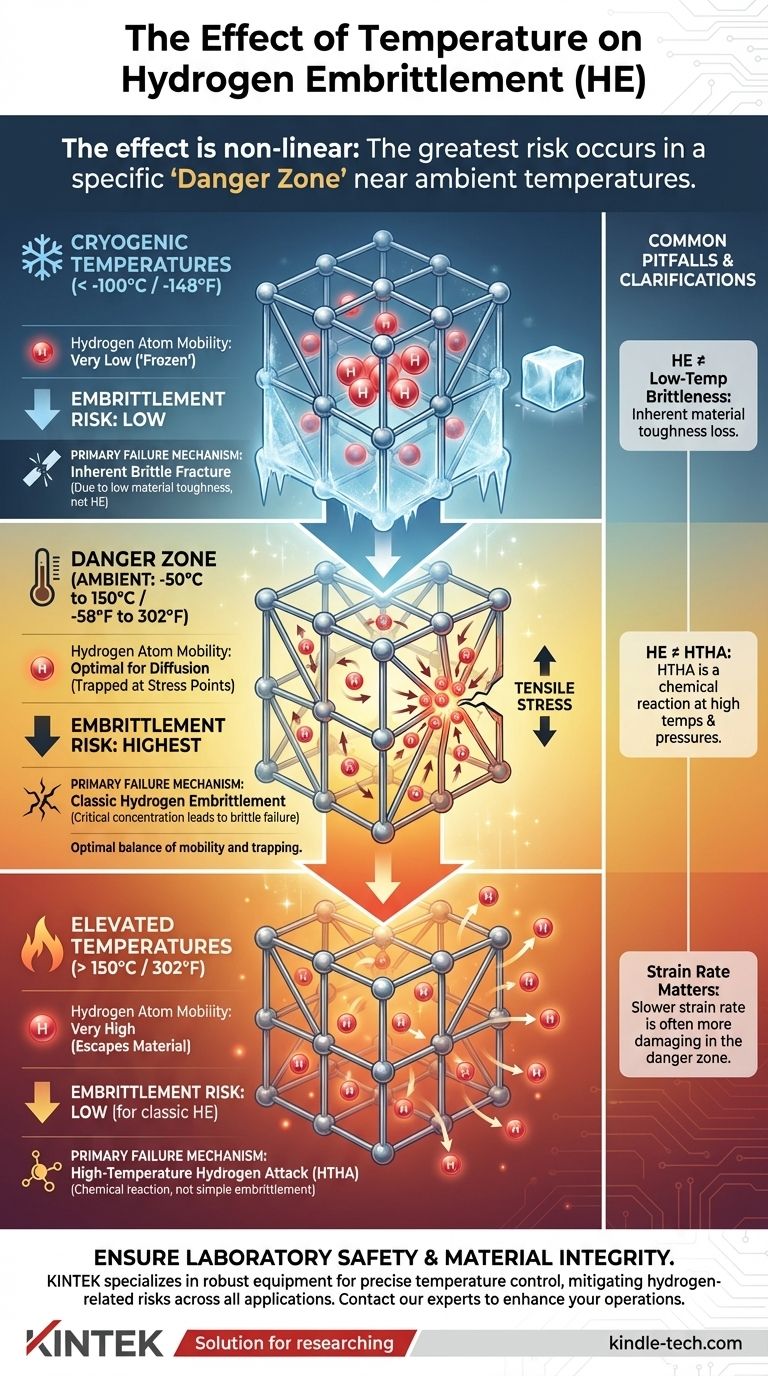
En resumen, el efecto de la temperatura en la fragilización por hidrógeno no es lineal. El fenómeno es más severo en un rango específico alrededor de la temperatura ambiente. Tanto las temperaturas muy bajas (criogénicas) como las elevadas reducen significativamente el riesgo de fragilización por hidrógeno clásica, pero por razones completamente diferentes relacionadas con la movilidad de los átomos de hidrógeno.
El mayor riesgo de falla por fragilización por hidrógeno ocurre cerca de las temperaturas ambiente, aproximadamente entre -50°C y 150°C (-58°F y 302°F). Esta ventana de temperatura crea un equilibrio peligroso donde los átomos de hidrógeno son lo suficientemente móviles para encontrar puntos de tensión, pero no tan energéticos como para escapar del material.

La mecánica subyacente: Movilidad del hidrógeno
Para comprender el papel de la temperatura, primero debemos reconocer que la fragilización por hidrógeno requiere tres condiciones: un material susceptible (como el acero de alta resistencia), tensión de tracción aplicada y una fuente de hidrógeno atómico. El papel principal de la temperatura es gobernar el comportamiento de estos átomos de hidrógeno dentro de la red cristalina del metal.
H3: La "Zona de Peligro" (Temperaturas Cercanas a la Ambiente)
Este rango representa el mayor riesgo porque proporciona las condiciones óptimas para la fragilización.
Los átomos de hidrógeno tienen suficiente energía térmica para difundirse, o moverse, a través del metal. Esta movilidad les permite migrar y acumularse en áreas de alta tensión, como la punta de una grieta microscópica.
Simultáneamente, la temperatura no es lo suficientemente alta como para que el hidrógeno se difunda fácilmente de nuevo fuera del material. Esta combinación de movilidad suficiente y atrapamiento efectivo conduce a una concentración crítica de hidrógeno en los puntos de tensión, lo que reduce severamente la ductilidad del material y provoca una falla frágil repentina.
H3: Bajas Temperaturas (Condiciones Criogénicas)
A medida que la temperatura desciende significativamente (por ejemplo, por debajo de -100°C / -148°F), el riesgo de fragilización por hidrógeno clásica disminuye.
A estas temperaturas criogénicas, la tasa de difusión de los átomos de hidrógeno se vuelve extremadamente lenta. Los átomos están esencialmente "congelados en su lugar" dentro de la red metálica.
Debido a que carecen de la movilidad para viajar a áreas de alta tensión de tracción, no pueden acumularse a las concentraciones críticas necesarias para causar fragilización.
H3: Temperaturas Elevadas
A temperaturas más altas (por ejemplo, por encima de 150°C / 302°F), el riesgo de fragilización por hidrógeno clásica también disminuye, pero por la razón opuesta.
La tasa de difusión del hidrógeno se vuelve muy alta. Esta movilidad extrema significa que los átomos de hidrógeno pueden difundirse fácilmente fuera del material hacia la atmósfera, lo que evita acumulaciones internas peligrosas.
Además, a estas temperaturas, el metal en sí se vuelve más dúctil y su límite elástico disminuye, lo que lo hace inherentemente menos propenso a la fractura frágil.
Errores comunes y aclaraciones
Una comprensión clara del efecto de la temperatura requiere diferenciar la fragilización por hidrógeno de otros mecanismos de falla dependientes de la temperatura.
H3: No confundir la FH con la fragilidad a baja temperatura
Aunque el riesgo de FH es bajo a temperaturas criogénicas, el riesgo de un modo de falla diferente—la fractura frágil—es muy alto para muchos aceros. Esto se debe a la pérdida inherente de tenacidad en el material a bajas temperaturas y es un fenómeno separado.
H3: Distinguir la FH del ataque por hidrógeno a alta temperatura (HTHA)
A temperaturas muy altas (típicamente por encima de 200°C / 400°F) y en ambientes de gas hidrógeno a alta presión, puede ocurrir un mecanismo diferente llamado Ataque por Hidrógeno a Alta Temperatura (HTHA).
Este no es un simple proceso de fragilización, sino una reacción química. El hidrógeno reacciona con los carburos en el acero para formar gas metano, lo que provoca agrietamiento interno, ampollamiento y una pérdida permanente de resistencia. El HTHA es una forma fundamentalmente diferente e irreversible de degradación del material.
H3: Considere el impacto de la tasa de deformación
El proceso de fragilización depende del tiempo. En la "zona de peligro", una tasa de deformación más lenta es a menudo más dañina porque da a los átomos de hidrógeno más tiempo para difundirse hasta la punta de una grieta en propagación, exacerbando el problema.
Tomar la decisión correcta para su aplicación
Su enfoque para mitigar las fallas relacionadas con el hidrógeno debe adaptarse al rango de temperatura operativa específico de su componente.
- Si su enfoque principal es el servicio criogénico (por debajo de -100°C): Su principal preocupación es la tenacidad intrínseca del material, no la fragilización por hidrógeno clásica. Seleccione materiales con excelentes valores de impacto Charpy V-notch a su temperatura mínima de diseño.
- Si su componente opera cerca de las temperaturas ambiente (-50°C a 150°C): Usted se encuentra en la zona de mayor riesgo. Dé prioridad a la selección de materiales menos susceptibles, controle rigurosamente todas las fuentes potenciales de hidrógeno (por ejemplo, procesos de fabricación como el plateado, la soldadura o la corrosión en servicio) y gestione cuidadosamente las tensiones de tracción.
- Si opera a temperaturas elevadas (por encima de 150°C): El riesgo de fragilización clásica es menor, pero debe cambiar su análisis al riesgo separado y severo del Ataque por Hidrógeno a Alta Temperatura (HTHA), especialmente para aceros al carbono y de baja aleación en servicio con hidrógeno.
En última instancia, la temperatura es la variable crítica que dicta si el hidrógeno dentro de un material es un pasajero benigno o un catalizador para una falla catastrófica.
Tabla de resumen:
| Rango de Temperatura | Movilidad del Átomo de Hidrógeno | Riesgo de Fragilización | Mecanismo de Falla Principal |
|---|---|---|---|
| Criogénico (< -100°C / -148°F) | Muy Baja ("Congelada") | Bajo | Fractura Frágil Inherente (Tenacidad del Material) |
| Zona de Peligro (-50°C a 150°C / -58°F a 302°F) | Óptima para Difusión | Más Alto | Fragilización por Hidrógeno Clásica |
| Elevada (> 150°C / 302°F) | Muy Alta (Escapa del Material) | Bajo (para FH) | Ataque por Hidrógeno a Alta Temperatura (HTHA) |
Asegure que los materiales y equipos de su laboratorio estén a salvo de fallas relacionadas con el hidrógeno. KINTEK se especializa en proporcionar equipos y consumibles de laboratorio robustos diseñados para un control preciso de la temperatura y la integridad del material. Ya sea que trabaje con aplicaciones criogénicas, condiciones ambiente o procesos a alta temperatura, nuestras soluciones ayudan a mitigar los riesgos de fragilización por hidrógeno y otros mecanismos de falla. Contacte a nuestros expertos hoy mismo para discutir cómo podemos apoyar las necesidades específicas de su laboratorio y mejorar la seguridad y confiabilidad de sus operaciones.
Guía Visual