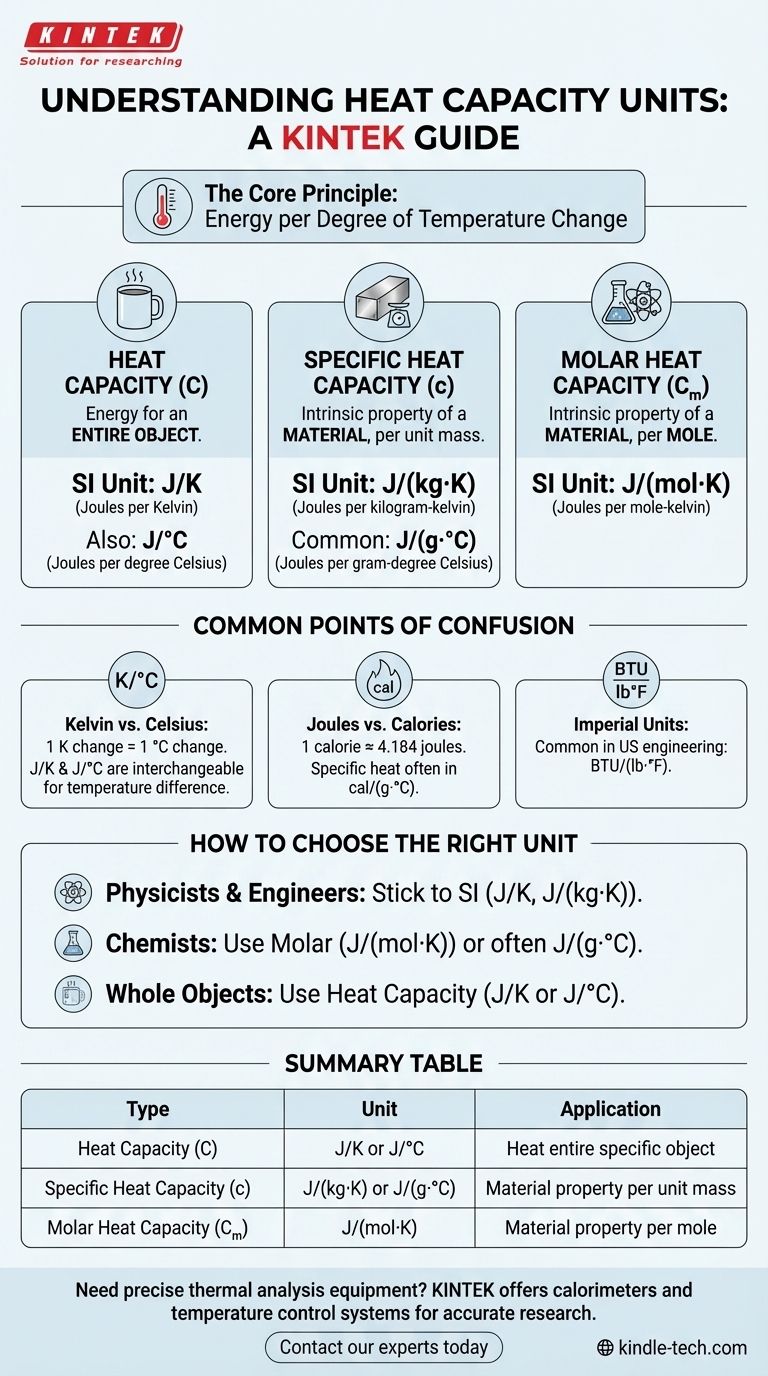
La unidad SI principal para la capacidad calorífica es el julio por kelvin (J/K). Esta unidad describe la cantidad de energía (en julios) necesaria para elevar la temperatura de un objeto o sistema completo en un grado Kelvin. Sin embargo, las unidades específicas que encuentre cambiarán dependiendo de si está midiendo un objeto completo, una masa específica de una sustancia o una cantidad molar.
Las unidades de capacidad calorífica siempre representan energía por grado de cambio de temperatura. Comprender la diferencia entre capacidad calorífica, capacidad calorífica específica y capacidad calorífica molar es la clave para identificar y utilizar la unidad correcta para su cálculo.

Lo que realmente significan las unidades
Capacidad Calorífica (C)
La capacidad calorífica se refiere a la energía necesaria para elevar la temperatura de un objeto completo en un grado. Debido a que es para un objeto específico y completo (como una taza de café o el bloque de un motor), su masa ya está incluida.
La unidad es simplemente energía dividida por temperatura: julios por kelvin (J/K). También puede verla expresada como julios por grado Celsius (J/°C).
Capacidad Calorífica Específica (c)
Esta es la medida más común que encontrará. El calor específico es una propiedad intrínseca de un material, no de un objeto. Es la energía requerida para elevar la temperatura de una unidad de masa de una sustancia en un grado.
La unidad SI estándar es julios por kilogramo-kelvin (J/(kg·K)).
En química y otros contextos de laboratorio, es muy común ver unidades basadas en gramos y Celsius, como julios por gramo-grado Celsius (J/(g·°C)).
Capacidad Calorífica Molar (Cₘ)
La capacidad calorífica molar también es una propiedad intrínseca de un material, pero se define por mol en lugar de por masa. Esto es particularmente útil en química, donde las reacciones se describen en términos de moles.
La unidad SI estándar es julios por mol-kelvin (J/(mol·K)).
Puntos comunes de confusión
Kelvin frente a Celsius
Para los cálculos de capacidad calorífica, un cambio de un grado Kelvin (1 K) es exactamente el mismo que un cambio de un grado Celsius (1 °C).
Por lo tanto, las unidades J/K y J/°C son funcionalmente intercambiables cuando se calcula una diferencia de temperatura. Lo mismo ocurre con J/(kg·K) y J/(kg·°C).
Julios frente a Calorías
La caloría (cal) es una unidad de energía más antigua, no SI. Todavía se utiliza en algunos contextos, particularmente en química y nutrición.
La conversión es aproximadamente 1 caloría = 4.184 julios. Puede ver el calor específico expresado como cal/(g·°C). Por ejemplo, el calor específico del agua es muy cercano a 1.0 cal/(g·°C).
Unidades Imperiales y Consuetudinarias de EE. UU.
En algunos campos de la ingeniería, particularmente en los Estados Unidos, puede encontrar unidades imperiales.
La unidad más común para el calor específico en este sistema es la Unidad Térmica Británica por libra por grado Fahrenheit (BTU/(lb·°F)).
Cómo elegir la unidad correcta para su aplicación
-
Si es físico o ingeniero: Cíñase a las unidades SI estándar. Utilice J/K para sistemas completos y J/(kg·K) para propiedades del material.
-
Si es químico: La capacidad calorífica molar (J/(mol·K)) suele ser la más útil para los cálculos de reacciones, aunque con frecuencia utilizará J/(g·°C) para el trabajo de laboratorio.
-
Si está trabajando con un objeto específico y completo: Utilice la unidad general de capacidad calorífica, J/K o J/°C, ya que la masa del objeto ya está contabilizada.
Comprender qué cantidad se está midiendo —un objeto completo, una unidad de masa o un mol— es la guía definitiva para elegir la unidad correcta.
Tabla de resumen:
| Tipo de Capacidad Calorífica | Unidad | Aplicación |
|---|---|---|
| Capacidad Calorífica (C) | J/K o J/°C | Energía para calentar un objeto específico y completo |
| Capacidad Calorífica Específica (c) | J/(kg·K) o J/(g·°C) | Propiedad intrínseca de un material (por unidad de masa) |
| Capacidad Calorífica Molar (Cₘ) | J/(mol·K) | Propiedad intrínseca de un material (por mol) |
¿Necesita equipos de análisis térmico precisos para su laboratorio? Comprender la capacidad calorífica es crucial para los experimentos en química, ciencia de materiales e ingeniería. KINTEK se especializa en equipos de laboratorio de alta calidad, incluidos calorímetros y sistemas de control de temperatura, para garantizar que sus mediciones sean precisas y fiables. Póngase en contacto con nuestros expertos hoy mismo para encontrar la solución perfecta para las necesidades de análisis térmico de su laboratorio.
Guía Visual