En esencia, la liofilización de laboratorio preserva los productos biológicos eliminando el agua sin destruir su delicada estructura. El proceso, formalmente conocido como liofilización, implica congelar el material hasta que esté sólido y luego usar un vacío de alta presión para transformar el hielo directamente en vapor, un proceso llamado sublimación. Esto evita por completo la fase líquida dañina, dejando intacta la arquitectura celular y química del producto.
La ventaja fundamental de la liofilización no es solo la eliminación del agua, sino el método de eliminación. Al convertir el hielo sólido directamente en gas, evita el estrés físico y la contracción que el agua líquida causa al salir de una estructura delicada, asegurando la máxima preservación de las propiedades originales del producto.

La ciencia detrás de la liofilización
La liofilización es un proceso de múltiples etapas regido por un principio físico clave. Comprender este principio es crucial para apreciar por qué es tan eficaz para materiales sensibles como enzimas, vacunas y cultivos celulares.
El principio de la sublimación
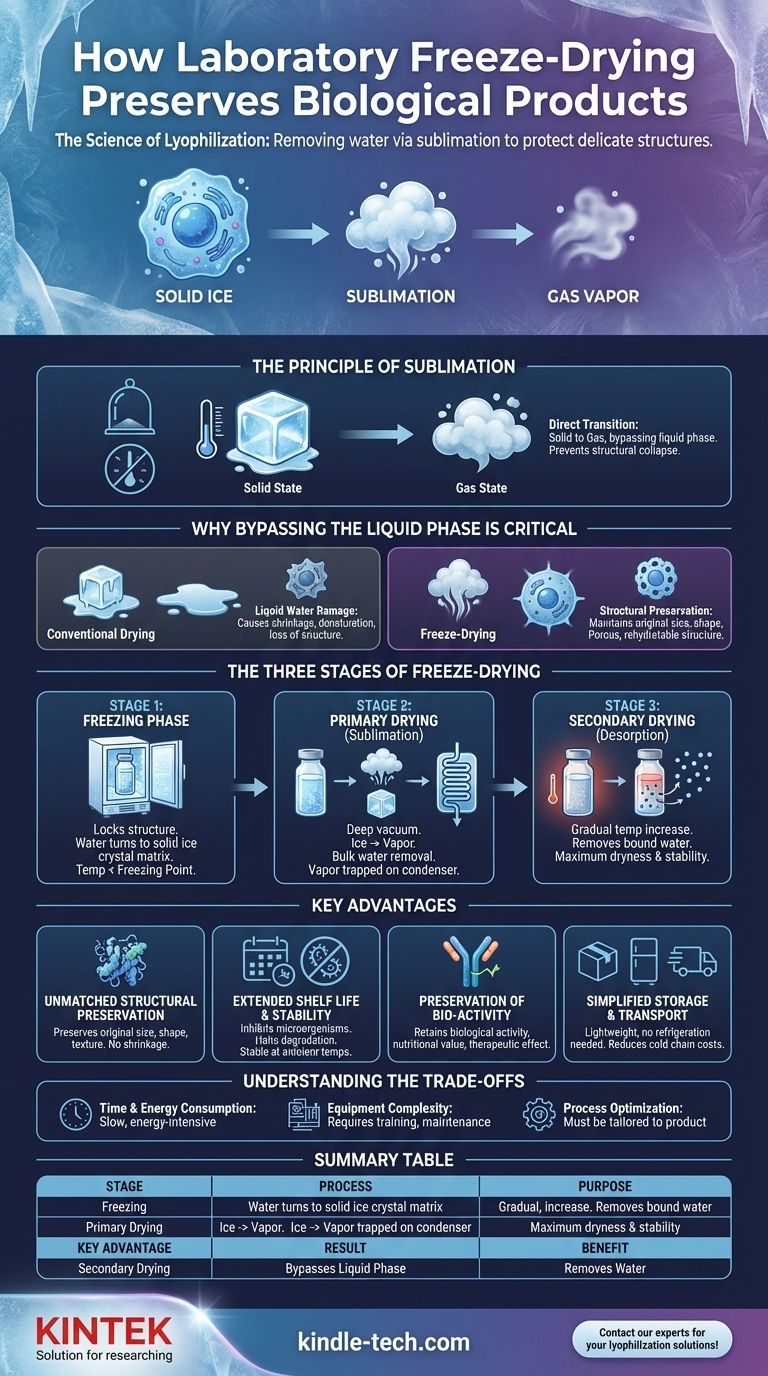
La sublimación es la transición directa de una sustancia de un estado sólido a uno gaseoso, sin pasar nunca por una fase líquida. Un ejemplo común es el hielo seco, que se convierte directamente en gas de dióxido de carbono sin derretirse.
Los liofilizadores crean las condiciones específicas (baja temperatura y presión extremadamente baja) donde el agua hace lo mismo. Esto permite extraer el agua de un producto en forma de vapor mientras el producto en sí permanece congelado.
Por qué es fundamental evitar la fase líquida
Cuando los métodos de secado convencionales utilizan calor, el agua líquida es expulsada del material. Este movimiento puede dañar y colapsar estructuras celulares delicadas, lo que lleva a un producto final encogido, descolorido y, a menudo, desnaturalizado.
Al sublimar el agua, la estructura del producto permanece rígida y en su lugar. El resultado es una estructura porosa, similar a una esponja, que se puede rehidratar fácilmente más tarde, a menudo volviendo a su estado original con una fidelidad notable.
Las tres etapas de la liofilización
La liofilización es un proceso cuidadosamente controlado que se divide en tres fases distintas. Cada etapa tiene un propósito específico para eliminar suavemente el agua de la muestra.
Etapa 1: La fase de congelación
El primer paso es congelar completamente el producto. El material se lleva a una temperatura muy por debajo de su punto de congelación, asegurando que toda el agua se convierta en una matriz de cristales de hielo sólida y estable.
Esta congelación inicial es un paso crítico que fija la estructura del producto antes de que comience el proceso de secado.
Etapa 2: Secado primario (sublimación)
Una vez congelado, el producto se coloca bajo un vacío profundo. Este ambiente de baja presión es el catalizador de la sublimación.
A medida que los cristales de hielo se convierten en vapor de agua, este vapor se extrae del producto y se recolecta en una superficie de condensador extremadamente fría dentro del liofilizador, donde vuelve a convertirse en hielo. Esto atrapa eficazmente el agua eliminada, evitando que vuelva a contaminar la muestra.
Etapa 3: Secado secundario (desorción)
Después de que todos los cristales de hielo se han sublimado, una pequeña cantidad de moléculas de agua "ligadas" pueden permanecer adheridas a la superficie del producto.
En esta etapa final, la temperatura se eleva gradualmente mientras aún está bajo vacío. Esto proporciona la energía suficiente para romper los enlaces de estas últimas moléculas de agua, eliminándolas y logrando la máxima sequedad y estabilidad a largo plazo.
Ventajas clave sobre otros métodos de conservación
La liofilización ofrece varios beneficios distintos que la convierten en la opción superior para materiales biológicos delicados o de alto valor.
Preservación estructural inigualable
A diferencia del secado por calor que causa encogimiento o la simple congelación que puede causar daños por grandes cristales de hielo, la liofilización preserva el tamaño, la forma, el color y la textura originales del material.
Vida útil y estabilidad prolongadas
La eliminación del agua inhibe el crecimiento de microorganismos como bacterias y moho. También detiene las reacciones enzimáticas y químicas que causan la degradación, haciendo que los productos sean estables durante años a temperaturas ambiente.
Preservación de la bioactividad
Debido a que el proceso evita las altas temperaturas, los compuestos sensibles como proteínas, enzimas y anticuerpos no se desnaturalizan. Esto asegura que se retenga su actividad biológica, valor nutricional y eficacia terapéutica.
Almacenamiento y transporte simplificados
Los productos liofilizados son ligeros y no requieren refrigeración. Esto reduce drásticamente el costo y la complejidad del almacenamiento y envío, eliminando la necesidad de una costosa cadena de frío.
Comprender las compensaciones
Aunque es muy eficaz, la liofilización no está exenta de consideraciones. Es un proceso que consume muchos recursos y requiere una planificación cuidadosa.
Consumo de tiempo y energía
La liofilización es un proceso lento, que a menudo tarda muchas horas o incluso días en completarse. La combinación de congelación profunda y el mantenimiento de un alto vacío consume una cantidad significativa de energía, lo que lo hace más costoso que otros métodos.
Complejidad del equipo
Los liofilizadores de laboratorio son instrumentos sofisticados y caros. Requieren una capacitación adecuada del operador y un mantenimiento regular para funcionar correctamente y lograr resultados consistentes y confiables para muestras sensibles.
La optimización del proceso es crucial
La liofilización no es una solución única para todos. Los parámetros de congelación, nivel de vacío y temperatura deben optimizarse cuidadosamente para cada producto específico para evitar daños y asegurar una conservación exitosa.
Tomar la decisión correcta para su objetivo
La decisión de utilizar la liofilización depende completamente de la naturaleza de su muestra y de su objetivo final.
- Si su enfoque principal es la estabilidad a largo plazo para vacunas, anticuerpos o productos farmacéuticos: La liofilización es el estándar de oro para crear un producto estable a temperatura ambiente, fácil de transportar y listo para la rehidratación.
- Si su enfoque principal es preservar la estructura celular de los tejidos para el análisis: La liofilización es superior para prevenir el daño por cristales de hielo y la contracción comunes con otros métodos de deshidratación.
- Si su enfoque principal es mantener el valor nutricional y la bioactividad de enzimas o suplementos: Este método evita la degradación por calor de compuestos sensibles que ocurre durante el secado convencional.
Al dominar los principios de la liofilización, puede asegurar la integridad y viabilidad a largo plazo de sus materiales biológicos más delicados.
Tabla resumen:
| Etapa clave | Proceso | Propósito |
|---|---|---|
| Congelación | Solidifica toda el agua en hielo | Fija la estructura del producto en su lugar |
| Secado primario | Sublima el hielo a vapor bajo vacío | Elimina la mayor parte del agua sin dañarla |
| Secado secundario | Elimina las moléculas de agua ligadas | Logra la máxima sequedad y estabilidad |
| Ventaja clave | Resultado | Beneficio |
| Evita la fase líquida | Estructura porosa e intacta | Preserva la integridad celular y la bioactividad |
| Elimina el agua | Producto ligero y estable | Permite el almacenamiento y transporte a temperatura ambiente |
¿Listo para preservar sus muestras biológicas más valiosas con precisión?
KINTEK se especializa en proporcionar equipos y consumibles de liofilización de laboratorio confiables adaptados a sus necesidades de investigación. Nuestras soluciones le ayudan a lograr la máxima estabilidad de la muestra, preservar la bioactividad crítica y simplificar el almacenamiento, asegurando que sus enzimas, vacunas, cultivos celulares y productos farmacéuticos mantengan su integridad durante años.
¡Contacte a nuestros expertos hoy para encontrar el sistema de liofilización perfecto para su laboratorio!
Guía Visual
Productos relacionados
- Liofilizador de Laboratorio de Alto Rendimiento
- Liofilizadora de Laboratorio de Alto Rendimiento para Investigación y Desarrollo
- Liofilizador de laboratorio de sobremesa para uso en laboratorio
- Liofilizador de Vacío de Laboratorio de Sobremesa
- Congelador Vertical de Ultra Baja Temperatura (ULT) de 108L
La gente también pregunta
- ¿Qué precauciones se deben tomar al usar un liofilizador de laboratorio? Pasos esenciales para una liofilización fiable
- ¿Qué papel juega una liofilizadora de laboratorio en la síntesis de electrocatalizadores a base de grafeno? Conservar estructuras 3D
- ¿Cuáles son las ventajas técnicas de utilizar un liofilizador de laboratorio para precursores de carbono poroso? Preservación de redes 3D
- ¿Cuáles son los componentes principales de un liofilizador de laboratorio? Una guía de los 5 sistemas esenciales
- ¿Qué tipos de muestras líquidas se pueden procesar con una liofilizadora de laboratorio? Conserve sus materiales sensibles















