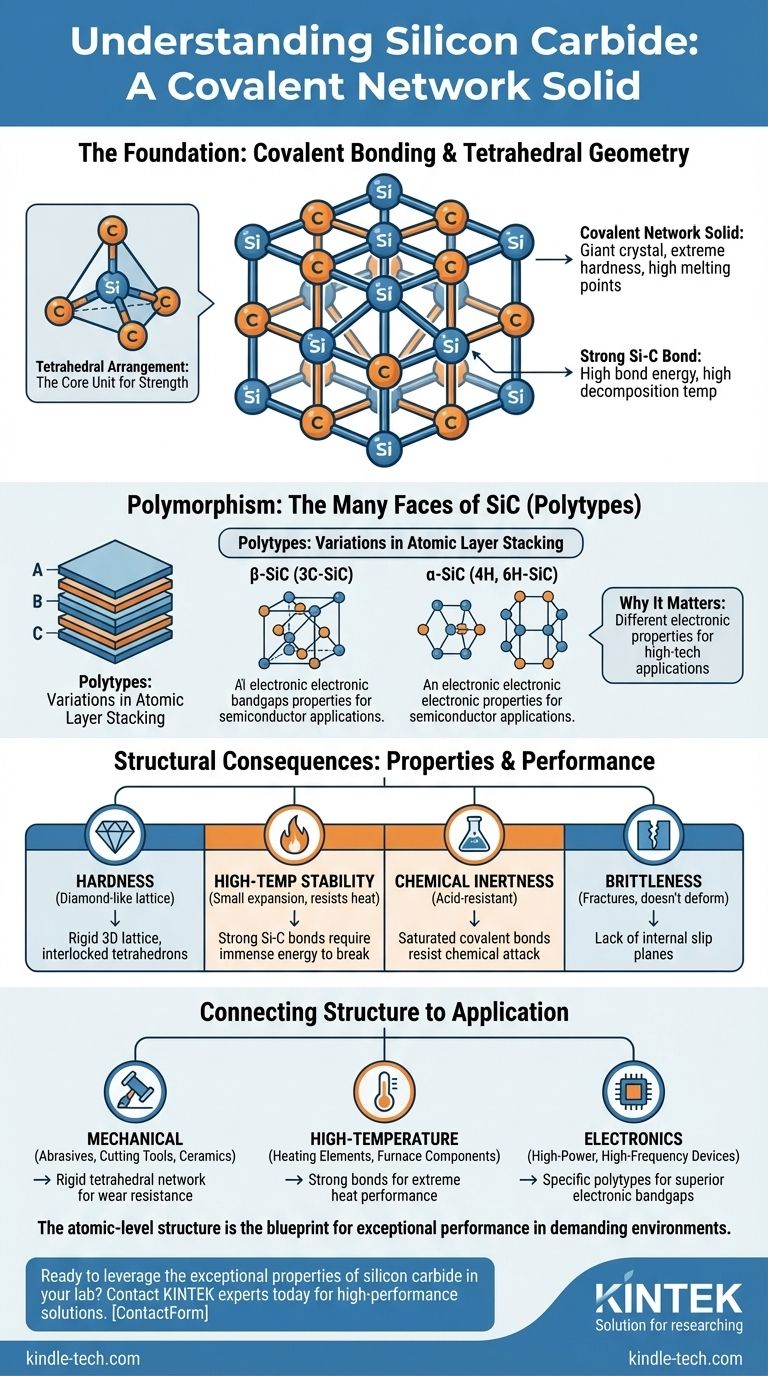
En su esencia, el carburo de silicio (SiC) es un sólido de red covalente. Esto significa que su estructura fundamental es una vasta red cristalina tridimensional construida a partir de átomos de silicio (Si) y carbono (C). Cada átomo está firmemente unido por fuertes enlaces covalentes en un patrón tetraédrico repetitivo, muy similar a la estructura del diamante. Esta disposición puede formarse en muchas variaciones de apilamiento diferentes, conocidas como politipos.
La cuestión de la estructura del carburo de silicio es fundamental para comprender sus notables propiedades. Su red covalente rígida, similar al diamante, es la causa directa de su excepcional dureza, estabilidad química y capacidad para soportar temperaturas extremas.

La base: Enlace covalente y geometría tetraédrica
La comprensión del SiC comienza con su disposición atómica. A diferencia de los metales con electrones libres o las sales unidas por atracción iónica, la fuerza del SiC proviene de fuertes enlaces de electrones compartidos que crean una única molécula masiva.
¿Qué es un sólido de red covalente?
Un sólido de red covalente es una sustancia donde los átomos están unidos por enlaces covalentes en una red continua que se extiende por todo el material. No existen moléculas individuales.
Todo el cristal es esencialmente una molécula gigante. Esta estructura es responsable de la dureza extrema y los altos puntos de fusión de materiales como el diamante y el carburo de silicio.
La disposición tetraédrica
En la red de SiC, cada átomo de silicio está químicamente unido a cuatro átomos de carbono vecinos. Del mismo modo, cada átomo de carbono está unido a cuatro átomos de silicio vecinos.
Esta disposición forma un tetraedro, una forma geométrica altamente estable y simétrica. Este patrón repetitivo de tetraedros entrelazados crea un marco increíblemente fuerte y rígido.
La fuerza del enlace Si-C
El enlace entre el silicio y el carbono es muy fuerte y relativamente corto. Se requiere una cantidad significativa de energía para romperlo.
Esta alta energía de enlace es la fuente directa de la alta temperatura de descomposición del SiC (se sublima en lugar de fundirse) y su dureza excepcional, que es superada por muy pocos materiales.
Polimorfismo: Las muchas caras del carburo de silicio
El carburo de silicio no es una única estructura. Exhibe un fenómeno llamado polimorfismo, lo que significa que puede existir en muchas estructuras cristalinas diferentes manteniendo la misma fórmula química (SiC). Estas diferentes formas se llaman politipos.
Comprendiendo los politipos
Los politipos son variaciones en la secuencia de apilamiento de las capas atómicas en el cristal. Imagine apilar capas de átomos representadas por A, B y C. Diferentes patrones repetitivos (como ABCABC... o ABAB...) dan como resultado diferentes estructuras cristalinas.
Aunque químicamente idénticos, estos politipos pueden tener propiedades físicas y, lo que es más importante, electrónicas distintas.
Categorías clave: α-SiC y β-SiC
Los cientos de politipos de SiC conocidos se agrupan ampliamente en dos categorías principales.
El Beta-SiC (β-SiC) se refiere al politipo cúbico (3C-SiC), que tiene una estructura similar a la blenda de zinc. El Alfa-SiC (α-SiC) abarca todos los demás politipos, que son principalmente hexagonales (como 4H-SiC y 6H-SiC) o romboédricos.
Por qué los politipos son importantes para las aplicaciones
La existencia de politipos no es solo un detalle académico; es fundamental para las aplicaciones de alta tecnología. Diferentes politipos tienen diferentes bandas prohibidas electrónicas, lo que determina sus propiedades semiconductoras.
Por ejemplo, el politipo 4H-SiC es el preferido para dispositivos electrónicos de alta potencia y alta frecuencia porque sus propiedades electrónicas son superiores para ese propósito específico, lo que sustenta su uso en el campo de los semiconductores avanzados.
Comprendiendo las consecuencias estructurales
Las propiedades enumeradas para el carburo de silicio (dureza, estabilidad y resistencia a la temperatura) son todas consecuencias directas de su estructura atómica subyacente.
Dureza extrema, pero alta fragilidad
La referencia señala que el SiC es "duro y frágil". La red covalente rígida que le proporciona su dureza extrema también significa que carece de los planos de deslizamiento internos que se encuentran en los metales.
Cuando se somete a una tensión más allá de lo que los enlaces pueden soportar, el cristal no puede deformarse permitiendo que los átomos se deslicen unos sobre otros. En cambio, se fractura catastróficamente, que es la definición de fragilidad.
Estabilidad a altas temperaturas
Los potentes enlaces Si-C requieren una inmensa energía térmica para vibrar y romperse. Por eso se describe al SiC como poseedor de un "pequeño coeficiente de expansión" y "buena resistencia al enfriamiento y calentamiento rápidos".
Esta estabilidad térmica lo convierte en un material ideal para elementos calefactores eléctricos de alta temperatura y componentes de hornos, ya que mantiene su integridad estructural a temperaturas donde la mayoría de los metales se derretirían o deformarían.
Inercia química
La referencia destaca la "buena estabilidad química" del SiC y señala que es "extremadamente resistente a los ácidos". Los enlaces covalentes estables y saturados no son fácilmente atacados o rotos por reactivos químicos.
Los electrones están firmemente unidos entre los átomos de silicio y carbono, dejando pocas oportunidades para que los ácidos u otros productos químicos reaccionen, lo que resulta en un material altamente duradero y no reactivo.
Conectando la estructura con la aplicación
Comprender la estructura atómica del carburo de silicio le permite seleccionarlo para el propósito correcto con confianza. Las propiedades no son arbitrarias; son el resultado directo de su red covalente.
- Si su enfoque principal es la resistencia mecánica y al desgaste: La red tetraédrica rígida e interconectada hace del SiC una opción ideal para abrasivos, herramientas de corte y cerámicas estructurales duraderas.
- Si su enfoque principal es el rendimiento a alta temperatura: La alta energía requerida para romper sus enlaces Si-C lo hace perfecto para elementos calefactores, componentes de hornos y materiales refractarios.
- Si su enfoque principal es la electrónica avanzada: Las distintas propiedades electrónicas de politipos específicos, como el 4H-SiC, son fundamentales para crear la próxima generación de dispositivos semiconductores de alta potencia y alta frecuencia.
En última instancia, la estructura a nivel atómico del carburo de silicio es el plan directo para su rendimiento excepcional en los entornos más exigentes del mundo.
Tabla resumen:
| Propiedad | Consecuencia de la estructura |
|---|---|
| Dureza | Red covalente 3D rígida de tetraedros entrelazados |
| Estabilidad a alta temperatura | Los fuertes enlaces Si-C requieren una inmensa energía para romperse |
| Inercia química | Los enlaces covalentes saturados resisten el ataque químico |
| Fragilidad | La falta de planos de deslizamiento en la red rígida provoca fracturas |
| Politipos (ej. 4H-SiC) | Diferentes secuencias de apilamiento de capas atómicas permiten aplicaciones avanzadas de semiconductores |
¿Listo para aprovechar las excepcionales propiedades del carburo de silicio en su laboratorio?
En KINTEK, nos especializamos en equipos y consumibles de laboratorio de alto rendimiento construidos para prosperar en entornos exigentes. Ya sea que su aplicación requiera una resistencia extrema al desgaste, estabilidad a altas temperaturas o capacidades avanzadas de semiconductores, nuestra experiencia en ciencia de materiales puede ayudarlo a lograr resultados superiores.
Contacte a nuestros expertos hoy para discutir cómo nuestras soluciones de carburo de silicio pueden mejorar la eficiencia y las capacidades de su laboratorio.
Guía Visual
Productos relacionados
- Compuesto cerámico de nitruro de boro conductor BN para aplicaciones avanzadas
- Tela de carbono conductora, papel de carbono y fieltro de carbono para electrodos y baterías
- Bola de cerámica de circonio mecanizada de precisión para cerámica fina avanzada de ingeniería
- Materiales de Diamante Dopado con Boro por CVD de Laboratorio
- Máquina tamizadora vibratoria de laboratorio para tamizado tridimensional en seco y húmedo
La gente también pregunta
- ¿Cuánto tiempo se tarda en soldar? Una guía sobre el tiempo y la técnica para juntas perfectas
- ¿Cuáles son las fortalezas del braseado? Lograr una unión metálica fuerte, limpia y precisa
- ¿Cuáles son las 4 desventajas de la soldadura fuerte? Comprender las limitaciones críticas de este método de unión
- ¿Cuáles son las desventajas de la soldadura fuerte? Comprender las limitaciones y compensaciones clave.
- ¿Qué es mejor, soldadura blanda o soldadura fuerte? Elija el método de unión de metales adecuado para su proyecto



















