En muchos entornos de laboratorio, los materiales de ánodo más comúnmente utilizados son el platino, el oro y el carbono (a menudo como grafito o carbono vítreo). Estos materiales se eligen por su inercia química y conductividad eléctrica, lo que garantiza que faciliten una reacción sin interferir con ella. Sin embargo, esto es solo una parte de un panorama mucho más amplio.
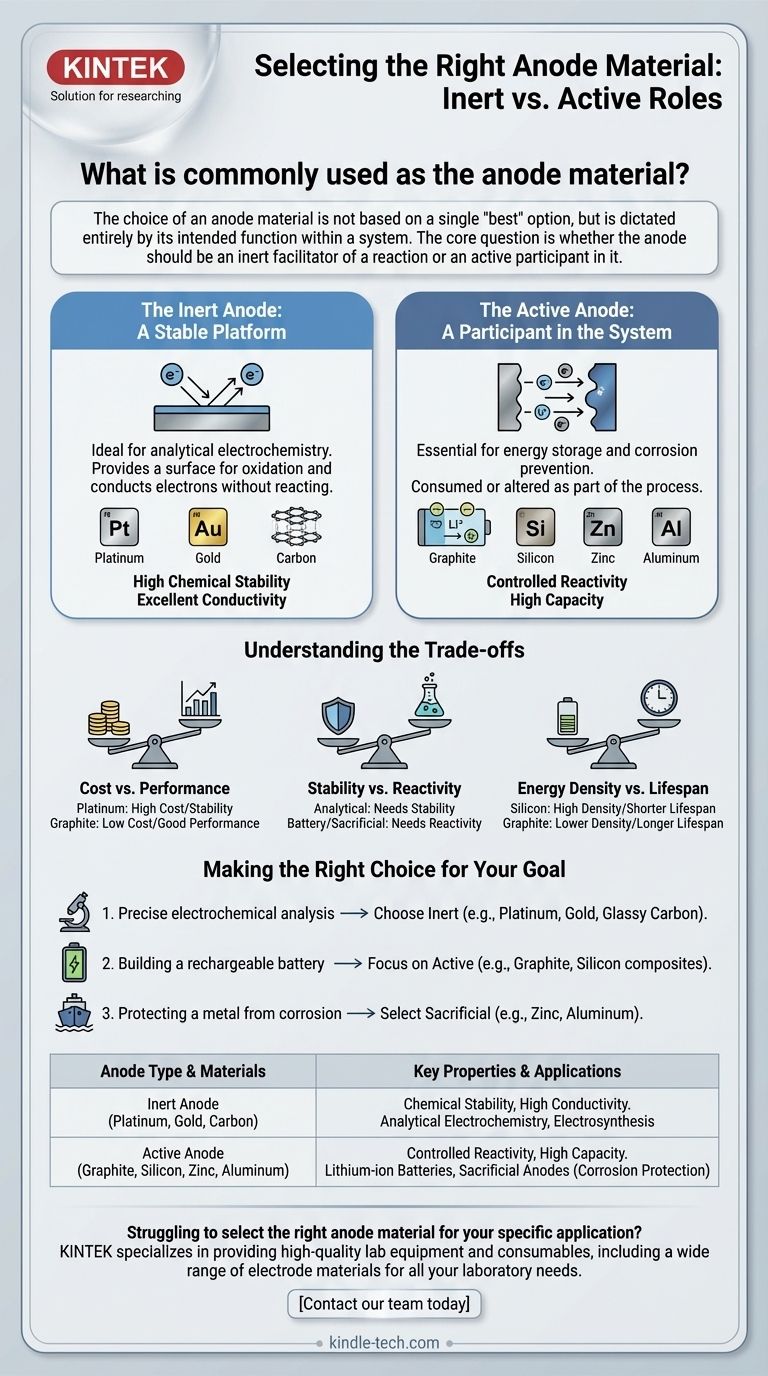
La elección de un material de ánodo no se basa en una única opción "mejor", sino que está dictada enteramente por su función prevista dentro de un sistema. La pregunta central es si el ánodo debe ser un facilitador inerte de una reacción o un participante activo en ella.

Los dos roles fundamentales de un ánodo
El término "ánodo" simplemente se refiere al electrodo donde ocurre la oxidación (la pérdida de electrones). El material ideal para este rol cambia drásticamente dependiendo del objetivo de la aplicación. Podemos separar estas aplicaciones en dos categorías principales: aquellas que requieren un ánodo inerte y aquellas que requieren uno activo.
El ánodo inerte: una plataforma estable
En aplicaciones como la electroquímica analítica, un ánodo inerte es esencial. Su única función es proporcionar una superficie para que ocurra la oxidación y conducir los electrones fuera del sistema.
El material en sí no debe cambiar ni reaccionar. Esto asegura que las mediciones tomadas reflejen la química de la solución, no la degradación del electrodo.
Es por eso que materiales como el platino, el oro y el carbono son opciones estándar. Poseen las propiedades críticas de alta conductividad y estabilidad química excepcional en una amplia gama de condiciones.
El ánodo activo: un participante en el sistema
En muchas otras tecnologías críticas, el ánodo está diseñado para ser un participante activo y esencial en el proceso químico. Aquí, el material se consume o se altera como parte de la función del sistema.
Esto es más común en el almacenamiento de energía y la prevención de la corrosión. El material se elige específicamente por sus propiedades reactivas.
Un excelente ejemplo es una batería de iones de litio, donde el ánodo suele ser grafito. La función del grafito es absorber y liberar iones de litio durante la carga y descarga. Su reactividad química es su característica principal.
Otro ejemplo clave es la prevención de la corrosión, donde un ánodo de sacrificio hecho de zinc, aluminio o magnesio se une a una estructura de acero como el casco de un barco. El zinc más reactivo se corroe (oxida) primero, sacrificándose para proteger el acero.
Comprender las compensaciones
La selección de un material de ánodo siempre implica equilibrar factores contrapuestos. No existe un único material que sea perfecto para cada situación.
Costo vs. Rendimiento
El platino ofrece una estabilidad y propiedades catalíticas excepcionales, pero es extremadamente caro. El grafito y otras formas de carbono ofrecen un excelente rendimiento para muchas aplicaciones a una fracción del costo, lo que los hace omnipresentes en productos comerciales.
Estabilidad vs. Reactividad
Esta es la compensación central. Para una medición analítica, necesita la máxima estabilidad para que el ánodo no interfiera. Para una batería o un sistema de sacrificio, necesita una reactividad precisamente controlada para que el dispositivo funcione.
Densidad de energía vs. Vida útil
En la tecnología de baterías, este es un desafío crítico. El silicio está siendo investigado intensamente como material de ánodo de próxima generación porque puede contener significativamente más iones de litio que el grafito. Sin embargo, se hincha y encoge físicamente drásticamente durante la carga y descarga, lo que puede hacer que se degrade y falle rápidamente.
Tomar la decisión correcta para su objetivo
El ánodo correcto es el que cumple el propósito específico de su sistema electroquímico. Su objetivo principal reducirá inmediatamente las opciones.
- Si su enfoque principal es el análisis electroquímico preciso: Elija un material inerte como platino, oro o carbono vítreo para asegurarse de que sus mediciones no estén influenciadas por el propio electrodo.
- Si su enfoque principal es construir una batería recargable: Céntrese en materiales activos con alta capacidad y estabilidad de ciclo, como el grafito o materiales emergentes como los compuestos de silicio.
- Si su enfoque principal es proteger un metal de la corrosión: Seleccione un material de sacrificio que sea más electroquímicamente activo que el metal que está protegiendo, como zinc o aluminio para el acero.
En última instancia, comprender el papel del ánodo, ya sea como una etapa estable o un participante activo, es clave para seleccionar el material correcto para la tarea.
Tabla resumen:
| Tipo de ánodo | Materiales comunes | Propiedades clave | Aplicaciones principales |
|---|---|---|---|
| Ánodo inerte | Platino, Oro, Carbono (Grafito, Carbono vítreo) | Estabilidad química, Alta conductividad | Electroquímica analítica, Electrosíntesis |
| Ánodo activo | Grafito, Silicio, Zinc, Aluminio | Reactividad controlada, Alta capacidad | Baterías de iones de litio, Ánodos de sacrificio (Protección contra la corrosión) |
¿Tiene dificultades para seleccionar el material de ánodo adecuado para su aplicación específica? KINTEK se especializa en proporcionar equipos y consumibles de laboratorio de alta calidad, incluida una amplia gama de materiales para electrodos para todas sus necesidades de laboratorio. Ya sea que necesite electrodos inertes para un análisis preciso o esté desarrollando tecnología de baterías de próxima generación, nuestros expertos pueden ayudarlo a encontrar la solución óptima. Contacte a nuestro equipo hoy para discutir su proyecto y mejorar las capacidades de su laboratorio.
Guía Visual
Productos relacionados
- Horno de grafito al vacío para material negativo Horno de grafiación
- Tela de carbono conductora, papel de carbono y fieltro de carbono para electrodos y baterías
- Material de pulido de electrodos para experimentos electroquímicos
- Dióxido de iridio IrO2 para electrólisis del agua
- Colector de corriente de papel de aluminio para batería de litio
La gente también pregunta
- ¿Cuáles son las ventajas de un horno de grafito? Logre precisión y pureza a altas temperaturas
- ¿Cuáles son las desventajas del horno de grafito? Limitaciones clave y costos operativos
- ¿Cuál es el uso de un horno de grafito? Logre el procesamiento a temperaturas extremas para materiales avanzados
- ¿Qué mide un horno de grafito? Una herramienta clave para el análisis de trazas y el procesamiento a alta temperatura
- ¿Cuál es la aplicación del horno de grafito? Esencial para el procesamiento y la síntesis de materiales a alta temperatura

















