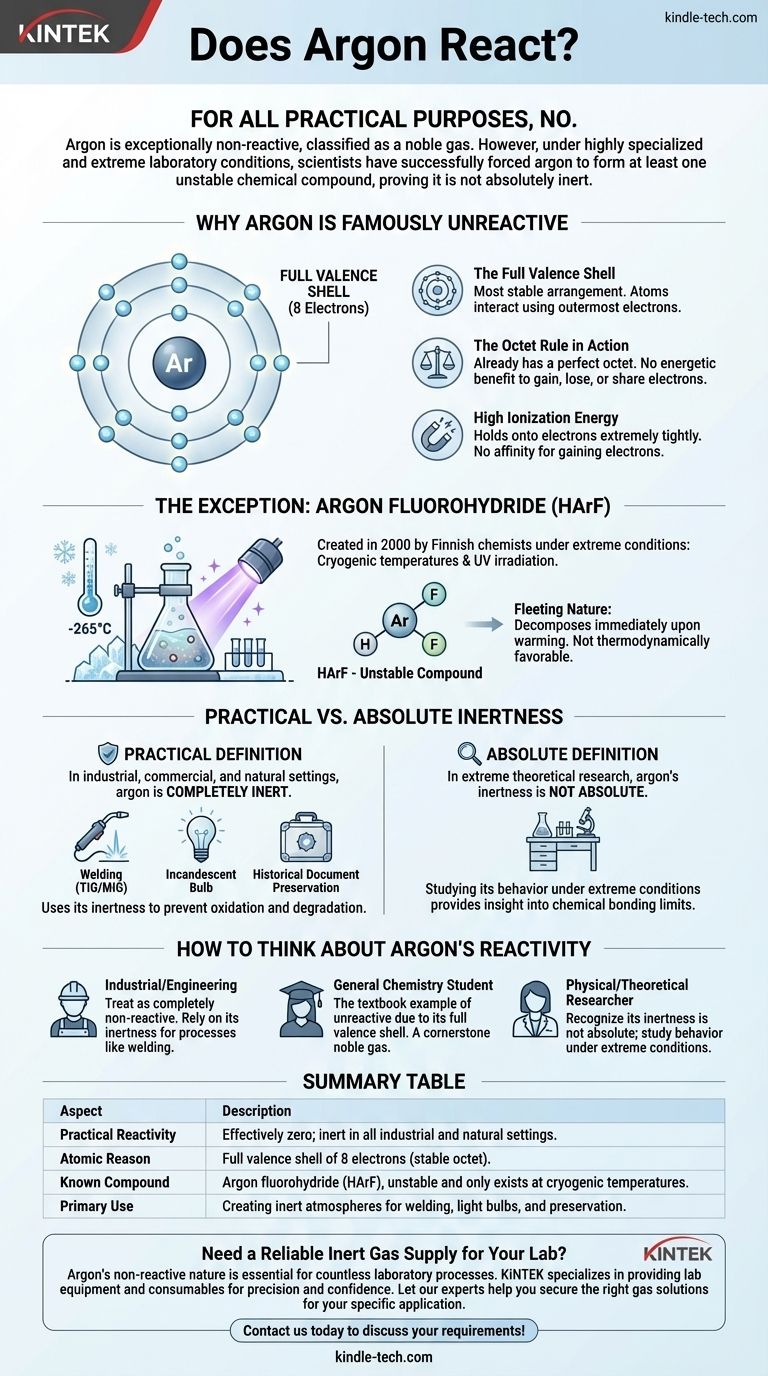
Para todos los propósitos prácticos, no. El argón es excepcionalmente no reactivo, razón por la cual se clasifica como un gas noble. Sin embargo, bajo condiciones de laboratorio altamente especializadas y extremas, los científicos han logrado forzar al argón a formar al menos un compuesto químico inestable, demostrando que no es absolutamente inerte.
La conclusión principal es que la "reactividad" de un elemento no es una simple pregunta de sí o no. Si bien la configuración perfecta de la capa de electrones del argón lo hace inerte en cualquier contexto natural o industrial, su no reactividad puede superarse con suficiente energía bajo condiciones criogénicas, revelando las sutiles complejidades del enlace químico.

Por qué el argón es famoso por ser "no reactivo"
Para entender por qué el argón se resiste tan fuertemente a formar enlaces químicos, debemos observar su estructura atómica. Su reputación de ser inerte no es arbitraria; es un resultado directo de su configuración electrónica.
La capa de valencia completa
Los átomos interactúan y forman enlaces utilizando sus electrones más externos, conocidos como electrones de valencia.
El argón tiene ocho electrones de valencia, lo que llena completamente su capa electrónica externa. Esta es la disposición más estable que puede tener un átomo.
La "regla del octeto" en acción
La "regla del octeto" es un principio fundamental en química que establece que los átomos tienden a ganar, perder o compartir electrones para lograr una capa externa completa de ocho electrones.
Dado que el argón ya tiene este octeto perfecto, no hay ningún beneficio energético para que gane, pierda o comparta electrones con otros átomos. Ya se encuentra en su estado ideal de baja energía.
Alta energía de ionización
La energía de ionización es la energía necesaria para eliminar un electrón de un átomo. El argón tiene una energía de ionización muy alta, lo que significa que retiene sus electrones con extrema fuerza.
De manera similar, no tiene afinidad por ganar electrones. Simplemente no hay un "motivo" químico para que el argón participe en una reacción en circunstancias normales.
La excepción que confirma la regla
Durante décadas, se creyó que el argón era completamente inerte. Esto cambió en el año 2000 cuando un equipo de químicos finlandeses creó el primer compuesto verdadero de argón conocido.
Forzar una reacción bajo condiciones extremas
El compuesto, fluorohidruro de argón (HArF), no se creó en un vaso de precipitados de laboratorio típico.
Los científicos tuvieron que congelar una mezcla de argón y fluoruro de hidrógeno sobre una superficie a temperaturas cercanas al cero absoluto (alrededor de -265°C o -445°F) y luego irradiarla con una potente luz ultravioleta. Esta entrada de energía extrema fue suficiente para forzar temporalmente al reacio átomo de argón a formar un enlace.
La naturaleza efímera de los compuestos de argón
El compuesto HArF resultante es increíblemente inestable. Solo existe a estas temperaturas criogénicas.
Si se calienta ligeramente, los enlaces débiles se rompen e inmediatamente se descompone de nuevo en argón y fluoruro de hidrógeno separados. Esto destaca que el compuesto no es termodinámicamente favorable y existe solo porque está "atrapado" por el frío extremo.
Inercia práctica vs. inercia absoluta
Este descubrimiento nos obliga a distinguir entre dos conceptos: lo que es cierto en un sentido práctico y lo que es cierto en un sentido absoluto y teórico.
La definición práctica de inerte
En cualquier entorno industrial, comercial o natural, el argón es completamente inerte. No reacciona con el aire, el agua, los metales ni ninguna otra sustancia con la que entre en contacto.
Es esta inercia práctica lo que lo hace tan valioso.
Por qué esto es importante para las aplicaciones
La no reactividad del argón es una característica, no una limitación. En la soldadura (TIG/MIG), crea un "escudo" inerte alrededor del metal fundido, evitando que se oxide o reaccione con los gases del aire, lo que garantiza una soldadura limpia y fuerte.
En las bombillas incandescentes, una atmósfera de argón evita que el filamento de tungsteno caliente se queme. En la conservación de documentos históricos, proporciona un ambiente libre de oxígeno para detener la degradación.
Cómo pensar sobre la reactividad del argón
Tu contexto determina cómo debes ver el comportamiento químico del argón. Comprender esta distinción es clave para aplicar correctamente los principios químicos.
- Si trabajas en un entorno industrial o de ingeniería: Trata el argón como un gas completamente no reactivo. Su inercia es su propiedad más valiosa y se puede confiar en ella para procesos como la soldadura y la fabricación.
- Si eres estudiante de química general: Comprende que el argón es el ejemplo de libro de texto de un elemento no reactivo debido a su capa de electrones de valencia completa, lo que lo convierte en una piedra angular del grupo de los gases nobles.
- Si eres investigador en química física o teórica: Reconoce que la inercia del argón no es absoluta, y estudiar su comportamiento en condiciones extremas proporciona información valiosa sobre los límites de los enlaces químicos.
En última instancia, la extrema renuencia del argón a reaccionar es una propiedad fundamental que lo hace tanto científicamente interesante como inmensamente útil en el mundo real.
Tabla resumen:
| Aspecto | Descripción |
|---|---|
| Reactividad práctica | Efectivamente cero; inerte en todos los entornos industriales y naturales. |
| Razón atómica | Capa de valencia completa de 8 electrones (octeto estable). |
| Compuesto conocido | Fluorohidruro de argón (HArF), inestable y solo existe a temperaturas criogénicas. |
| Uso principal | Creación de atmósferas inertes para soldadura, bombillas y conservación. |
¿Necesitas un suministro fiable de gas inerte para tu laboratorio?
La naturaleza no reactiva del argón es esencial para innumerables procesos de laboratorio, desde la creación de atmósferas controladas hasta la manipulación de materiales sensibles. Asegurarte de tener un suministro constante y de alta pureza es fundamental para tus resultados.
KINTEK se especializa en proporcionar el equipo de laboratorio y los consumibles que necesitas para operar con precisión y confianza. Deja que nuestros expertos te ayuden a asegurar las soluciones de gas adecuadas para tu aplicación específica.
¡Contáctanos hoy a través de nuestro formulario para discutir tus requisitos!
Guía Visual