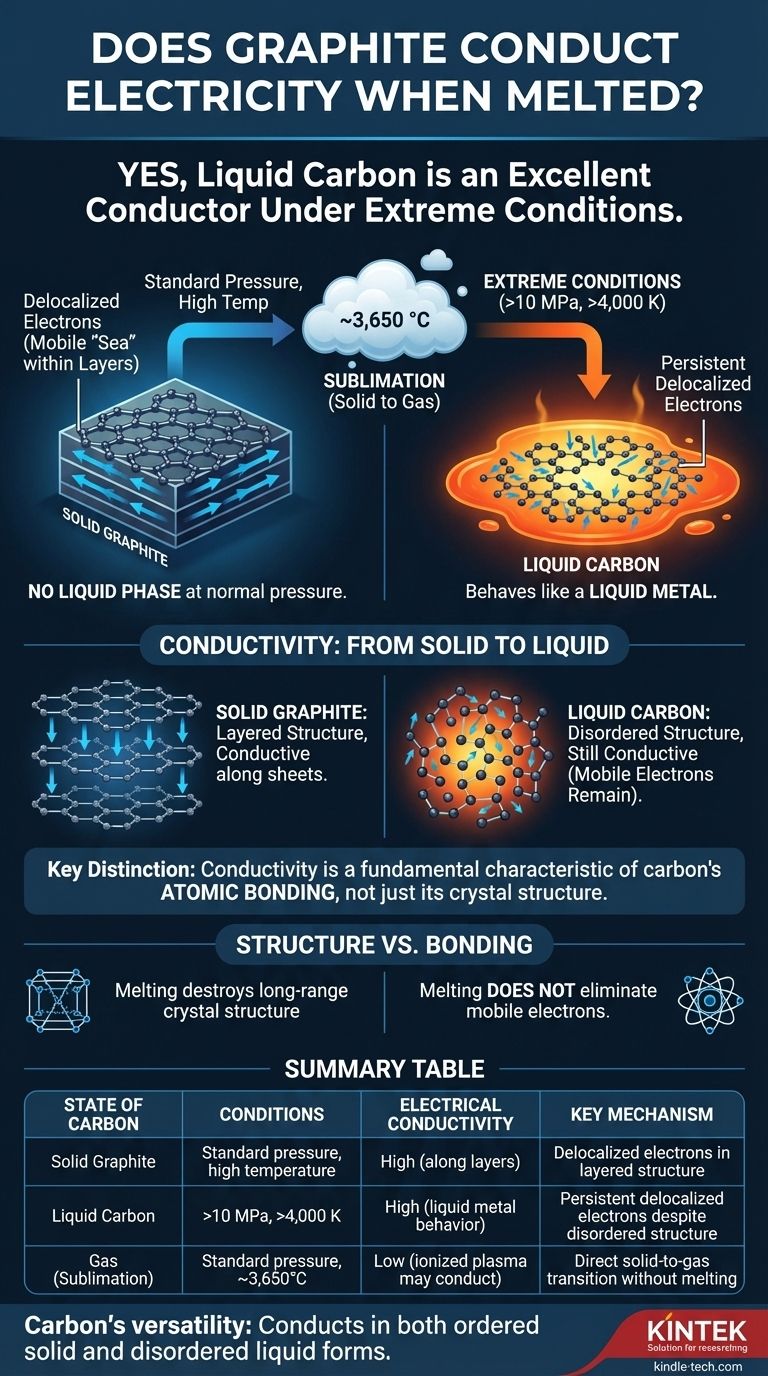
Sí, bajo las condiciones extremas requeridas para fundirlo, el carbono líquido es un excelente conductor eléctrico. Aunque el grafito no se funde bajo presión atmosférica normal, el carbono líquido que puede formarse a presiones y temperaturas muy altas se comporta como un metal líquido, con electrones libres para moverse y transportar una corriente eléctrica.
La pregunta no es simplemente si el grafito fundido conduce la electricidad —lo hace— sino por qué. La respuesta revela que la conductividad no es únicamente una propiedad de la famosa estructura en capas del grafito, sino una característica más fundamental del enlace atómico del carbono que persiste incluso en un estado líquido desordenado.

El desafío de fundir grafito
Para entender la conducción en el carbono líquido, primero debemos apreciar lo difícil que es crearlo. Para la mayoría de los propósitos prácticos, el grafito no tiene una fase líquida.
Sublimación, no fusión
A presión atmosférica estándar, cuando se calienta el grafito hasta su límite, no se convierte en líquido. En cambio, se sublima, transformándose directamente de sólido a gas a temperaturas de alrededor de 3.650 °C (6.600 °F).
La necesidad de condiciones extremas
Para forzar al carbono a un estado líquido, es necesario aplicar una presión y una temperatura inmensas simultáneamente. El carbono líquido solo existe a presiones superiores a 10 megapascales (~100 veces la presión atmosférica normal) y temperaturas que superan los 4.000 K (~3.727 °C o 6.740 °F).
Conductividad: del sólido al líquido
La razón por la que tanto el grafito sólido como el carbono líquido conducen la electricidad reside en la naturaleza única de los electrones del carbono.
Cómo conduce el grafito sólido
En el grafito sólido, los átomos de carbono están dispuestos en láminas planas y hexagonales. Cada átomo de carbono forma enlaces fuertes con tres vecinos, dejando su cuarto electrón externo deslocalizado.
Estos electrones deslocalizados no están ligados a ningún átomo individual. En cambio, forman un "mar" móvil de electrones dentro de cada lámina, razón por la cual el grafito es un excelente conductor eléctrico a lo largo de sus capas.
Conducción en estado líquido
Cuando el grafito se ve obligado a fundirse, su estructura rígida y en capas se destruye. Los átomos se desordenan y pueden moverse libremente, como en cualquier líquido.
Sin embargo, el entorno de enlace local aún permite la existencia de electrones deslocalizados. El líquido es una mezcla compleja y fluctuante de tipos de enlace, pero la presencia de electrones móviles persiste. Esto hace que el carbono líquido se comporte como un metal líquido, con alta conductividad eléctrica.
Comprendiendo la distinción clave
Es fácil asumir que la conductividad del grafito es puramente el resultado de su estructura laminar. El comportamiento del carbono líquido demuestra que esta es una imagen incompleta.
Estructura vs. Enlace
La clave es la diferencia entre estructura y enlace. Si bien la fusión destruye la estructura cristalina de largo alcance del grafito, no elimina el enlace atómico fundamental que permite que los electrones se vuelvan móviles.
Una limitación práctica
Este fenómeno es principalmente de interés en la física extrema y la ciencia de los materiales. En la mayoría de las aplicaciones de ingeniería, como en los hornos de arco eléctrico, se trata de un electrodo de grafito sólido que se sublima en un gas caliente ionizado (un plasma), no de un charco de carbono líquido.
Dando sentido a las propiedades del carbono
Su comprensión de este tema depende de su objetivo. Utilice estos puntos para enmarcar el concepto para su contexto específico.
- Si su enfoque principal es la química fundamental: La conductividad del carbono líquido demuestra que los electrones deslocalizados, una característica del enlace sp2 del carbono, no se pierden cuando la estructura reticular rígida se funde.
- Si su enfoque principal es la ingeniería práctica: Para prácticamente todas las aplicaciones, recuerde que el grafito se sublimará en un gas mucho antes de que tenga la oportunidad de fundirse, un factor crítico para el diseño de sistemas de alta temperatura.
En última instancia, la capacidad del carbono para conducir la electricidad tanto en su forma sólida ordenada como en su forma líquida desordenada revela la notable versatilidad de sus enlaces atómicos.
Tabla resumen:
| Estado del carbono | Condiciones requeridas | Conductividad eléctrica | Mecanismo clave |
|---|---|---|---|
| Grafito sólido | Presión estándar, alta temperatura | Alta (a lo largo de las capas) | Electrones deslocalizados en estructura laminar |
| Carbono líquido | >10 MPa, >4.000 K | Alta (comportamiento de metal líquido) | Electrones deslocalizados persistentes a pesar de la estructura desordenada |
| Gas (Sublimación) | Presión estándar, ~3.650°C | Baja (el plasma ionizado puede conducir) | Transición directa de sólido a gas sin fusión |
Desbloquee la precisión en la investigación de alta temperatura con KINTEK
Comprender los comportamientos extremos de los materiales, como la conductividad del carbono líquido, requiere equipos de laboratorio fiables. KINTEK se especializa en hornos de laboratorio, electrodos y consumibles de alto rendimiento diseñados para condiciones rigurosas. Ya sea que esté explorando la ciencia de los materiales o desarrollando sistemas de ingeniería avanzados, nuestros productos garantizan precisión y durabilidad.
¿Listo para mejorar las capacidades de su laboratorio? Contáctenos hoy para discutir cómo las soluciones de KINTEK pueden apoyar sus experimentos y objetivos de investigación de alta temperatura.
Guía Visual
Productos relacionados
- Horno de Grafización de Película de Alta Conductividad Térmica de Vacío de Grafito
- Electrodo Electrolítico de Grafito en Disco y Varilla de Grafito
- Horno de grafización al vacío a ultra alta temperatura de grafito
- Crisol de grafito puro de alta pureza para evaporación
- Placa de grafito de carbono fabricada por el método de prensado isostático
La gente también pregunta
- ¿Cuál es la temperatura de un horno de grafito? Alcanza un calor extremo de hasta 3000 °C
- ¿Qué gas se utiliza en el horno de grafito? Maximice la precisión con el gas inerte adecuado
- ¿Cuáles son las interferencias del horno de grafito? Supere los problemas de matriz y espectrales para una GFAAS precisa
- ¿Cuáles son las ventajas y desventajas de un horno de grafito? Desbloquee el rendimiento de calor extremo
- ¿Qué hace un horno de grafito? Logra calor extremo y análisis ultrasensible












