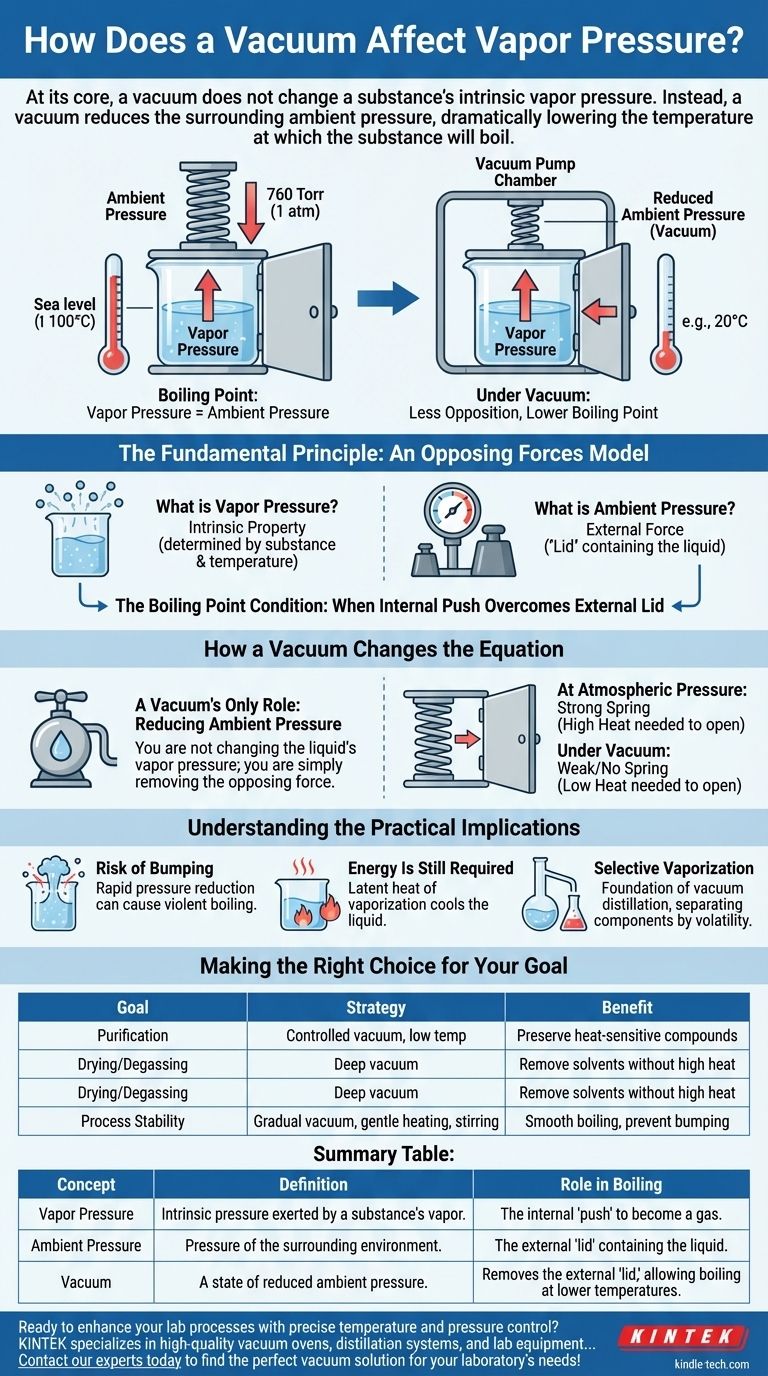
En esencia, el vacío no cambia la presión de vapor intrínseca de una sustancia. En cambio, el vacío reduce la presión ambiental circundante, lo que disminuye drásticamente la temperatura a la que la sustancia hervirá. La presión de vapor de una sustancia es una propiedad fundamental determinada únicamente por la sustancia misma y su temperatura.
La ebullición ocurre cuando la presión de vapor interna de un líquido iguala o excede la presión externa que lo empuja hacia abajo. Un vacío simplemente elimina esa presión externa, lo que facilita mucho que la presión de vapor del líquido "gane" e inicie la ebullición, incluso a temperaturas mucho más bajas.
El Principio Fundamental: Un Modelo de Fuerzas Opuestas
Para comprender el papel del vacío, primero debe distinguir entre dos conceptos clave: el "empuje" interno del líquido y el "empuje" externo del entorno.
¿Qué es la Presión de Vapor?
La presión de vapor es la presión ejercida por el vapor de una sustancia cuando está en equilibrio con su fase líquida o sólida. Piense en ello como la tendencia inherente de la sustancia a escapar y convertirse en gas.
Esta propiedad es intrínseca al material y es principalmente una función de la temperatura. A medida que se añade calor, las moléculas se mueven más rápido y más de ellas tienen suficiente energía para escapar de la superficie del líquido, aumentando la presión de vapor.
¿Qué es la Presión Ambiental?
La presión ambiental es la presión del entorno circundante que empuja hacia abajo sobre la superficie de la sustancia. A nivel del mar, este es el peso de la atmósfera sobre nosotros (aproximadamente 760 Torr o 1 atm).
Esta fuerza externa actúa como una "tapa", conteniendo el líquido y dificultando que las moléculas escapen.
La Condición del Punto de Ebullición
Un líquido hierve cuando su empuje interno supera la tapa externa. La definición técnica del punto de ebullición es la temperatura a la que la presión de vapor iguala la presión ambiental. Esta es la relación crítica a comprender.
Cómo un Vacío Cambia la Ecuación
Un sistema de vacío no interactúa con las moléculas del líquido para cambiar sus propiedades inherentes. Su único trabajo es cambiar el entorno externo.
El Único Papel del Vacío: Reducir la Presión Ambiental
Una bomba de vacío funciona eliminando moléculas de gas (como el aire) de una cámara sellada. Al eliminar estas moléculas, reduce drásticamente la presión ambiental que empuja hacia abajo sobre el líquido en el interior.
Usted no está cambiando la presión de vapor del líquido; simplemente está eliminando la fuerza opuesta.
Alcanzando el Punto de Ebullición Más Rápido
Imagine intentar abrir una puerta con resorte. La presión de vapor es la fuerza que aplica a la puerta, y la presión ambiental es la fuerza del resorte que empuja hacia atrás.
- A Presión Atmosférica: El resorte es fuerte. Necesita empujar muy fuerte (añadir mucho calor) para abrir la puerta (hacer que el líquido hierva).
- Bajo Vacío: Ha quitado el resorte. Ahora, incluso un empujón suave (una pequeña cantidad de calor) es suficiente para abrir la puerta fácilmente.
La naturaleza de la puerta no cambió, solo la oposición. Por eso el agua, que hierve a 100°C (212°F) a nivel del mar, puede hervir a temperatura ambiente bajo un vacío suficiente.
Comprendiendo las Implicaciones Prácticas
Aplicar un vacío es una técnica poderosa, pero conlleva comportamientos y limitaciones específicos que debe gestionar.
Riesgo de "Golpeo"
Si la presión se reduce demasiado rápido, el líquido puede sobrecalentarse. La energía se acumula sin hervir hasta que estalla en un evento único y violento conocido como golpeo. Por eso, la aplicación gradual y controlada del vacío y la agitación son críticas en entornos de laboratorio e industriales.
Todavía se Requiere Energía
Incluso bajo un vacío perfecto, la ebullición no es instantánea ni "gratuita". El cambio de fase de líquido a gas (evaporación) todavía requiere energía, conocida como calor latente de vaporización. Si no hay una fuente de calor externa, el líquido extraerá esta energía de sí mismo, lo que provocará una rápida caída de su temperatura. Este es el principio detrás de la liofilización.
Vaporización Selectiva
Todo este principio es la base de la destilación al vacío. Dos líquidos con diferentes puntos de ebullición pueden separarse a una baja temperatura que evita que se degraden. La sustancia más volátil (con la presión de vapor intrínseca más alta) hervirá primero bajo vacío, dejando atrás la sustancia menos volátil.
Tomando la Decisión Correcta para Su Objetivo
Comprender esta relación le permite controlar los procesos con precisión. Su estrategia dependerá de lo que intente lograr.
- Si su enfoque principal es la purificación: Utilice un vacío controlado para separar componentes volátiles de una mezcla a bajas temperaturas, preservando compuestos sensibles al calor.
- Si su enfoque principal es el secado o la desgasificación: Aplique un vacío profundo para eliminar disolventes residuales como agua o aire de una muestra sin tener que hornearla a altas temperaturas.
- Si su enfoque principal es la estabilidad del proceso: Combine un vacío gradual con calentamiento suave y agitación para lograr una ebullición suave y evitar golpes violentos.
Al dominar la interacción entre la temperatura y la presión, obtiene un control preciso sobre el estado físico de sus materiales.

Tabla Resumen:
| Concepto | Definición | Función en la Ebullición |
|---|---|---|
| Presión de Vapor | Presión intrínseca ejercida por el vapor de una sustancia. | El 'empuje' interno del líquido para convertirse en gas. |
| Presión Ambiental | Presión del entorno circundante (ej., atmósfera). | La 'tapa' externa que contiene el líquido. |
| Vacío | Un estado de presión ambiental reducida. | Elimina la 'tapa' externa, permitiendo la ebullición a temperaturas más bajas. |
¿Listo para mejorar los procesos de su laboratorio con un control preciso de la temperatura y la presión?
KINTEK se especializa en hornos de vacío de alta calidad, sistemas de destilación y equipos de laboratorio diseñados para una ebullición, secado y purificación eficientes a baja temperatura. Nuestras soluciones le ayudan a preservar materiales sensibles al calor y a mejorar la estabilidad del proceso.
¡Contacte hoy a nuestros expertos para encontrar la solución de vacío perfecta para las necesidades de su laboratorio!
Guía Visual