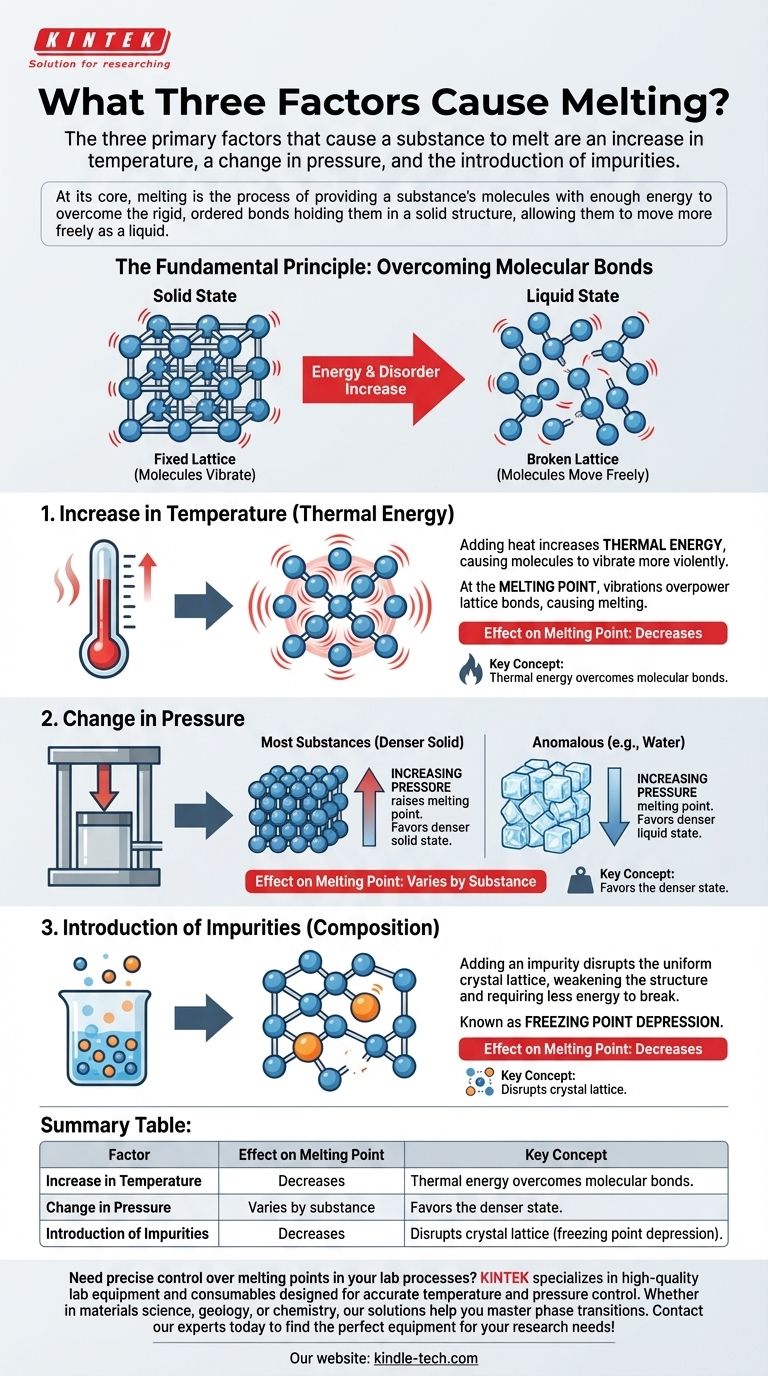
Los tres factores principales que causan la fusión de una sustancia son un aumento de temperatura, un cambio de presión y la introducción de impurezas. Si bien la temperatura es el factor más intuitivo, la presión y la composición desempeñan roles igualmente críticos para determinar las condiciones precisas bajo las cuales un sólido pasará a estado líquido.
En esencia, la fusión es el proceso de proporcionar a las moléculas de una sustancia suficiente energía para superar los enlaces rígidos y ordenados que las mantienen en una estructura sólida, permitiéndoles moverse más libremente como un líquido.

El Principio Fundamental: Superar los Enlaces Moleculares
Antes de examinar los factores, es crucial entender qué es la fusión a nivel microscópico. Representa un cambio fundamental en el estado físico de una sustancia, conocido como transición de fase.
El Estado Sólido
En un sólido, los átomos y las moléculas están encerrados en una estructura fija, a menudo cristalina, llamada red. Vibran en su lugar pero carecen de la energía para liberarse de sus vecinos. Esto es lo que le da a un sólido su forma y volumen definidos.
El Estado Líquido
En un líquido, las moléculas han absorbido suficiente energía para salir de esa red rígida. Ahora pueden deslizarse unas sobre otras, razón por la cual un líquido fluye y toma la forma de su recipiente, aunque mantiene un volumen relativamente constante.
Los Tres Factores Clave de la Fusión
Cada uno de los tres factores proporciona un mecanismo diferente para alterar la red sólida y permitir la transición a un líquido.
1. Aumento de Temperatura (Energía Térmica)
Esta es la causa más común de fusión. Añadir calor a una sustancia aumenta su energía térmica.
Esta energía adicional se traduce directamente en un aumento de la energía cinética de las moléculas, lo que hace que vibren cada vez con más violencia. A una temperatura específica, el punto de fusión, estas vibraciones se vuelven tan intensas que superan los enlaces que mantienen unida la red, y la sustancia se funde.
2. Cambio de Presión
El efecto de la presión sobre la fusión es menos intuitivo porque depende de la sustancia. Actúa favoreciendo el estado de la materia más denso.
Para la mayoría de las sustancias, la forma sólida es más densa que la forma líquida. El aumento de la presión fuerza a las moléculas a acercarse, reforzando la red sólida y haciendo que sea más difícil fundirse. Esto significa que un aumento de la presión eleva el punto de fusión.
Sin embargo, para sustancias anómalas como el agua, la forma sólida (hielo) es menos densa que la forma líquida. Aquí, un aumento de la presión favorece el estado líquido más denso, lo que efectivamente reduce el punto de fusión. Por eso la cuchilla de un patinador sobre hielo puede derretir el hielo directamente debajo de ella.
3. Introducción de Impurezas (Composición)
Añadir una sustancia diferente, o una impureza, a un sólido puro puede reducir significativamente su punto de fusión. Este fenómeno se conoce como descenso crioscópico.
Las moléculas extrañas de la impureza alteran la formación de la red cristalina uniforme. Esta estructura debilitada requiere menos energía para romperse. Un ejemplo común es echar sal en carreteras heladas; la sal se mezcla con el hielo, reduciendo su punto de fusión y haciendo que se derrita incluso cuando la temperatura ambiente está por debajo del punto de congelación normal del agua de 0°C (32°F).
Comprendiendo la Interacción de los Factores
Estos tres factores no operan de forma aislada. El estado de una sustancia (sólido, líquido o gas) está determinado por la combinación precisa de temperatura, presión y composición.
Diagramas de Fase
Los científicos utilizan gráficos llamados diagramas de fase para mapear el estado de una sustancia bajo diferentes condiciones de temperatura y presión. Estos diagramas muestran claramente cómo el cambio de una variable puede alterar el punto de fusión.
Un Efecto Combinado
En muchos escenarios del mundo real, múltiples factores están en juego. Por ejemplo, la fusión de rocas para formar magma en las profundidades de la Tierra es el resultado complejo de un calor inmenso, presiones extremas y la presencia de varios minerales y agua (impurezas).
Aplicando Estos Principios
Comprender estos factores le permite predecir y explicar fenómenos físicos en diferentes contextos.
- Si su enfoque principal son los fenómenos cotidianos: La temperatura y la adición de impurezas son los factores más relevantes para cosas como derretir hielo o hacer helado.
- Si su enfoque principal es la geología o la ciencia planetaria: La interacción entre la inmensa presión y la alta temperatura es crítica para comprender procesos como la formación de magma o la composición de los núcleos planetarios.
- Si su enfoque principal es la ciencia de los materiales: La composición es clave, ya que la creación de aleaciones con puntos de fusión específicos es fundamental para la ingeniería y la metalurgia.
En última instancia, la transición de un sólido a un líquido es un proceso universal gobernado por la batalla constante entre los enlaces moleculares y la energía.
Tabla Resumen:
| Factor | Efecto en el Punto de Fusión | Concepto Clave |
|---|---|---|
| Aumento de Temperatura | Disminuye | La energía térmica supera los enlaces moleculares. |
| Cambio de Presión | Varía según la sustancia | Favorece el estado más denso (aumenta o disminuye el punto de fusión). |
| Introducción de Impurezas | Disminuye | Altera la red cristalina (descenso crioscópico). |
¿Necesita un control preciso sobre los puntos de fusión en sus procesos de laboratorio? KINTEK se especializa en equipos y consumibles de laboratorio de alta calidad diseñados para un control preciso de la temperatura y la presión. Ya sea que se encuentre en la ciencia de los materiales, la geología o la química, nuestras soluciones le ayudan a dominar las transiciones de fase. ¡Contacte a nuestros expertos hoy mismo para encontrar el equipo perfecto para sus necesidades de investigación!
Guía Visual