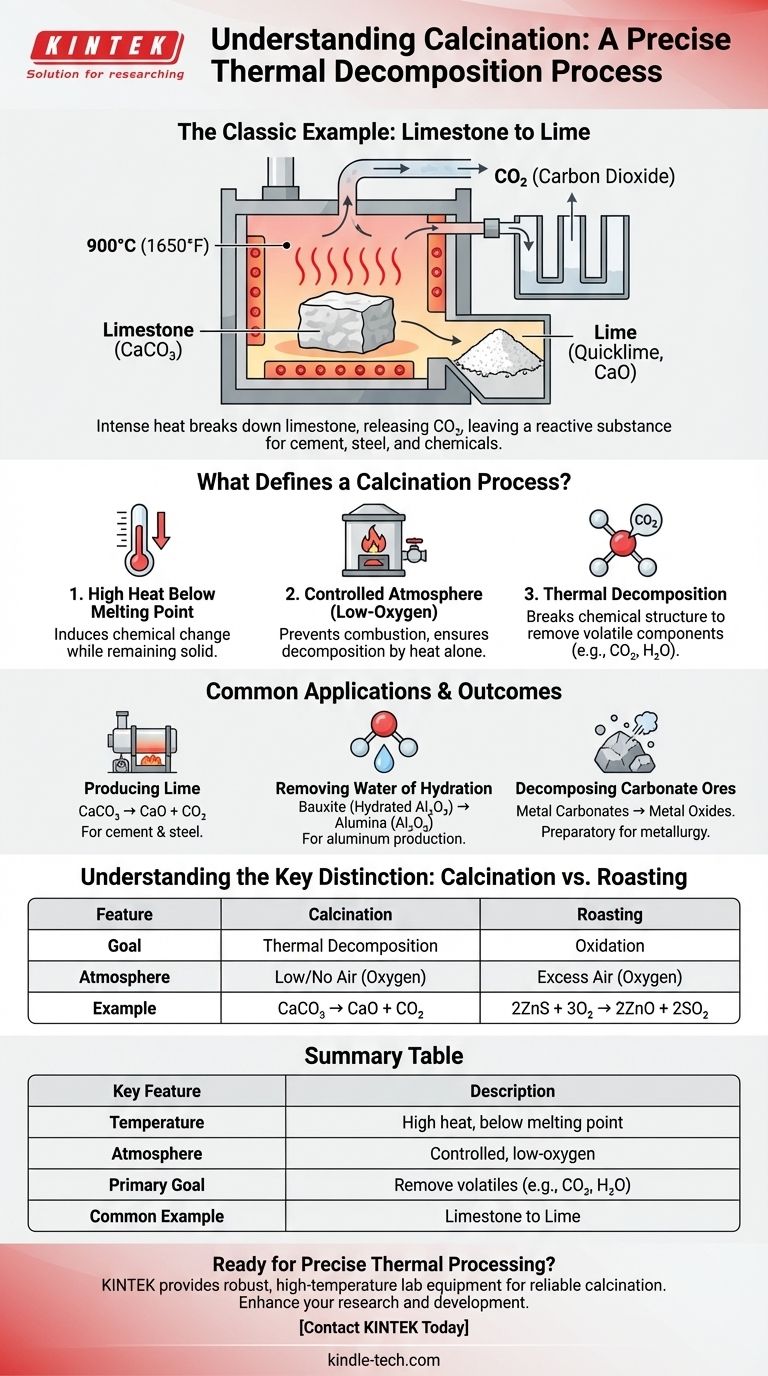
El ejemplo clásico de calcinación es el calentamiento de piedra caliza (carbonato de calcio) para producir cal (óxido de calcio). En este proceso, el calor intenso descompone la piedra caliza, haciendo que libere dióxido de carbono gaseoso y dejando una sustancia pulverulenta más reactiva. Este es un proceso fundamental utilizado durante siglos en la producción de cemento y otros materiales industriales.
La calcinación no es simplemente calentar; es un proceso preciso de descomposición térmica. Utiliza altas temperaturas por debajo del punto de fusión del material en una atmósfera controlada y con bajo contenido de oxígeno para eliminar componentes volátiles como el dióxido de carbono o el agua.

¿Qué define un proceso de calcinación?
Para identificar verdaderamente la calcinación, debe ir más allá de la simple aplicación de calor. Tres condiciones específicas definen el proceso y lo separan de otros tratamientos térmicos como el tostado o el secado.
El papel del calor intenso
La calcinación implica calentar un material sólido a una temperatura muy alta. Críticamente, esta temperatura se mantiene por debajo del punto de fusión del material.
El objetivo es inducir un cambio químico o descomposición mientras el material permanece en su estado sólido, a menudo volviéndolo quebradizo o poroso.
Una atmósfera controlada
El proceso se lleva a cabo en ausencia o con un suministro muy limitado de aire (oxígeno). Este es un diferenciador clave de otros procesos térmicos.
Al restringir el oxígeno, la calcinación previene la combustión o una oxidación significativa. El objetivo principal es la descomposición impulsada únicamente por el calor, no por la reacción con el aire.
El objetivo: descomposición térmica
El propósito fundamental de la calcinación es descomponer la estructura química de una sustancia.
Esta descomposición resulta en la eliminación de un componente volátil del sólido. La parte que se desprende es típicamente un gas, como el dióxido de carbono (CO2) de los carbonatos o el vapor de agua (H2O) de los minerales hidratados.
Aplicaciones y resultados comunes
Si bien la producción de cal es el caso de estudio, la calcinación se utiliza en varias industrias para transformar materiales.
Producción de cal a partir de piedra caliza
Este es el ejemplo más común. La piedra caliza (CaCO₃) se calienta a temperaturas alrededor de 900 °C (1650 °F). Se descompone en cal viva (CaO) y libera dióxido de carbono gaseoso.
Esta cal es un ingrediente crucial en la fabricación de cemento, acero y ciertos productos químicos.
Eliminación del agua de hidratación
La calcinación se utiliza ampliamente para eliminar el agua químicamente ligada de los minerales hidratados.
Por ejemplo, el mineral de bauxita, una forma hidratada de óxido de aluminio, se calcina para eliminar el agua y producir alúmina pura (Al₂O₃), la principal materia prima para la producción de aluminio metálico.
Descomposición de minerales de carbonato
Similar a la piedra caliza, otros minerales de carbonato metálico se calcinan para convertirlos en sus formas de óxido.
Este es a menudo un paso preparatorio en la metalurgia, ya que los óxidos metálicos son generalmente más fáciles de reducir a metal puro que sus formas de carbonato originales.
Comprendiendo las distinciones clave
Un punto común de confusión es diferenciar la calcinación de un proceso similar llamado tostado. La distinción es crítica y reside enteramente en el objetivo y la atmósfera utilizada.
Calcinación vs. Tostado
La calcinación busca la descomposición térmica en ausencia de aire. Piense en ello como "cocer" un mineral para descomponerlo. Un ejemplo es CaCO₃ → CaO + CO₂.
El tostado, en contraste, es calentar un mineral en un exceso de aire (oxígeno). El objetivo es la oxidación, a menudo para convertir minerales de sulfuro en óxidos. Un ejemplo es 2ZnS + 3O₂ → 2ZnO + 2SO₂.
¿Por qué controlar la atmósfera?
Limitar el aire durante la calcinación es esencial para prevenir reacciones secundarias no deseadas. Si hubiera oxígeno presente al calentar piedra caliza, por ejemplo, no cambiaría fundamentalmente la reacción principal, pero para otros materiales, podría conducir a una oxidación indeseable.
Controlar la atmósfera asegura que la descomposición térmica sea la transformación dominante e intencionada.
Cómo identificar un proceso de calcinación
Basándose en estos principios, puede identificar fácilmente si un proceso es un ejemplo de calcinación.
- Si su objetivo es descomponer un mineral de carbonato: Calentar piedra caliza, dolomita u otros carbonatos para eliminar CO₂ y formar un óxido es un ejemplo definitivo de calcinación.
- Si su objetivo es eliminar agua químicamente ligada: Calentar un mineral hidratado como bauxita o yeso para producir su forma anhidra (libre de agua) es otra aplicación principal de la calcinación.
- Si la distinción clave es la atmósfera: Un proceso que implica calentar un sólido por debajo de su punto de fusión con poco o ningún aire para causar una descomposición química es calcinación.
Reconocer estas condiciones le permite distinguir la calcinación como una herramienta fundamental de la ingeniería química y de materiales.
Tabla resumen:
| Característica clave | Descripción |
|---|---|
| Temperatura | Calor intenso, pero por debajo del punto de fusión del material. |
| Atmósfera | Controlada, con bajo o nulo contenido de oxígeno. |
| Objetivo principal | Descomposición térmica para eliminar componentes volátiles (p. ej., CO₂, H₂O). |
| Ejemplo común | Calentamiento de piedra caliza (CaCO₃) para producir cal (CaO). |
¿Listo para lograr un procesamiento térmico preciso en su laboratorio?
La calcinación es un proceso fundamental para transformar materiales, desde la descomposición de carbonatos hasta la deshidratación de minerales. KINTEK se especializa en proporcionar el equipo de laboratorio robusto y de alta temperatura, como hornos avanzados con control preciso de la atmósfera, que necesita para ejecutar estos procesos de manera confiable y segura.
Ya sea que trabaje en ciencia de materiales, metalurgia o ingeniería química, nuestras soluciones están diseñadas para satisfacer las rigurosas demandas de su investigación y desarrollo. Permítanos ayudarle a mejorar las capacidades de su laboratorio.
Contacte a KINTEK hoy mismo para discutir sus necesidades específicas de procesamiento térmico y descubrir el equipo adecuado para su aplicación.
Guía Visual
Productos relacionados
- Horno Rotatorio Eléctrico de Trabajo Continuo, Pequeña Planta de Pirólisis con Calefacción de Horno Rotatorio
- Planta de Horno de Pirólisis de Horno Rotatorio Eléctrico Máquina Calcinadora Horno Rotatorio Pequeño Horno Giratorio
La gente también pregunta
- ¿Cuáles son las características de los modos de movimiento de lecho de deslizamiento, colapso y rodadura? Optimice su proceso rotatorio
- ¿A qué temperatura ocurre la pirólisis? Una guía para controlar la producción de su producto
- ¿Cuáles son los principios de un horno rotatorio? Domina la mecánica del procesamiento a alta temperatura
- ¿Cuál es la temperatura de un horno rotatorio? Depende de su material y objetivo de proceso
- ¿Por qué hay cadenas dentro de un horno rotatorio? Aumente la eficiencia y el control con el intercambio de calor interno

