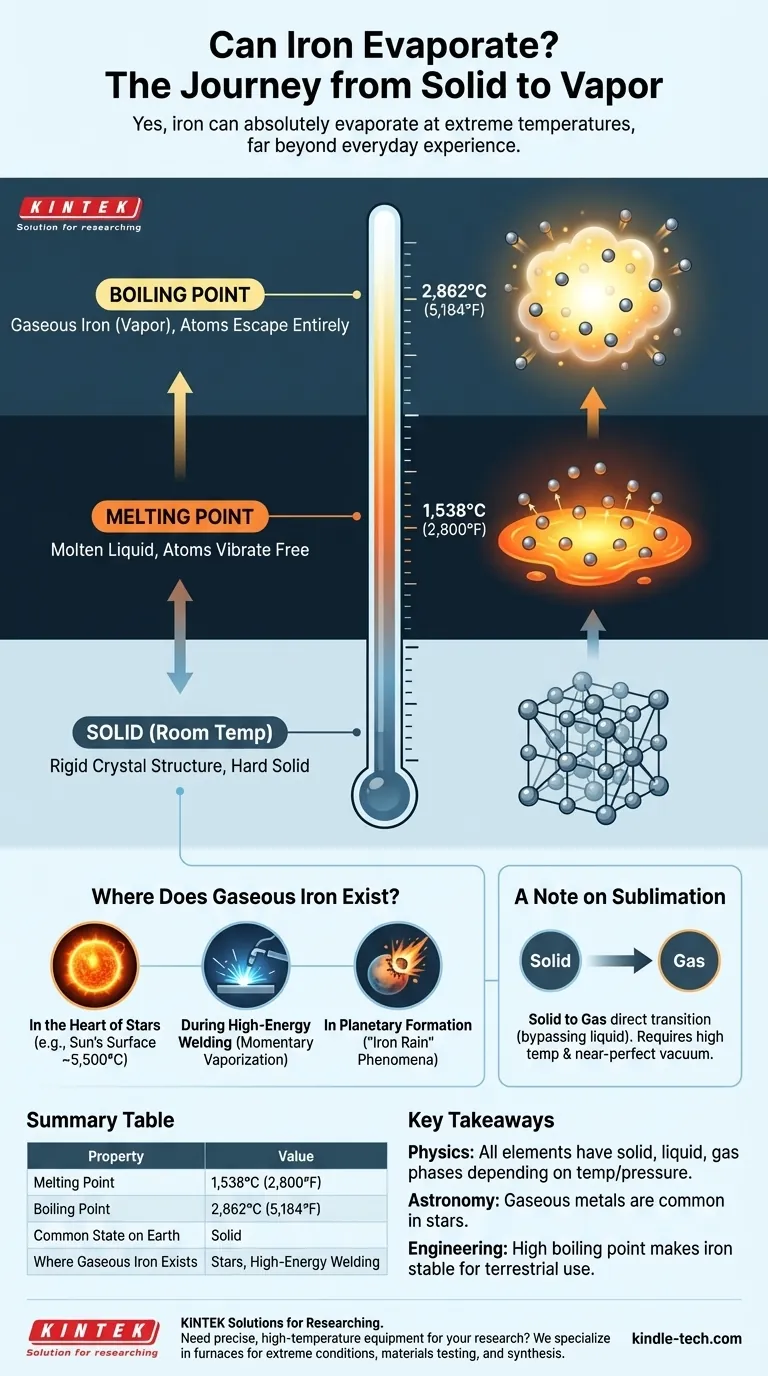
Sí, el hierro puede evaporarse absolutamente. Como prácticamente toda la materia, el hierro puede existir como sólido, líquido y gas. Sin embargo, las condiciones requeridas para convertir el hierro sólido en gas, o vapor, implican temperaturas tan extremas que están muy lejos del ámbito de la experiencia humana cotidiana.
El principio fundamental es que cualquier elemento hará la transición a gas si se calienta hasta su punto de ebullición. Para el hierro, esta temperatura es increíblemente alta, 2,862°C (5,184°F), razón por la cual lo percibimos como un material permanentemente sólido bajo todas las condiciones normales.

Comprendiendo el viaje al vapor de hierro
Para entender cómo se evapora el hierro, es mejor pensar en el mismo proceso por el que pasa el agua, pero a una escala de temperatura mucho más alta. El estado de cualquier materia —sólido, líquido o gas— está determinado por la energía y el movimiento de sus átomos.
Primer paso: De sólido a líquido
Antes de que el hierro pueda hervir, primero debe fundirse. A temperatura ambiente, los átomos de hierro están encerrados en una estructura cristalina rígida, que es lo que lo convierte en un sólido duro.
A medida que se añade un calor inmenso, los átomos vibran cada vez más violentamente hasta que se liberan de esta estructura. Esto ocurre en el punto de fusión del hierro de 1,538°C (2,800°F), convirtiéndolo en un líquido fundido.
Segundo paso: De líquido a gas
Para evaporarse, o hervir, los átomos de hierro necesitan aún más energía para superar por completo las fuerzas que los mantienen unidos como un líquido.
Cuando la temperatura alcanza el punto de ebullición del hierro de 2,862°C (5,184°F), los átomos escapan por completo, formando una nube sobrecalentada de átomos de hierro individuales. Esto es vapor de hierro, o hierro gaseoso.
¿Dónde existe realmente el hierro gaseoso?
Aunque nunca verá un charco de hierro evaporándose en un día caluroso, este proceso es común en ciertos entornos extremos del universo y en aplicaciones industriales especializadas.
En el corazón de las estrellas
El lugar más común para encontrar hierro gaseoso es dentro de las estrellas, incluido nuestro Sol. La superficie del Sol está a unos 5,500°C (9,940°F), muy por encima del punto de ebullición del hierro. Aquí, el hierro existe como un componente del plasma solar.
Durante la soldadura de alta energía
A una escala mucho menor y más controlada, el calor intenso de un arco de soldadura industrial puede vaporizar momentáneamente una pequeña cantidad del metal que se está soldando. Este vapor de hierro se enfría y se vuelve a solidificar inmediatamente como parte de la soldadura.
En la formación planetaria
Durante la formación de nuestro sistema solar, los impactos masivos entre cuerpos celestes habrían generado suficiente energía para vaporizar roca y hierro. Esto podría haber llevado a fenómenos como la "lluvia de hierro" en protoplanetas a medida que el vapor se enfriaba y condensaba.
Una nota sobre la sublimación
Existe otra vía hacia el estado gaseoso llamada sublimación, donde un material pasa directamente de sólido a gas, omitiendo por completo la fase líquida. Esto es lo que hace el hielo seco (dióxido de carbono sólido) a temperatura ambiente.
Teóricamente, el hierro también puede sublimarse. Sin embargo, esto requeriría una combinación de temperaturas muy altas y una presión extremadamente baja (un vacío casi perfecto). Bajo cualquier presión atmosférica normal, la tasa de sublimación del hierro es prácticamente cero.
Conclusiones clave para comprender la materia
- Si su enfoque principal es la física básica: Recuerde que todos los elementos pueden existir en fases sólida, líquida y gaseosa; es solo cuestión de alcanzar la temperatura y presión adecuadas.
- Si le interesa la astronomía: Reconozca que los metales gaseosos, incluido el hierro, son un componente común e importante de las estrellas y desempeñan un papel clave en los eventos cósmicos.
- Si está pensando en ingeniería: Aprecie que el punto de ebullición increíblemente alto del hierro es la propiedad fundamental que lo convierte en un material estable y confiable para casi todas las aplicaciones terrestres.
En última instancia, saber que incluso algo tan fuerte como el hierro puede convertirse en gas refuerza las leyes físicas universales que gobiernan toda la materia.
Tabla resumen:
| Propiedad | Valor |
|---|---|
| Punto de fusión | 1,538°C (2,800°F) |
| Punto de ebullición | 2,862°C (5,184°F) |
| Estado común en la Tierra | Sólido |
| Dónde existe el hierro gaseoso | Estrellas, soldadura de alta energía |
¿Necesita equipos de alta temperatura precisos para su investigación o procesos industriales? KINTEK se especializa en equipos y consumibles de laboratorio, incluidos hornos que pueden manejar condiciones extremas para pruebas y síntesis de materiales. Ya sea que esté estudiando transiciones de fase o desarrollando nuevas aleaciones, nuestras soluciones confiables lo ayudan a lograr resultados precisos y repetibles. Contacte a nuestros expertos hoy para discutir cómo podemos apoyar las necesidades de alta temperatura de su laboratorio.
Guía Visual