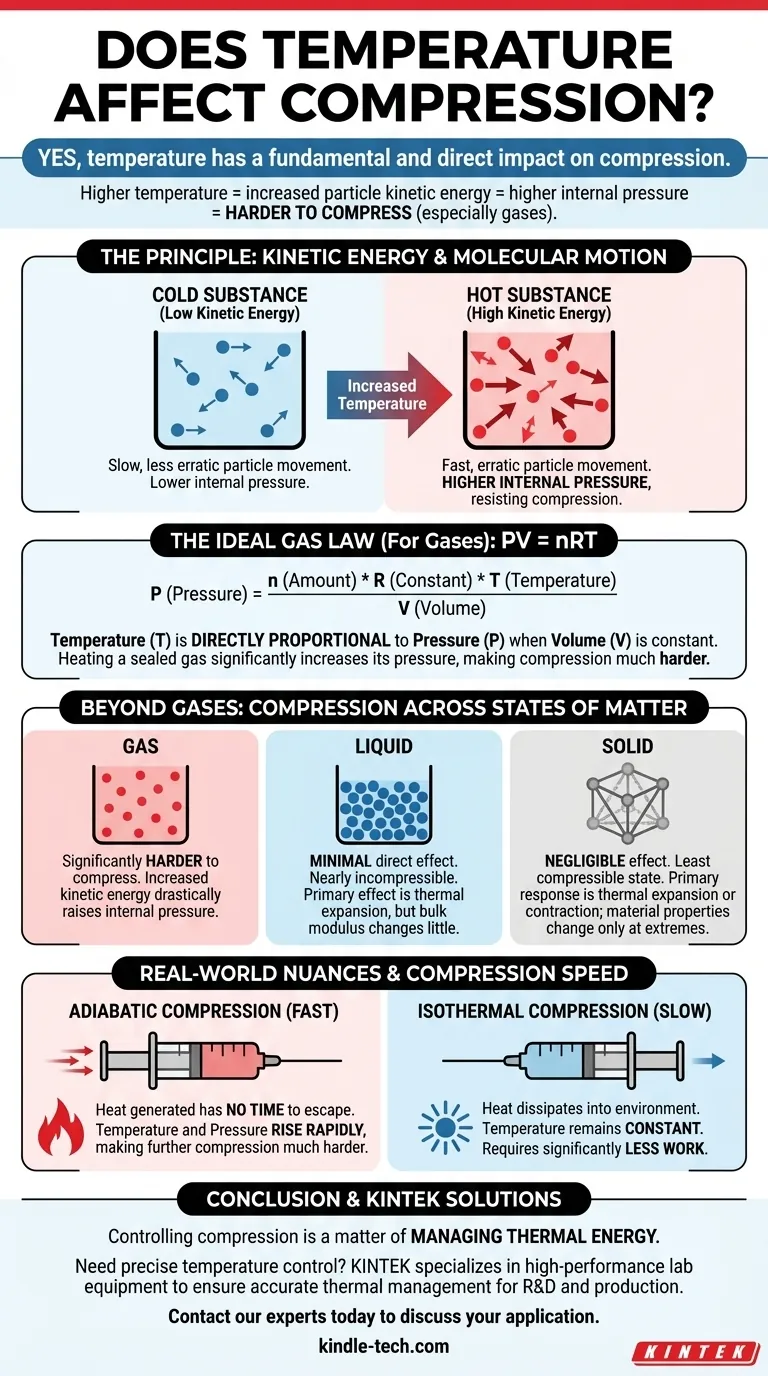
Sí, la temperatura tiene un impacto fundamental y directo en la compresión. Para los gases en particular, a medida que se aumenta la temperatura de una sustancia, sus partículas ganan energía cinética, se mueven más rápido y empujan hacia afuera con mayor fuerza. Este aumento de la presión interna hace que la sustancia sea significativamente más difícil de comprimir.
El principio fundamental es una relación directa entre energía y presión. Una temperatura más alta significa más energía de las partículas, lo que crea una presión interna más alta que debe superarse para comprimir una sustancia, especialmente un gas. Esta relación es una piedra angular de la termodinámica.

El Principio: Energía Cinética y Movimiento Molecular
Para entender por qué la temperatura afecta la compresión, necesitamos observar lo que sucede a nivel molecular.
Qué Representa la Temperatura
La temperatura no es una propiedad abstracta; es una medida directa de la energía cinética promedio de los átomos o moléculas dentro de una sustancia.
Las partículas más calientes se mueven más rápido y de forma más errática. Las partículas más frías se mueven más lentamente.
Cómo la Energía Cinética Resiste la Compresión
Cuando se comprime una sustancia, se están forzando sus partículas a acercarse. La energía cinética de estas partículas crea una presión interna que se opone a esta fuerza externa.
En un gas caliente, las partículas que se mueven rápidamente chocan con las paredes de su recipiente con más frecuencia y con mayor fuerza. Para reducir el volumen, se debe aplicar una fuerza externa significativamente mayor para superar esta potente presión interna.
Cuantificando la Relación: La Ley de los Gases Ideales
Para los gases, esta relación se describe elegantemente mediante un principio fundamental en física y química.
La Fórmula: PV = nRT
La Ley de los Gases Ideales proporciona un modelo matemático para el comportamiento de la mayoría de los gases bajo condiciones comunes. La fórmula es PV = nRT, donde:
- P es la presión
- V es el volumen
- n es la cantidad de gas
- R es la constante de los gases ideales
- T es la temperatura
El Papel Directo de la Temperatura
En esta ecuación, la temperatura (T) es directamente proporcional a la presión (P) si el volumen se mantiene constante.
Esto significa que si se toma un recipiente sellado de aire y se calienta, la presión en su interior aumentará. Este aumento de presión es la misma resistencia que se siente al intentar comprimir un gas caliente.
Una Analogía Simple: Una Bomba de Bicicleta
Cuando se usa una bomba manual para inflar un neumático, se está comprimiendo aire rápidamente. Se notará que el cilindro de la bomba se calienta.
Esto no se debe solo a la fricción. Se está realizando un trabajo sobre el gas, lo que aumenta su energía interna y, por lo tanto, su temperatura. Este efecto, conocido como calentamiento adiabático, hace que el aire sea más difícil de comprimir a medida que se bombea más rápido.
Más Allá de los Gases: Líquidos y Sólidos
Aunque el efecto es más dramático en los gases, la temperatura también influye en la compresión de líquidos y sólidos, aunque de diferentes maneras.
El Caso de los Líquidos
Los líquidos se consideran casi incompresibles. Sus moléculas ya están en contacto cercano, dejando poco espacio libre.
El efecto principal de la temperatura en un líquido es la expansión térmica. Calentar un líquido hará que se expanda ligeramente, pero su resistencia a la compresión (su módulo de compresibilidad) no cambia tan drásticamente como lo hace para un gas.
El Comportamiento de los Sólidos
Los sólidos son el estado de la materia menos compresible. Al igual que los líquidos, su respuesta principal al cambio de temperatura es la expansión o contracción térmica.
Si bien las temperaturas extremas pueden afectar las propiedades materiales de un sólido, como la rigidez, el impacto directo en su compresibilidad es insignificante en la mayoría de los escenarios de ingeniería en comparación con el efecto en los gases.
Errores Comunes y Matices del Mundo Real
La Ley de los Gases Ideales es un modelo potente, pero las aplicaciones del mundo real tienen complejidades importantes.
Gas Ideal vs. Gas Real
La Ley de los Gases Ideales asume que las partículas de gas no tienen volumen ni atracciones intermoleculares. Esta es una simplificación útil, pero los gases reales se desvían de este modelo a presiones muy altas o temperaturas muy bajas.
Compresión Adiabática vs. Isotérmica
La velocidad de compresión importa inmensamente.
- Compresión Adiabática (Rápida): Cuando se comprime un gas rápidamente, el calor generado no tiene tiempo para escapar. Este aumento de temperatura eleva la presión interna, haciendo que la compresión posterior sea mucho más difícil.
- Compresión Isotérmica (Lenta): Si se comprime un gas muy lentamente, el calor puede disiparse en el ambiente, manteniendo la temperatura constante. Esto requiere significativamente menos trabajo que la compresión adiabática.
Tomar la Decisión Correcta para su Objetivo
Su enfoque depende completamente de lo que esté tratando de lograr.
- Si su enfoque principal es la ingeniería de un sistema neumático o hidráulico: Debe gestionar activamente el calor. El aumento de temperatura por la compresión rápida (calentamiento adiabático) aumentará significativamente la fuerza requerida y puede afectar los sellos y la viscosidad del fluido.
- Si su enfoque principal es la gestión de recipientes sellados y presurizados: Debe tener en cuenta las fluctuaciones de temperatura ambiente. Un tanque llenado en una mañana fresca experimentará un aumento significativo de presión bajo el sol de la tarde, lo que puede convertirse en un factor crítico de seguridad.
- Si su enfoque principal es comprender la física fundamental: Comience con la Ley de los Gases Ideales (PV=nRT). Es el modelo esencial para comprender la relación directa y predecible entre temperatura, presión y volumen.
En última instancia, la temperatura es una forma de energía, y controlar la compresión es una cuestión de gestionar esa energía.
Tabla Resumen:
| Estado de la Materia | Efecto del Aumento de Temperatura en la Compresión | Principio Clave |
|---|---|---|
| Gas | Significativamente más difícil de comprimir | Ley de los Gases Ideales (PV=nRT); el aumento de la energía cinética eleva la presión interna. |
| Líquido | Efecto directo mínimo en la compresibilidad (casi incompresible) | El efecto principal es la expansión térmica; el módulo de compresibilidad cambia poco. |
| Sólido | Efecto insignificante en la compresibilidad en la mayoría de los escenarios | El efecto principal es la expansión/contracción térmica; las propiedades del material pueden cambiar en los extremos. |
¿Necesita un control preciso de la temperatura para sus procesos de compresión?
Comprender la termodinámica de la compresión es crucial para la I+D, el control de calidad y la optimización de procesos. KINTEK se especializa en equipos de laboratorio de alto rendimiento, incluidos hornos, estufas y sistemas de control de temperatura, diseñados para ayudarle a gestionar con precisión la energía térmica en sus experimentos y producción.
Deje que nuestros expertos le ayuden a seleccionar el equipo adecuado para garantizar resultados fiables y repetibles. Contacte hoy mismo a nuestro equipo técnico para discutir sus necesidades de aplicación específicas.
Guía Visual