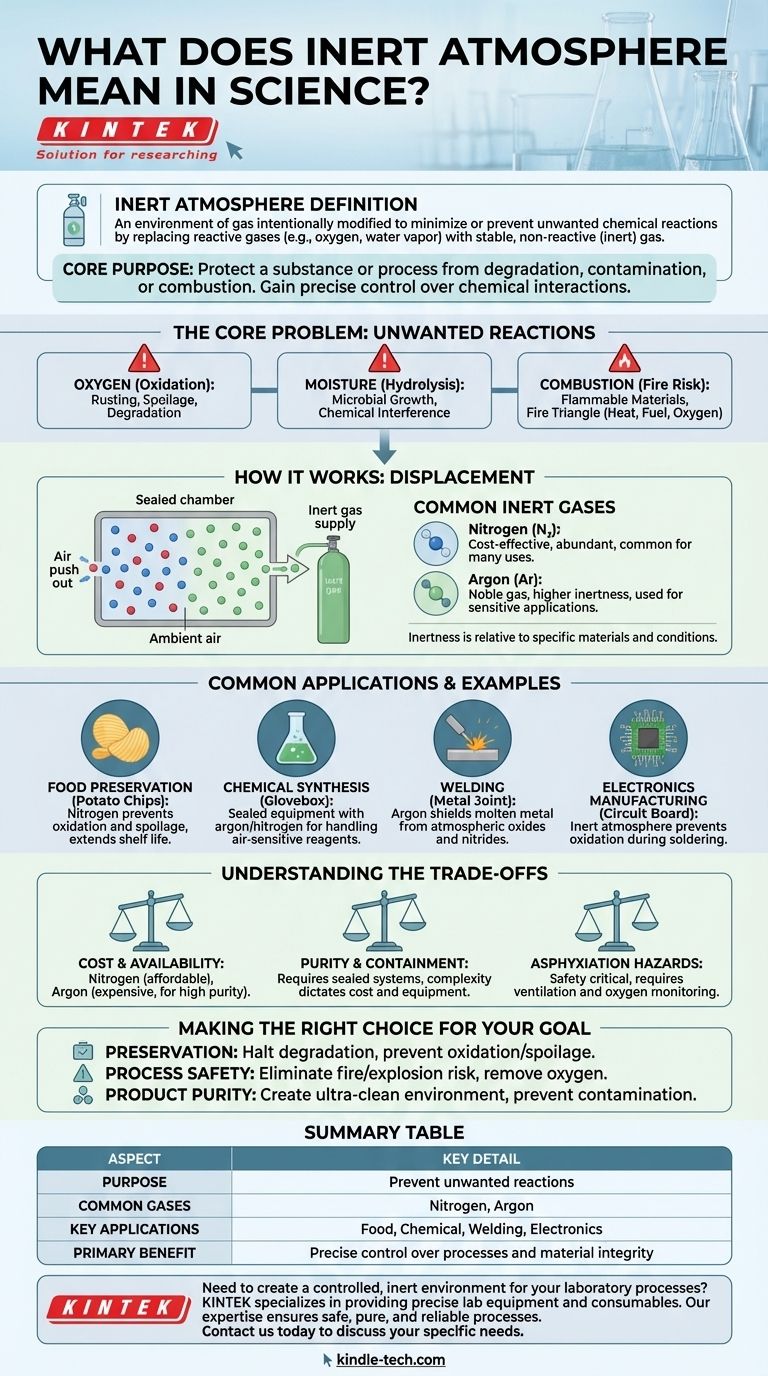
En un contexto científico, una atmósfera inerte se refiere a un entorno gaseoso que ha sido modificado intencionalmente para minimizar o prevenir reacciones químicas no deseadas. Esto se logra reemplazando gases reactivos, comúnmente oxígeno y vapor de agua, con un gas estable y no reactivo (o "inerte") como el nitrógeno o el argón.
El propósito central de crear una atmósfera inerte es proteger una sustancia o proceso de la degradación, contaminación o combustión. Al eliminar los elementos reactivos del entorno, se obtiene un control preciso sobre las interacciones químicas que pueden ocurrir.

El Problema Central: Reacciones No Deseadas
Para entender por qué son necesarias las atmósferas inertes, primero debemos identificar los problemas que resuelven. El aire ambiente es una mezcla de gases sorprendentemente reactiva y a menudo hostil para materiales y procesos sensibles.
El Papel del Oxígeno
El oxígeno es el culpable más común. Es altamente reactivo y participa fácilmente en la oxidación, un proceso que puede alterar fundamentalmente los materiales.
Esto incluye la oxidación de metales, el deterioro de los alimentos y la degradación de compuestos químicos sensibles.
El Impacto de la Humedad
El vapor de agua presente en el aire es otra fuente importante de reacciones no deseadas. Puede hidrolizar materiales sensibles, promover el crecimiento microbiano o interferir con la síntesis química.
El Riesgo de Combustión
Muchos procesos involucran materiales inflamables o altas temperaturas. La presencia de oxígeno crea un riesgo significativo de incendio o explosión, ya que es un componente clave del triángulo del fuego (calor, combustible y oxígeno).
Cómo Funciona una Atmósfera Inerte
La solución es conceptualmente simple: reemplazar la atmósfera reactiva con una no reactiva. Esto se logra típicamente a través de un proceso de purga o desplazamiento.
El Principio de Desplazamiento
El proceso implica purgar un contenedor o cámara sellada (como una caja de guantes o un recipiente de reacción) con un gas inerte. Este nuevo gas expulsa físicamente el aire ambiente, reemplazando efectivamente el oxígeno y la humedad reactivos con un gas estable.
Gases Inertes Comunes
La elección del gas depende de la aplicación específica, el costo y el nivel de inercia requerido.
El más común es el Nitrógeno (N₂), que es efectivo para muchas aplicaciones y relativamente económico. Para situaciones de mayor pureza o más exigentes, se utilizan gases nobles como el Argón (Ar) porque son aún menos reactivos.
El Concepto de "Inercia"
Es importante entender que "inerte" es un término relativo. Un gas se considera inerte si no reacciona con los materiales específicos en un sistema dado bajo condiciones específicas. El nitrógeno, por ejemplo, es inerte para la mayoría de los propósitos, pero puede reaccionar bajo temperaturas y presiones muy altas.
Aplicaciones y Ejemplos Comunes
El uso práctico de atmósferas inertes es generalizado en la ciencia y la industria, a menudo en formas que usted encuentra a diario.
En la Conservación de Alimentos
El aire dentro de una bolsa de patatas fritas no es solo "aire", sino típicamente nitrógeno. Esta atmósfera inerte evita que los aceites de las patatas se oxiden y se vuelvan rancios, extendiendo drásticamente su vida útil.
En la Síntesis Química
Muchos reactivos químicos son extremadamente sensibles al aire o la humedad. Los químicos utilizan equipos sellados purgados con argón o nitrógeno para manipular estos materiales, asegurando que sus reacciones se lleven a cabo según lo previsto y sin contaminación.
En Soldadura y Metalurgia
Al soldar aleaciones de alta resistencia, se utiliza un gas inerte como el argón para proteger el metal fundido de la atmósfera. Esto previene la formación de óxidos y nitruros que de otro modo debilitarían la soldadura.
En la Fabricación de Electrónica
Durante la soldadura de microchips y placas de circuito, los componentes son vulnerables a la oxidación. Una atmósfera inerte previene esto, asegurando que se formen conexiones eléctricas fuertes y fiables.
Comprender las Compensaciones
Aunque es potente, la implementación de una atmósfera inerte implica consideraciones prácticas que deben sopesarse.
Costo y Disponibilidad
El nitrógeno es abundante y asequible, lo que lo convierte en el caballo de batalla para muchas aplicaciones industriales. El argón de alta pureza y otros gases nobles son significativamente más caros y se reservan para cuando la no reactividad absoluta es crítica.
Pureza y Contención
Mantener una atmósfera verdaderamente inerte requiere sistemas bien sellados. El nivel de pureza requerido dicta la complejidad y el costo del equipo, desde contenedores simplemente purgados hasta sofisticadas cajas de guantes con circulación y purificación de gas constantes.
Riesgos de Asfixia
Una consideración de seguridad crítica es que los gases inertes desplazan el oxígeno. En un área mal ventilada, una fuga puede crear un ambiente con deficiencia de oxígeno que puede causar asfixia. Una ventilación adecuada y la monitorización del oxígeno son medidas de seguridad esenciales.
Tomar la Decisión Correcta para su Objetivo
La decisión de utilizar una atmósfera inerte está impulsada por el resultado específico que necesita lograr.
- Si su enfoque principal es la preservación: Su objetivo es detener la degradación desplazando el oxígeno y la humedad, previniendo así la oxidación y el deterioro.
- Si su enfoque principal es la seguridad del proceso: Su objetivo es eliminar el riesgo de incendio o explosión al eliminar el oxígeno necesario para la combustión.
- Si su enfoque principal es la pureza del producto: Su objetivo es crear un entorno ultra limpio, asegurando que ningún contaminante reactivo interfiera con un proceso sensible como la síntesis química o la fabricación de productos electrónicos.
En última instancia, una atmósfera inerte es una herramienta poderosa para tomar el control de un entorno químico y lograr un resultado preciso y fiable.
Tabla Resumen:
| Aspecto | Detalle Clave |
|---|---|
| Propósito | Prevenir reacciones no deseadas (oxidación, contaminación, combustión) |
| Gases Comunes | Nitrógeno (N₂), Argón (Ar) |
| Aplicaciones Clave | Conservación de alimentos, síntesis química, soldadura, fabricación de electrónica |
| Beneficio Principal | Control preciso sobre los procesos químicos y la integridad del material |
¿Necesita crear un ambiente inerte controlado para sus procesos de laboratorio? KINTEK se especializa en proporcionar el equipo de laboratorio y los consumibles precisos requeridos para sus aplicaciones, desde la síntesis química hasta la investigación de materiales. Nuestra experiencia garantiza que sus procesos sean seguros, puros y fiables. Contáctenos hoy para discutir sus necesidades específicas y descubrir la solución adecuada para su laboratorio.
Guía Visual
Productos relacionados
- Horno de Atmósfera Controlada de 1700 ℃ Horno de Atmósfera Inerte de Nitrógeno
- Horno de atmósfera controlada de 1200℃, horno de atmósfera inerte de nitrógeno
- Horno de atmósfera controlada de 1400 ℃ con nitrógeno y atmósfera inerte
- Horno de Atmósfera de Hidrógeno y Nitrógeno Controlado
La gente también pregunta
- ¿Cuáles son los dos propósitos principales del uso de una atmósfera controlada? Protección maestra vs. Modificación de materiales
- ¿Se puede soldar cobre con latón sin fundente? Sí, pero solo bajo estas condiciones específicas.
- ¿Cuál es la necesidad de hornos de atmósfera controlada para la corrosión por gas? Asegure un modelado preciso de fallas de materiales
- ¿Cómo se utiliza el oxígeno (O2) en atmósferas de horno controladas? Dominando la ingeniería de superficies para metales
- ¿Por qué es deseable un horno de atmósfera controlada en la sinterización? Lograr pureza y densidad superiores



