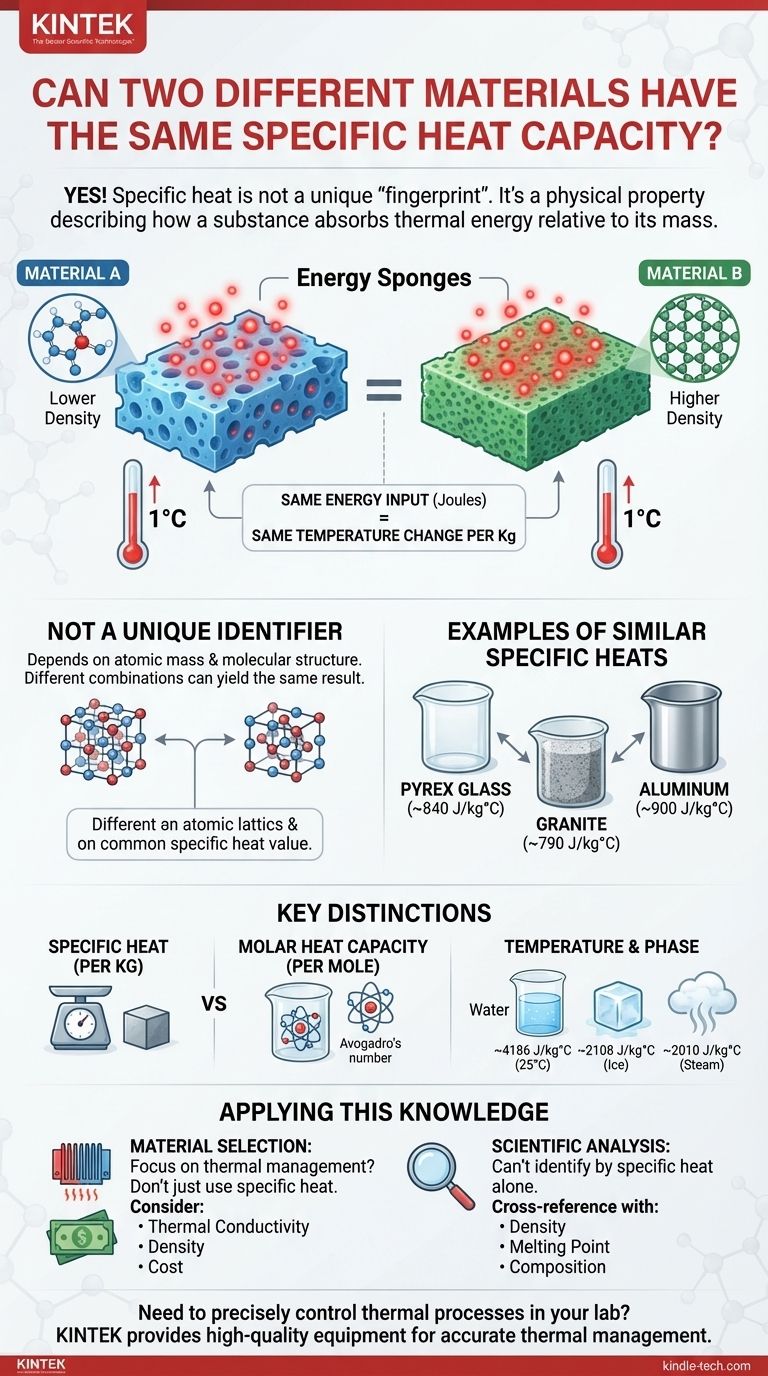
Sí, es totalmente posible que dos materiales diferentes tengan el mismo valor, o casi idéntico, de capacidad calorífica específica. La capacidad calorífica específica no es una "huella dactilar" única como un número atómico. En cambio, es una propiedad física que describe cómo una sustancia absorbe energía térmica en relación con su masa, y diferentes combinaciones de masa atómica y estructura molecular pueden conducir al mismo resultado.
La conclusión principal es que la capacidad calorífica específica es una medida del comportamiento térmico, no un identificador fundamental. Surge de interacciones complejas a nivel atómico, y es totalmente posible que dos materiales distintos exhiban el mismo comportamiento a través de diferentes estructuras subyacentes.

Lo que realmente representa la capacidad calorífica específica
Una analogía de la "esponja de energía"
Piense en la capacidad calorífica específica como la "absorbencia" de la esponja térmica de un material. Cuantifica cuánta energía (en julios) debe agregar a un kilogramo de una sustancia para elevar su temperatura en un grado Celsius (o Kelvin).
Un material con una capacidad calorífica baja, como el cobre (~385 J/kg°C), es como una esponja pequeña y densa. Se "satura" de energía muy rápidamente, lo que significa que su temperatura aumenta rápido.
Un material con una capacidad calorífica alta, como el agua (~4186 J/kg°C), es como una esponja grande y absorbente. Puede absorber una gran cantidad de energía antes de que su temperatura aumente significativamente.
Por qué no es un identificador único
El calor específico es una propiedad macroscópica que resulta de factores microscópicos, principalmente:
- Masa atómica: Los átomos más pesados generalmente significan menos átomos en un kilogramo de material.
- Estructura molecular: La forma en que los átomos están unidos determina cómo pueden almacenar energía a través de vibraciones y rotaciones (sus "grados de libertad").
Dado que el calor específico depende de la interacción de estos factores, diferentes combinaciones pueden producir coincidentemente el mismo valor. Un material con átomos más ligeros pero enlaces muy fuertes podría terminar teniendo el mismo calor específico que uno con átomos más pesados y enlaces más débiles.
Ejemplos de calores específicos similares
Si bien encontrar dos materiales con el valor exacto es raro, muchos tienen valores extremadamente cercanos e indistinguibles en la práctica para fines de ingeniería.
Materiales comunes
Considere estos valores (a temperatura ambiente):
- Vidrio Pyrex: ~840 J/kg°C
- Granito: ~790 J/kg°C
- Aluminio: ~900 J/kg°C
Aquí, el vidrio y el granito tienen capacidades muy similares para absorber y almacenar calor por unidad de masa, a pesar de ser sustancias completamente diferentes.
Materiales avanzados
El principio es aún más claro con los materiales de ingeniería. Es posible crear aleaciones o compuestos con propiedades térmicas específicas. Un ingeniero podría diseñar intencionalmente un material para que coincida con el calor específico de otra sustancia para una aplicación en particular.
Distinciones y consideraciones clave
Calor específico frente a capacidad calorífica molar
Esta es la distinción más crítica. Mientras que el calor específico se mide por unidad de masa (por kilogramo), la capacidad calorífica molar se mide por unidad de sustancia (por mol).
Un mol es un número fijo de átomos o moléculas (número de Avogadro). Para muchos elementos sólidos simples, la capacidad calorífica molar es sorprendentemente similar (la ley de Dulong-Petit).
Esto nos dice que en base por átomo, muchos materiales absorben una cantidad similar de energía. La razón principal por la que sus calores específicos (por kilogramo) son tan diferentes es que sus átomos tienen masas diferentes.
La influencia de la temperatura y la fase
El calor específico de un material no es una constante fija. Cambia con la temperatura y cambia drásticamente durante las transiciones de fase.
Por ejemplo, el calor específico del agua (~4186 J/kg°C) es casi el doble que el del hielo (~2108 J/kg°C) o el vapor (~2010 J/kg°C). Por lo tanto, dos materiales podrían compartir un valor de calor específico a 25 °C pero tener valores muy diferentes a 100 °C.
Cómo aplicar este conocimiento
Para la selección de materiales
Si su objetivo principal es la gestión térmica (como en un disipador de calor o una batería térmica), no puede elegir un material basándose únicamente en el calor específico.
Un alto calor específico es bueno para almacenar energía térmica, pero también debe considerar la conductividad térmica (qué tan rápido absorbe/libera energía), la densidad (cuánta masa cabe en un volumen dado) y el costo. El hecho de que varios materiales puedan tener calores específicos similares le brinda la flexibilidad de optimizar estos otros factores críticos.
Para el análisis científico
Nunca podrá identificar de forma concluyente una sustancia desconocida midiendo solo su calor específico. Proporciona una pista, pero no es una prueba concluyente.
La identificación adecuada requiere la referencia cruzada de múltiples propiedades, como la densidad, el punto de fusión, la conductividad térmica y la composición química.
Haciendo la interpretación correcta
Comprender este concepto le permite utilizar las propiedades de los materiales de manera más efectiva.
- Si su enfoque principal es la ingeniería: Reconozca que el calor específico es una métrica de rendimiento, y que varios materiales pueden cumplir con sus requisitos térmicos, lo que le permite optimizar otros factores como el peso, la conductividad o el costo.
- Si su enfoque principal es el análisis científico: Utilice el calor específico como una propiedad entre muchas para caracterizar una sustancia, pero nunca confíe en él de forma aislada para la identificación.
En última instancia, ver las propiedades de un material como una descripción de su comportamiento, en lugar de una identidad fija, es la clave para una comprensión más profunda y la innovación.
Tabla de resumen:
| Material | Capacidad calorífica específica (J/kg°C) | Conclusión clave |
|---|---|---|
| Vidrio Pyrex | ~840 | Valores similares muestran que el calor específico no es una huella dactilar única. |
| Granito | ~790 | Sustancias diferentes pueden tener un comportamiento térmico casi idéntico. |
| Agua | ~4186 | El alto calor específico es bueno para el almacenamiento de energía, pero otros factores importan. |
| Aluminio | ~900 | La selección de materiales también debe considerar la conductividad, la densidad y el costo. |
¿Necesita controlar con precisión los procesos térmicos en su laboratorio?
Comprender las propiedades de los materiales como la capacidad calorífica específica es crucial para obtener resultados fiables. KINTEK se especializa en proporcionar equipos de laboratorio y consumibles de alta calidad, desde hornos hasta herramientas de análisis térmico, que le ayudan a medir y gestionar con precisión la transferencia de calor.
Permita que nuestra experiencia apoye su investigación y desarrollo. Contacte hoy a nuestros especialistas en térmica para discutir sus necesidades específicas de laboratorio y encontrar la solución adecuada.
Guía Visual