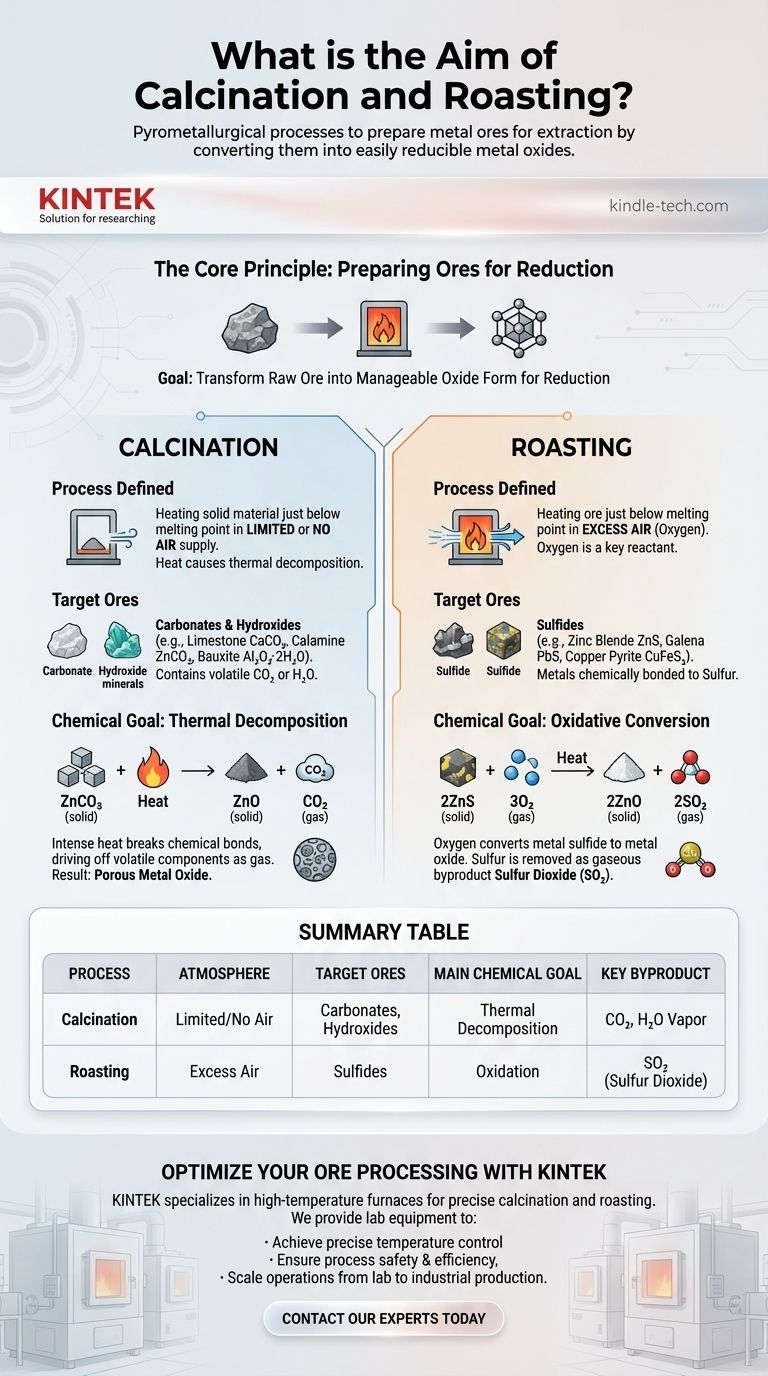
En resumen, la calcinación y la tostación son procesos pirometalúrgicos diseñados para preparar los minerales metálicos para la extracción. Ambos utilizan altas temperaturas para convertir los minerales en óxidos metálicos, una forma química que es mucho más fácil de reducir a un metal puro. La calcinación logra esto descomponiendo térmicamente el mineral en aire limitado o nulo, mientras que la tostación utiliza un exceso de aire para oxidar el mineral.
La distinción principal radica en el tipo de mineral que se trata. La calcinación es para minerales que se descomponen solo con calor, como carbonatos e hidróxidos. La tostación es para minerales que requieren oxígeno para ser convertidos, principalmente sulfuros.

El Principio Fundamental: Preparación de Minerales para la Reducción
El objetivo final de la metalurgia es extraer un metal puro de su mineral natural. La mayoría de los minerales, como los carbonatos (como la piedra caliza) o los sulfuros (como la blenda de zinc), no se convierten fácilmente directamente en metal.
Sin embargo, los óxidos metálicos se "reducen" fácilmente a su forma metálica, a menudo reaccionando con carbono (coque) en un horno de alta temperatura. Por lo tanto, tanto la calcinación como la tostación sirven como un paso de pretratamiento crucial: transformar el mineral crudo en esta forma de óxido más manejable.
Entendiendo la Calcinación
El Proceso Definido
La calcinación implica calentar un material sólido a una temperatura alta, justo por debajo de su punto de fusión, en la ausencia total o un suministro muy limitado de aire.
El calor en sí mismo es el agente principal del cambio, haciendo que el material se descomponga sin quemarse.
Los Minerales Objetivo
Este proceso es ideal para minerales de carbonato e hidróxido. Estos minerales contienen componentes volátiles como dióxido de carbono (CO₂) o agua (H₂O) unidos químicamente dentro de su estructura.
Ejemplos comunes incluyen la piedra caliza (CaCO₃), la calamina (ZnCO₃) y la bauxita (Al₂O₃·2H₂O).
El Objetivo Químico: Descomposición Térmica
El objetivo de la calcinación es la descomposición térmica. El calor intenso rompe los enlaces químicos en el mineral, expulsando los componentes volátiles en forma de gas.
Para un mineral de carbonato como el carbonato de zinc, la reacción es simple:
ZnCO₃ (sólido) + Calor → ZnO (sólido) + CO₂ (gas)
El resultado es un óxido metálico sólido y poroso (óxido de zinc) listo para la siguiente etapa de reducción.
Entendiendo la Tostación
El Proceso Definido
La tostación implica calentar un mineral a alta temperatura, también por debajo de su punto de fusión, pero en presencia de un exceso de aire (oxígeno).
A diferencia de la calcinación, el oxígeno es un reactivo clave en el proceso.
Los Minerales Objetivo
La tostación es el método estándar para procesar minerales de sulfuro. Estos minerales contienen metales valiosos unidos químicamente al azufre.
Ejemplos famosos incluyen la blenda de zinc (ZnS), la galena (PbS) y la pirita de cobre (CuFeS₂).
El Objetivo Químico: Conversión Oxidativa
El objetivo de la tostación es usar el oxígeno del aire para convertir el sulfuro metálico en un óxido metálico. El azufre se elimina como un subproducto gaseoso, dióxido de azufre (SO₂).
Para un mineral de sulfuro como la blenda de zinc, la reacción es:
2ZnS (sólido) + 3O₂ (gas) + Calor → 2ZnO (sólido) + 2SO₂ (gas)
Esta reacción reemplaza el azufre con oxígeno, produciendo nuevamente el óxido metálico deseado (óxido de zinc).
Entendiendo las Ventajas y Desventajas y las Diferencias Clave
Suministro de Aire: El Factor Determinante
La diferencia más crítica es la atmósfera dentro del horno.
La calcinación requiere la exclusión de aire para asegurar que el mineral simplemente se descomponga. La tostación requiere una abundancia de aire para proporcionar el oxígeno necesario para la reacción de oxidación.
Gestión de Subproductos
Los subproductos de cada proceso son fundamentalmente diferentes y tienen implicaciones ambientales y económicas distintas.
La calcinación produce principalmente dióxido de carbono (CO₂) o vapor de agua, que son relativamente benignos. La tostación produce dióxido de azufre (SO₂), un importante contaminante atmosférico responsable de la lluvia ácida. Las fundiciones modernas deben capturar este SO₂, que a menudo se utiliza para fabricar ácido sulfúrico, convirtiendo un producto de desecho dañino en un producto valioso.
¿Por qué no simplemente calcinar un mineral de sulfuro?
Calentar un mineral de sulfuro sin aire (calcinación) no eliminaría eficazmente el azufre ni lo convertiría en un óxido. El proceso depende del oxígeno para romper el enlace metal-azufre y formar el enlace metal-oxígeno más estable.
Selección del Proceso de Pretratamiento Correcto
Elegir entre calcinación y tostación no es una cuestión de preferencia, sino una necesidad química dictada por la composición del mineral.
- Si su enfoque principal es procesar un mineral de carbonato o hidróxido: Use la calcinación para descomponer térmicamente el mineral y expulsar el dióxido de carbono o el agua.
- Si su enfoque principal es procesar un mineral de sulfuro: Use la tostación para oxidar el mineral con exceso de aire, convirtiéndolo en un óxido metálico y eliminando el azufre como dióxido de azufre.
Hacer coincidir el proceso pirometalúrgico correcto con la química específica del mineral es el paso fundamental para una extracción de metales eficiente y exitosa.
Tabla Resumen:
| Proceso | Atmósfera | Minerales Objetivo | Objetivo Químico Principal | Subproducto Clave |
|---|---|---|---|---|
| Calcinación | Aire Limitado/Nulo | Carbonatos, Hidróxidos | Descomposición Térmica | CO₂, Vapor de H₂O |
| Tostación | Exceso de Aire | Sulfuros | Oxidación | SO₂ (Dióxido de Azufre) |
Optimice su Procesamiento de Minerales con KINTEK
Comprender el proceso de pretratamiento correcto es el primer paso para una extracción de metales eficiente. KINTEK se especializa en el suministro de los robustos hornos de alta temperatura necesarios para operaciones precisas de calcinación y tostación.
Proporcionamos el equipo de laboratorio y los consumibles esenciales para ayudarle a:
- Lograr un control preciso de la temperatura para una descomposición térmica u oxidación efectiva.
- Garantizar la seguridad y eficiencia del proceso, ya sea que trabaje con carbonatos o sulfuros.
- Escalar sus operaciones desde la investigación de laboratorio hasta la producción industrial.
¿Listo para mejorar sus procesos pirometalúrgicos? Contacte a nuestros expertos hoy para discutir la solución de horno perfecta para la química de su mineral y sus objetivos de producción específicos.
Guía Visual