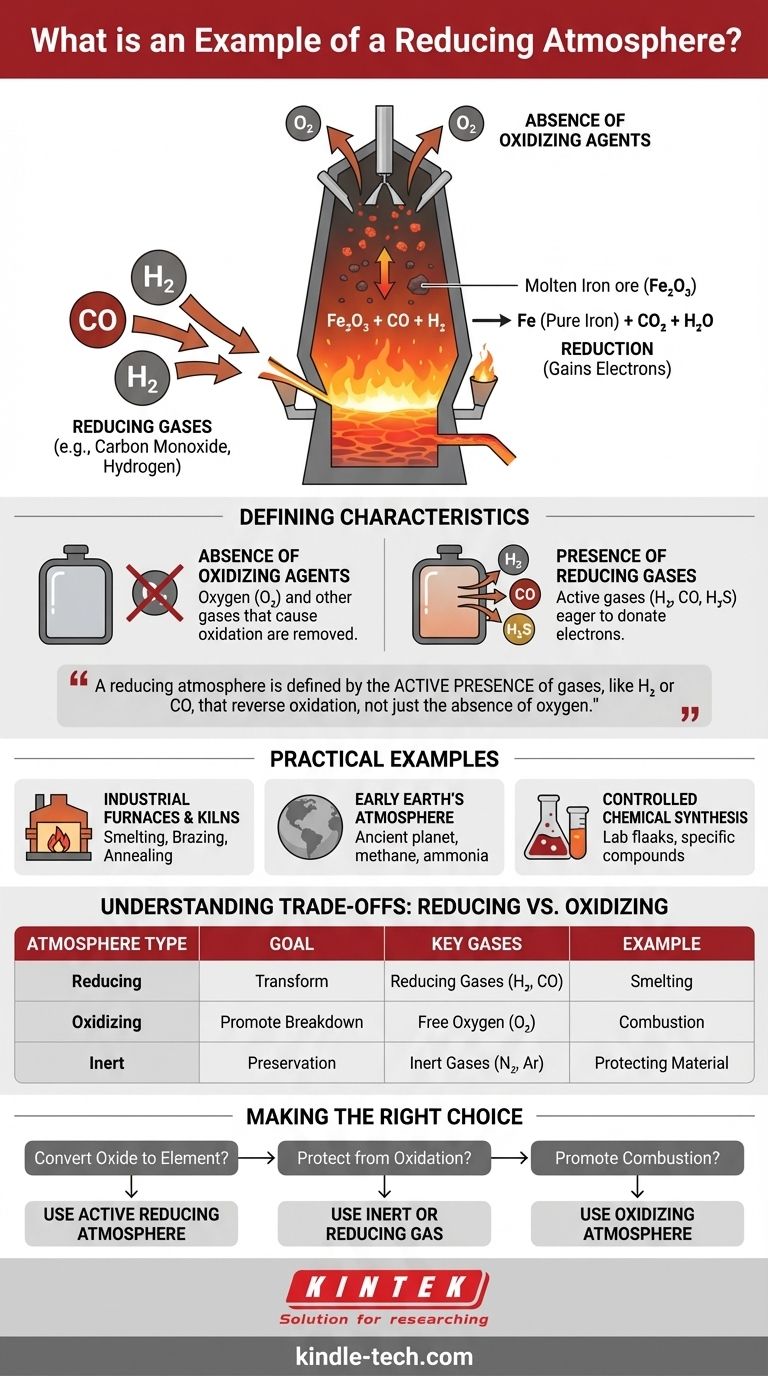
Un ejemplo clásico de atmósfera reductora es el entorno dentro de un alto horno utilizado para fundir mineral de hierro. En este proceso de alta temperatura, el oxígeno se elimina deliberadamente y se introduce monóxido de carbono, creando una condición que despoja activamente a los átomos de oxígeno del mineral de hierro, "reduciéndolo" así a hierro metálico puro.
La conclusión fundamental es que una atmósfera reductora no se trata solo de la ausencia de oxígeno; se define por la presencia activa de gases, como el hidrógeno o el monóxido de carbono, que están químicamente impulsados a donar electrones y revertir el proceso de oxidación.

¿Qué define una atmósfera "reductora"?
Para comprender completamente el concepto, es esencial comprender sus dos características definitorias: lo que está ausente y lo que está presente.
La ausencia de agentes oxidantes
El primer paso para crear una atmósfera reductora es la eliminación de oxígeno y otros gases que causan oxidación.
La atmósfera de nuestra vida cotidiana es una atmósfera oxidante. Es la razón por la que una rodaja de manzana se vuelve marrón y el hierro se oxida. Estos procesos son impulsados por la presencia de oxígeno libre.
La presencia de gases reductores
Una verdadera atmósfera reductora contiene agentes reductores activos. Estos son gases que son químicamente inestables y están ansiosos por donar electrones a otras sustancias.
Los ejemplos comunes incluyen hidrógeno (H₂), monóxido de carbono (CO) y sulfuro de hidrógeno (H₂S). Estos gases buscan activamente átomos de oxígeno en otros materiales y se unen a ellos.
La reacción química (Reducción)
Este entorno facilita una reacción química llamada reducción. En química, la reducción ocurre cuando un átomo o molécula gana electrones, disminuyendo su estado de oxidación.
En el ejemplo del alto horno, el monóxido de carbono (CO) cede electrones al óxido de hierro (Fe₂O₃), que los gana. Esto reduce el mineral de hierro a hierro elemental (Fe).
Ejemplos prácticos en la naturaleza y la industria
Comprender dónde ocurren estas atmósferas ayuda a solidificar el concepto y su importancia.
Hornos y calcinadores industriales
La fundición, soldadura fuerte y recocido de metales a menudo se realizan en una atmósfera reductora. Esto evita la formación de óxidos (cascarilla u óxido) en la superficie del metal a altas temperaturas, asegurando un producto final limpio y fuerte.
La atmósfera de la Tierra primitiva
Hace miles de millones de años, antes del surgimiento de la vida fotosintética, la atmósfera de la Tierra era naturalmente reductora. Era rica en gases como metano, amoníaco y vapor de agua, pero contenía prácticamente nada de oxígeno libre.
Síntesis química controlada
En laboratorios y plantas químicas, se crean atmósferas reductoras para producir compuestos químicos específicos. El entorno controlado asegura que solo ocurra la reacción de reducción deseada sin la interferencia de una oxidación no deseada.
Comprender las compensaciones: Reductora frente a Oxidante
La elección entre crear una atmósfera reductora, inerte u oxidante es una decisión de ingeniería crítica impulsada por el resultado deseado. Las compensaciones son fundamentales.
Objetivo: Transformación frente a Preservación
Una atmósfera oxidante promueve la descomposición (oxidación, combustión). Una atmósfera reductora promueve la transformación al eliminar el oxígeno de los compuestos. Una atmósfera inerte (como el argón puro) se utiliza para la preservación, evitando que ocurra cualquier reacción.
El desafío de la seguridad y el control
Las atmósferas reductoras a menudo involucran gases que son inflamables (hidrógeno) o tóxicos (monóxido de carbono). Mantener estas condiciones, especialmente a altas temperaturas, requiere controles de ingeniería sofisticados para garantizar la seguridad y la eficiencia del proceso.
Costo y complejidad
Crear y mantener una condición atmosférica específica es una capa adicional de complejidad y costo. Sin embargo, para muchos procesos industriales, este control no es opcional: es la única forma de producir el material deseado.
Tomar la decisión correcta para su objetivo
Su comprensión de las condiciones atmosféricas debe vincularse directamente con el objetivo químico que desea lograr.
- Si su enfoque principal es convertir un óxido en su elemento puro (p. ej., mineral a metal): Necesita una atmósfera reductora activa que contenga un gas como monóxido de carbono o hidrógeno.
- Si su enfoque principal es proteger un material de la oxidación superficial durante el tratamiento térmico: Necesita desplazar el oxígeno, lo que se puede hacer con un gas inerte (como nitrógeno o argón) o un gas reductor.
- Si su enfoque principal es la combustión o la simulación del desgaste natural: Necesita una atmósfera oxidante, específicamente una con una cantidad controlada de oxígeno.
En última instancia, la naturaleza de una atmósfera se define por qué reacciones químicas promueve y cuáles previene.
Tabla de resumen:
| Característica | Atmósfera Reductora | Atmósfera Oxidante |
|---|---|---|
| Objetivo principal | Transformar materiales (p. ej., mineral a metal) | Promover la descomposición (p. ej., combustión, oxidación) |
| Ausencia clave | Oxígeno Libre (O₂) | N/A |
| Presencia clave | Gases Reductores (H₂, CO) | Oxígeno Libre (O₂) |
| Proceso de ejemplo | Fundición de hierro en un alto horno | Quema de combustible, desgaste natural |
¿Necesita un control atmosférico preciso para sus procesos de laboratorio? KINTEK se especializa en equipos y consumibles de laboratorio, proporcionando las herramientas y la experiencia para crear y gestionar los entornos reductores, inertes u oxidantes exactos que su investigación o producción requiere. Asegure la pureza y calidad de sus materiales: ¡contacte a nuestros expertos hoy para discutir su aplicación específica!
Guía Visual
Productos relacionados
La gente también pregunta
- ¿Por qué la celda electroquímica debe purgarse continuamente con nitrógeno? Garantice la precisión en las pruebas de corrosión de Ni-Cr
- ¿Cuál es la diferencia entre una pila voltaica y una celda electroquímica? Comprenda los Dos Tipos de Conversión de Energía
- ¿Por qué las celdas electroquímicas deben tener un condensador y un sello de agua para estudios de la aleación 22 a 90 °C? Garantizar la integridad de los datos
- ¿Por qué se especifican los materiales de PTFE para las pruebas de REH alcalinas? Garantice el rendimiento y la precisión de los catalizadores de alta pureza
- ¿Cuál es el procedimiento para iniciar el experimento y qué se debe observar? Una guía paso a paso para una electroquímica fiable
