Contrariamente a una idea errónea común, la calcinación no es un proceso de quema. Si bien ambos implican altas temperaturas, son transformaciones químicas fundamentalmente diferentes. La calcinación es un proceso de descomposición térmica, donde el calor se utiliza para descomponer un compuesto, a menudo para eliminar un componente volátil como el dióxido de carbono o el agua.
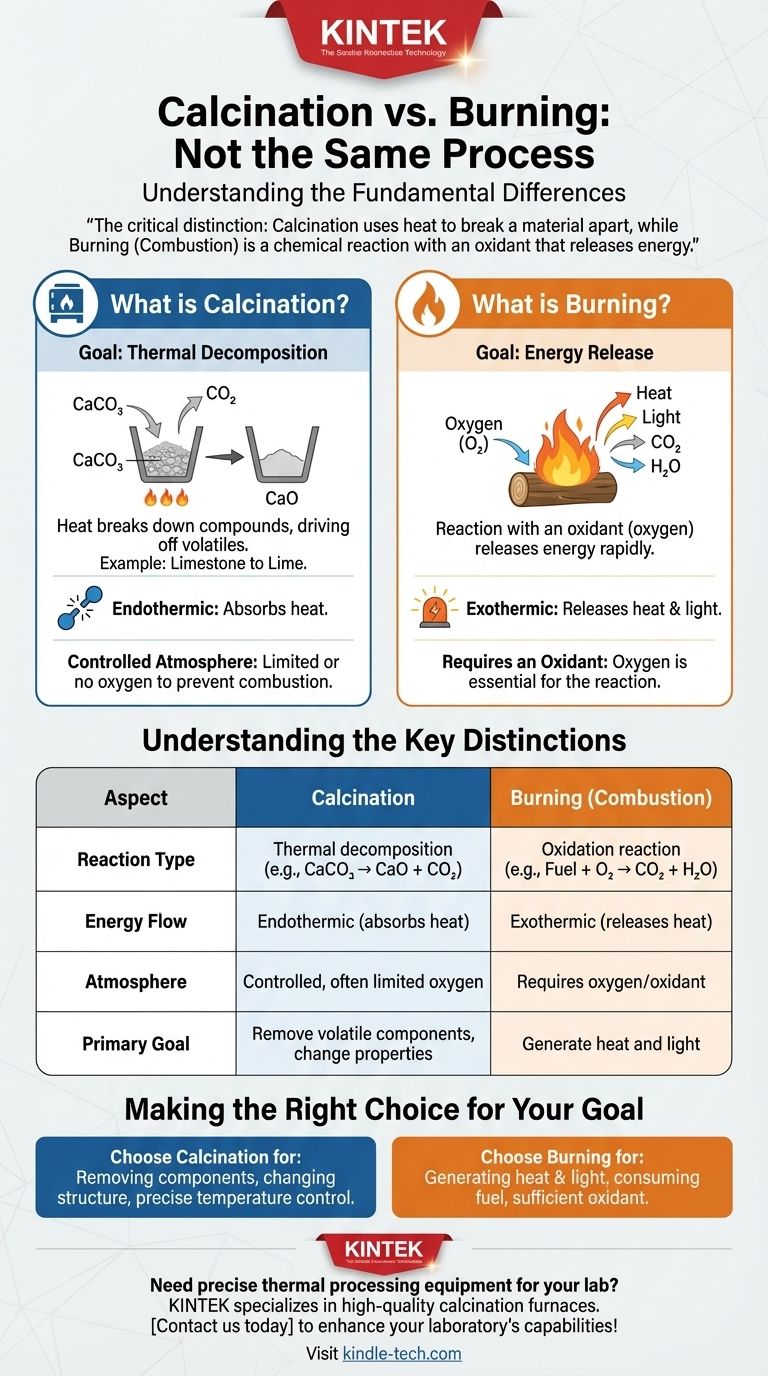
La distinción crítica es esta: la calcinación utiliza el calor para romper un material, a menudo en una atmósfera controlada, mientras que la quema (combustión) es una reacción química con un oxidante como el oxígeno que libera energía.

¿Qué es la Calcinación?
La calcinación es un proceso de tratamiento térmico preciso utilizado para cambiar las propiedades químicas y físicas de un material. El término se deriva del latín calcinare, que significa 'quemar cal'.
El Objetivo: Descomposición Térmica
El propósito principal de la calcinación es provocar la descomposición térmica. El calor proporciona la energía necesaria para romper los enlaces químicos dentro de una sustancia, haciendo que se separe en componentes más simples.
Un Ejemplo Común: Piedra Caliza a Cal Viva
La producción de cal a partir de piedra caliza es el ejemplo clásico. Cuando la piedra caliza (carbonato de calcio, CaCO₃) se calienta a una temperatura alta, se descompone.
Este proceso elimina el dióxido de carbono (CO₂) gaseoso, dejando atrás la cal viva (óxido de calcio, CaO), un componente crucial en el cemento y otros materiales industriales.
El Papel de una Atmósfera Controlada
Fundamentalmente, la calcinación a menudo tiene lugar en una atmósfera con oxígeno limitado o nulo. Esto se hace específicamente para prevenir la combustión y asegurar que solo ocurra la reacción de descomposición deseada.
¿Cómo se Diferencia de la Quema?
La quema, conocida químicamente como combustión, es una reacción exotérmica a alta temperatura entre un combustible y un oxidante, más comúnmente oxígeno del aire.
El Requisito de un Oxidante
A diferencia de la calcinación, la quema no puede ocurrir sin un oxidante. Cuando se quema madera, los compuestos orgánicos de la madera no solo se están descomponiendo; están reaccionando activamente con el oxígeno.
El Objetivo: Liberación de Energía
El resultado principal de la combustión es la rápida liberación de energía en forma de calor y luz. Si bien también produce nuevas sustancias químicas (como ceniza, dióxido de carbono y vapor de agua), la liberación de energía es su característica definitoria.
Comprender las Distinciones Clave
Confundir estos dos procesos puede llevar a errores significativos en el procesamiento de materiales, la química y la ingeniería. Las diferencias son claras y absolutas.
Tipo de Reacción
La calcinación es una reacción de descomposición. Un solo compuesto se descompone en dos o más productos más simples (p. ej., CaCO₃ → CaO + CO₂).
La combustión es una reacción de oxidación. Un combustible reacciona con un oxidante para formar nuevos productos oxidados (p. ej., CH₄ + 2O₂ → CO₂ + 2H₂O).
Flujo de Energía
La calcinación es típicamente un proceso endotérmico. Requiere una entrada continua de energía (calor) para sostener la reacción y romper los enlaces químicos.
La combustión es un proceso exotérmico. Una vez iniciada, libera mucha más energía de la que se requirió para comenzar, creando una reacción autosostenida.
Tomar la Decisión Correcta para su Objetivo
Comprender si necesita calcinar o quemar es fundamental para lograr el resultado deseado en cualquier proceso térmico.
- Si su enfoque principal es eliminar un componente específico de un sólido (como agua o CO₂) o cambiar su estructura cristalina: Está realizando una calcinación, donde el control preciso de la temperatura y la gestión de la atmósfera son críticos.
- Si su enfoque principal es generar calor y luz consumiendo un combustible: Está realizando una combustión, donde asegurar un suministro suficiente de un oxidante como el aire es la principal prioridad.
Distinguir entre estos dos procesos fundamentales es esencial para controlar las reacciones químicas e ingeniar materiales de manera efectiva.
Tabla Resumen:
| Aspecto | Calcinación | Quema (Combustión) |
|---|---|---|
| Tipo de Reacción | Descomposición térmica | Reacción de oxidación |
| Flujo de Energía | Endotérmica (absorbe calor) | Exotérmica (libera calor) |
| Atmósfera | Controlada, a menudo con oxígeno limitado | Requiere oxígeno/oxidante |
| Objetivo Principal | Eliminar componentes volátiles, cambiar propiedades del material | Generar calor y luz |
¿Necesita equipo de procesamiento térmico preciso para su laboratorio? KINTEK se especializa en hornos de calcinación de alta calidad y equipos de laboratorio diseñados para la descomposición térmica controlada. Nuestras soluciones garantizan un control preciso de la temperatura y una gestión de la atmósfera para la transformación de materiales. Contáctenos hoy para mejorar las capacidades de su laboratorio.
Guía Visual
Productos relacionados
- Planta de Horno de Pirólisis de Horno Rotatorio Eléctrico Máquina Calcinadora Horno Rotatorio Pequeño Horno Giratorio
- Horno Rotatorio Eléctrico de Trabajo Continuo, Pequeña Planta de Pirólisis con Calefacción de Horno Rotatorio
- Horno de Fusión por Inducción de Arco al Vacío No Consumible
- Horno Vertical de Vacío de Grafito de Alta Temperatura para Grafización
- Horno de grafización al vacío a ultra alta temperatura de grafito
La gente también pregunta
- ¿Qué aparato se utiliza en la pirólisis? Seleccione el reactor adecuado para su producción de bioaceite o biocarbón
- ¿Cuáles son los principios de un horno rotatorio? Domina la mecánica del procesamiento a alta temperatura
- ¿Cuáles son las características de los modos de movimiento de lecho de deslizamiento, colapso y rodadura? Optimice su proceso rotatorio
- ¿Cómo se calientan los hornos rotatorios? Explicación de los métodos de calentamiento directo vs. indirecto
- ¿Cuáles son las ventajas del horno de horno rotatorio? Logre una uniformidad y eficiencia superiores



















