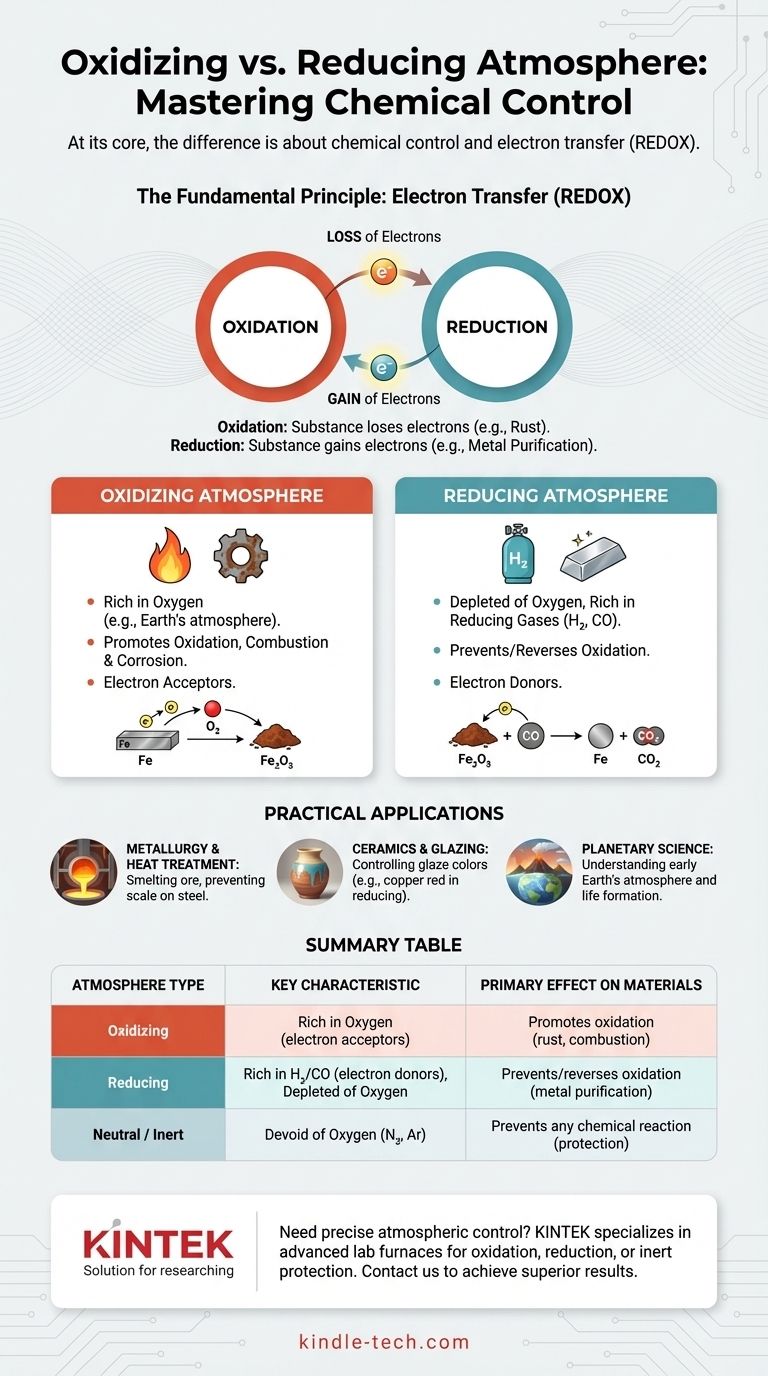
En esencia, la diferencia radica en el control químico. Una atmósfera oxidante es rica en oxígeno u otras sustancias que aceptan electrones, promoviendo reacciones como la combustión y la corrosión. En contraste directo, una atmósfera reductora está intencionalmente desprovista de oxígeno y a menudo contiene gases como hidrógeno o monóxido de carbono que donan electrones, lo que previene o incluso revierte la oxidación.
La distinción clave no es solo la presencia de oxígeno, sino si la química de la atmósfera hace que un material pierda electrones (oxidación) o gane electrones (reducción). Elegir la atmósfera correcta es fundamental para controlar el resultado de los procesos de alta temperatura, desde la fabricación de acero hasta la cocción de cerámica artística.

El Principio Fundamental: Transferencia de Electrones
Para comprender verdaderamente la diferencia, debe ir más allá de los gases y centrarse en la química subyacente del intercambio de electrones. Esto se conoce como REDOX (Reducción-Oxidación).
Comprendiendo la Oxidación: La Pérdida de Electrones
La oxidación es un proceso químico donde una sustancia pierde electrones. Aunque el oxígeno es el agente oxidante más famoso, no es el único.
El ejemplo clásico es el óxido. Cuando el hierro se expone a una atmósfera rica en oxígeno, los átomos de hierro pierden electrones a los átomos de oxígeno, formando óxido de hierro. El material ha sido oxidado.
Comprendiendo la Reducción: La Ganancia de Electrones
La reducción es el proceso exactamente opuesto: una sustancia gana electrones. Esto "reduce" su estado de oxidación.
En una atmósfera reductora, están presentes gases como el hidrógeno (H₂) o el monóxido de carbono (CO). Estos gases son donantes de electrones; ceden fácilmente sus electrones a otras sustancias, revirtiendo el proceso de oxidación.
Características de Cada Entorno
La composición de la atmósfera dicta directamente su comportamiento químico y su efecto sobre los materiales dentro de ella.
La Atmósfera Oxidante
Un ambiente oxidante se caracteriza por una abundancia de oxígeno libre u otros agentes oxidantes. La atmósfera terrestre es el ejemplo más común.
Este ambiente soporta y acelera la combustión. También es el principal impulsor de la corrosión y degradación de muchos materiales, especialmente metales a altas temperaturas.
La Atmósfera Reductora
Una atmósfera reductora se define por la ausencia casi total de oxígeno. Para ser activamente "reductora", también debe contener gases reductores.
Estos gases, como el hidrógeno o el monóxido de carbono, eliminarán químicamente los átomos de oxígeno de los materiales con los que entren en contacto. Esto es esencial para procesos como la fundición de mineral en metal puro.
La Atmósfera Neutra (o Inerte)
Es importante reconocer un tercer estado: una atmósfera neutra o inerte. Este ambiente, típicamente compuesto de nitrógeno o argón, también está desprovisto de oxígeno.
Sin embargo, a diferencia de una atmósfera reductora, estos gases no donan electrones activamente. Su propósito es simplemente desplazar el oxígeno y evitar que ocurran reacciones químicas, protegiendo el material sin alterarlo.
Implicaciones Prácticas y Por Qué Es Importante
La elección entre estas atmósferas no es académica; es una decisión crítica en innumerables procesos industriales y científicos.
En Metalurgia y Tratamiento Térmico
Al fundir mineral de hierro, un alto horno se llena con coque (una forma de carbono), que se quema para crear una atmósfera reductora rica en monóxido de carbono y pobre en oxígeno. El CO elimina el oxígeno del mineral de óxido de hierro, reduciéndolo a hierro líquido puro.
De manera similar, al tratar térmicamente el acero, se utiliza una atmósfera reductora para evitar la formación de "cascarilla" (una capa de óxido de hierro) en la superficie caliente del metal.
En Cerámica y Esmaltado
La atmósfera dentro de un horno tiene un efecto profundo en el color final de los esmaltes cerámicos.
Un esmalte de carbonato de cobre, por ejemplo, se volverá verde en una atmósfera oxidante. En una atmósfera reductora, el mismo esmalte producirá un rojo brillante a medida que el óxido de cobre se "reduce" químicamente a cobre puro.
En Ciencias Planetarias
La distinción también es crucial para comprender la formación planetaria. La Tierra primitiva tenía una atmósfera reductora, lo que fue una condición necesaria para la formación de las complejas moléculas orgánicas que dieron origen a la vida.
Solo después de la evolución de los organismos fotosintéticos nuestro planeta desarrolló la atmósfera rica en oxígeno y oxidante de la que dependemos hoy.
Tomando la Decisión Correcta para su Objetivo
Su elección está dictada completamente por la transformación química que necesita lograr.
- Si su enfoque principal es prevenir la corrosión o eliminar el oxígeno de un compuesto (como la fundición de mineral): Necesita una atmósfera reductora rica en agentes como monóxido de carbono o hidrógeno.
- Si su enfoque principal es la combustión completa o la creación de un óxido químico específico: Necesita una atmósfera oxidante con un suministro controlado de oxígeno.
- Si su enfoque principal es simplemente proteger un material de cualquier cambio químico a altas temperaturas: Debe usar una atmósfera neutra o inerte, como argón o nitrógeno puro.
En última instancia, dominar las condiciones atmosféricas significa dominar el estado final y la integridad de su material.
Tabla Resumen:
| Tipo de Atmósfera | Característica Clave | Efecto Principal en los Materiales | Aplicaciones Comunes |
|---|---|---|---|
| Oxidante | Rica en oxígeno (aceptores de electrones) | Promueve la oxidación (ej., óxido, combustión) | Combustión completa, creación de óxidos específicos |
| Reductora | Desprovista de oxígeno, rica en H₂/CO (donantes de electrones) | Previene/revierte la oxidación (ej., purificación de metales) | Fundición de mineral, prevención de cascarilla en acero, efectos de color en cerámica |
| Neutra/Inerte | Desprovista de oxígeno (ej., N₂, Ar) | Previene cualquier reacción química | Protección de materiales contra cambios a altas temperaturas |
¿Necesita un control atmosférico preciso para los procesos de su laboratorio? La atmósfera adecuada del horno es fundamental para lograr las propiedades deseadas de sus materiales, ya sea que esté tratando térmicamente metales, desarrollando nuevas cerámicas o protegiendo muestras sensibles. KINTEK se especializa en hornos de laboratorio y equipos avanzados diseñados para un control atmosférico exacto. Nuestros expertos pueden ayudarle a seleccionar la solución perfecta para garantizar la oxidación, reducción o protección inerte para su aplicación específica. Contacte a KINTEK hoy para discutir sus necesidades de laboratorio y lograr resultados superiores.
Guía Visual
Productos relacionados
- Horno de Atmósfera Controlada de 1700 ℃ Horno de Atmósfera Inerte de Nitrógeno
- Horno de atmósfera controlada de 1200℃, horno de atmósfera inerte de nitrógeno
- Horno de atmósfera controlada de 1400 ℃ con nitrógeno y atmósfera inerte
- Horno de Atmósfera de Hidrógeno y Nitrógeno Controlado
- Horno de atmósfera controlada con cinta de malla
La gente también pregunta
- ¿Por qué es deseable un horno de atmósfera controlada en la sinterización? Lograr pureza y densidad superiores
- ¿Cómo se utiliza el oxígeno (O2) en atmósferas de horno controladas? Dominando la ingeniería de superficies para metales
- ¿Se puede soldar cobre con latón sin fundente? Sí, pero solo bajo estas condiciones específicas.
- ¿Qué es un horno de atmósfera controlada? Calentamiento de precisión sin oxidación para materiales superiores
- ¿Cuál es la necesidad de un horno de atmósfera controlada para la investigación de la corrosión? Replicando Riesgos Industriales Realistas



















