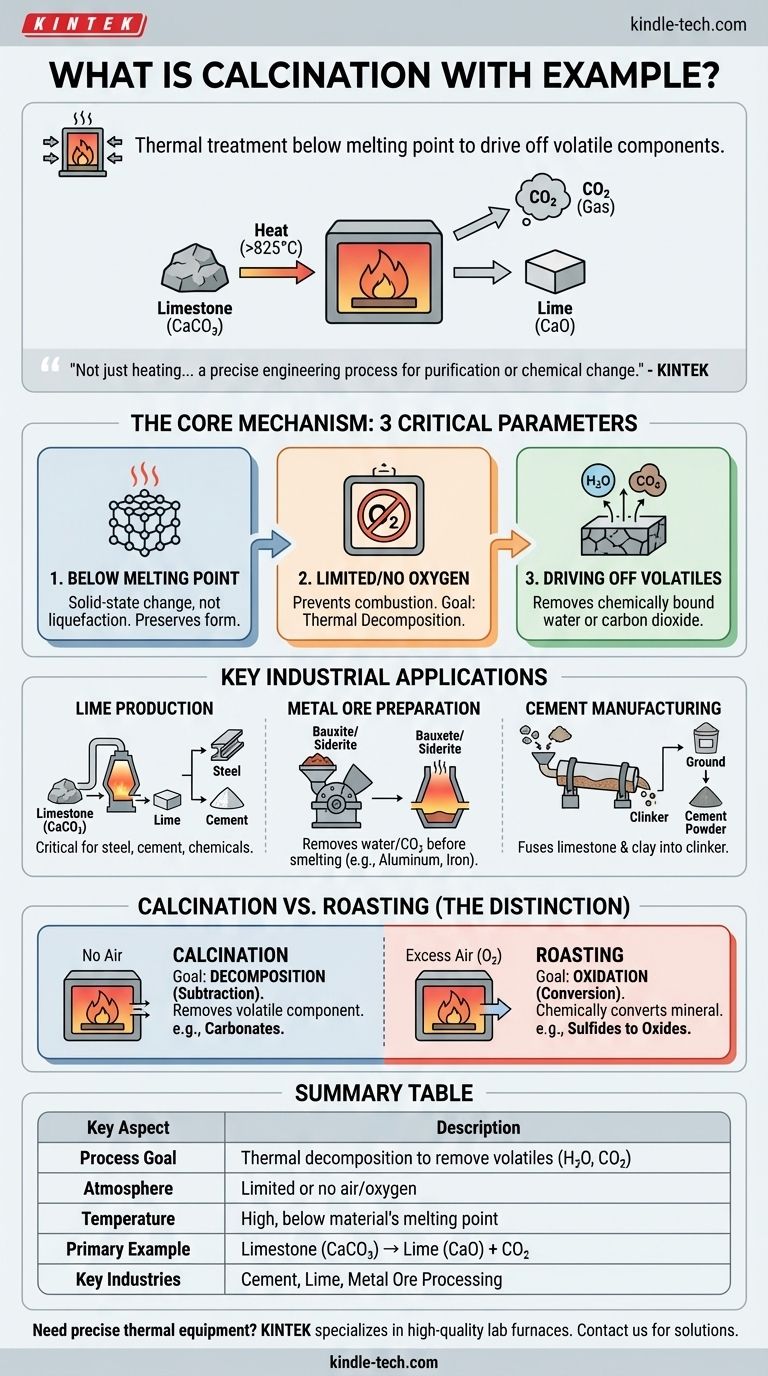
En esencia, la calcinación es un proceso de tratamiento térmico en el que un material sólido se calienta a una temperatura alta, por debajo de su punto de fusión, en ausencia o con un suministro limitado de aire. Este calentamiento controlado no tiene como objetivo fundir la sustancia, sino provocar una descomposición térmica, eliminando los componentes volátiles. El ejemplo más común es calentar piedra caliza (carbonato de calcio) para producir cal (óxido de calcio) y liberar dióxido de carbono gaseoso.
La calcinación no se trata simplemente de calentar algo. Es un proceso de ingeniería preciso diseñado para purificar un material o cambiar su composición química mediante el uso de calor para romper enlaces y eliminar sustancias volátiles específicas como agua o dióxido de carbono.

El mecanismo central: ¿Qué ocurre durante la calcinación?
La calcinación se define por tres parámetros críticos: temperatura, atmósfera y el cambio químico resultante. Comprender cada uno es clave para entender el proceso.
Calentamiento por debajo del punto de fusión
La temperatura se eleva lo suficiente como para romper los enlaces químicos, pero se mantiene intencionadamente por debajo del punto de fusión del material. El objetivo es inducir un cambio dentro del estado sólido, no licuarlo.
Esto preserva la forma sólida del material mientras altera su composición química, a menudo haciéndolo más poroso o reactivo para los pasos posteriores.
Oxígeno limitado o nulo
El proceso ocurre en un ambiente con muy poco o ningún oxígeno. Esta es una distinción crucial de otros procesos de tratamiento térmico.
La falta de oxígeno previene la combustión o la oxidación. El objetivo es la descomposición térmica (descomposición por calor), no una reacción con el aire circundante.
Eliminación de sustancias volátiles
El propósito principal de la calcinación es eliminar una fracción volátil del sólido. Esto típicamente implica la eliminación de agua químicamente ligada (hidratos) o dióxido de carbono (de carbonatos).
Por ejemplo, cuando la piedra caliza (CaCO₃) se calcina, el calor la descompone en cal sólida (CaO) y dióxido de carbono gaseoso (CO₂), que escapa.
Aplicaciones industriales clave
La calcinación es un proceso fundamental en varias industrias importantes, utilizado para preparar materiales para su posterior procesamiento o para crear un producto terminado.
Producción de cal a partir de piedra caliza
Este es el ejemplo por excelencia. La piedra caliza se calienta a más de 825 °C (1517 °F), lo que provoca la reacción: CaCO₃(s) → CaO(s) + CO₂(g).
El producto resultante, la cal (CaO), es un componente crítico en la fabricación de acero, cemento y numerosos procesos químicos.
Preparación de minerales metálicos
En metalurgia, la calcinación es un paso preparatorio común antes de la fundición. Elimina el agua de minerales hidratados como la bauxita (mineral de aluminio) o la siderita (mineral de hierro).
También elimina el dióxido de carbono de los minerales de carbonato como la smithsonita (ZnCO₃) o la calamina (una mezcla de minerales de zinc), lo que hace que la extracción posterior del metal sea más eficiente.
Fabricación de cemento
La producción de cemento Portland implica calentar una mezcla de piedra caliza y arcilla en un horno a unos 1450 °C (2640 °F).
Este proceso de calcinación elimina el CO₂ y fusiona químicamente los materiales en una nueva sustancia llamada "clínker". El clínker se muele luego hasta obtener el polvo fino que conocemos como cemento.
Comprender la distinción clave: Calcinación vs. Tostación
Muchas personas confunden la calcinación con la tostación, otro proceso de alta temperatura utilizado en metalurgia. La diferencia radica en las condiciones atmosféricas y la reacción química deseada.
El objetivo de la calcinación: Descomposición
Como se estableció, la calcinación utiliza calor en ausencia de aire para descomponer un compuesto. Es un proceso de sustracción, donde un componente volátil se elimina del mineral.
El objetivo de la tostación: Oxidación
La tostación, por el contrario, se realiza con exceso de aire. Su propósito es convertir químicamente un mineral a un nuevo estado mediante la oxidación. Un uso común es convertir minerales sulfurados en óxidos más fáciles de procesar (por ejemplo, 2ZnS + 3O₂ → 2ZnO + 2SO₂).
Tomar la decisión correcta para su análisis
Para identificar correctamente el proceso que está observando, concéntrese en los insumos y el resultado deseado.
- Si el objetivo principal es eliminar agua o CO₂ de un carbonato o hidrato: Está observando la calcinación, que utiliza calor para descomponer térmicamente un compuesto.
- Si el objetivo principal es hacer reaccionar un mineral sulfurado con oxígeno para formar un óxido: Está observando la tostación, que aprovecha tanto el calor como el exceso de aire para desencadenar la oxidación.
- Si el objetivo principal es producir clínker de cemento o cal industrial: Está observando una de las aplicaciones más extendidas y críticas de la calcinación.
Comprender esta diferencia fundamental entre la descomposición térmica (calcinación) y la oxidación (tostación) es clave para dominar estos procesos industriales fundamentales.
Tabla resumen:
| Aspecto clave | Descripción |
|---|---|
| Objetivo del proceso | Descomposición térmica para eliminar sustancias volátiles (p. ej., H₂O, CO₂) |
| Atmósfera | Aire/oxígeno limitado o nulo |
| Temperatura | Alta, pero por debajo del punto de fusión del material |
| Ejemplo principal | Piedra caliza (CaCO₃) → Cal (CaO) + Dióxido de carbono (CO₂) |
| Industrias clave | Producción de cemento, fabricación de cal, procesamiento de minerales metálicos |
| Proceso contrastante | Tostación (utiliza exceso de aire para la oxidación) |
¿Necesita equipos de procesamiento térmico precisos para su laboratorio o línea de producción?
La calcinación es un paso crítico en muchas aplicaciones industriales y de investigación, que requiere equipos de calentamiento confiables y precisos. KINTEK se especializa en hornos de laboratorio y soluciones de procesamiento térmico de alta calidad diseñados para procesos como la calcinación, la tostación y más.
Nuestros equipos ofrecen el control preciso de la temperatura y las condiciones atmosféricas necesarias para lograr resultados consistentes y de alta pureza, ya sea que esté procesando minerales, sintetizando materiales o desarrollando nuevos productos.
Contacte a KINTEK hoy para discutir cómo nuestros equipos térmicos especializados pueden mejorar la eficiencia y precisión de sus flujos de trabajo de procesamiento de materiales.
Guía Visual
Productos relacionados
- Planta de Horno de Pirólisis de Horno Rotatorio Eléctrico Máquina Calcinadora Horno Rotatorio Pequeño Horno Giratorio
- Horno Rotatorio Eléctrico de Trabajo Continuo, Pequeña Planta de Pirólisis con Calefacción de Horno Rotatorio
- Horno de Fusión por Inducción de Arco al Vacío No Consumible
- Horno Vertical de Vacío de Grafito de Alta Temperatura para Grafización
- Horno de grafización al vacío a ultra alta temperatura de grafito
La gente también pregunta
- ¿Cómo se calientan los hornos rotatorios? Explicación de los métodos de calentamiento directo vs. indirecto
- ¿Cuáles son las ventajas del horno de horno rotatorio? Logre una uniformidad y eficiencia superiores
- ¿Cuáles son las desventajas de un horno rotatorio? Altos costos y desafíos operativos
- ¿Es un horno rotatorio un horno? Descubra las diferencias clave para el procesamiento industrial
- ¿Cuáles son los diferentes tipos de calcinadores? Una guía para seleccionar el equipo de procesamiento térmico adecuado



















