En esencia, la calcinación es un proceso de purificación térmica. Implica calentar un material sólido a una temperatura alta, pero por debajo de su punto de fusión, en una atmósfera controlada con poco o nada de aire. Este calentamiento preciso elimina sustancias volátiles como agua y dióxido de carbono, desencadena la descomposición química o cambia la estructura cristalina interna del material, lo que da como resultado un sólido más puro, más estable o más reactivo.
El propósito principal de la calcinación no es fundir un material, sino transformarlo. Al controlar cuidadosamente el calor y la atmósfera, se pueden eliminar selectivamente componentes no deseados o cambiar las propiedades de un material sin alterar su estado sólido.

Cómo funciona fundamentalmente la calcinación
Para comprender la calcinación, es esencial entender sus tres componentes principales: calor controlado, una atmósfera específica y los cambios químicos resultantes.
El papel del calor (por debajo del punto de fusión)
El parámetro más crítico en la calcinación es la temperatura. El material se calienta intensamente, pero siempre se mantiene por debajo de su punto de fusión.
Esto asegura que el proceso se centre en la descomposición química en lugar de un cambio de estado (de sólido a líquido). Permite la descomposición controlada de compuestos dentro de la estructura sólida.
La atmósfera controlada
La calcinación se realiza típicamente en ausencia o con un suministro limitado de aire (oxígeno).
Esta es una distinción crucial. Al limitar el oxígeno, se previene la oxidación o la combustión. El objetivo es descomponer el material solo con calor (descomposición térmica), no hacerlo reaccionar con oxígeno.
El objetivo principal: la descomposición
El calor aplicado durante la calcinación proporciona la energía necesaria para romper los enlaces químicos. Esto se conoce como descomposición térmica.
Un ejemplo clásico es la producción de cal a partir de piedra caliza. Cuando la piedra caliza (carbonato de calcio, CaCO₃) se calcina, se descompone en cal (óxido de calcio, CaO) y libera gas dióxido de carbono (CO₂), un componente volátil.
Resultados clave de la calcinación
Dependiendo del material y el objetivo, la calcinación logra varios resultados específicos.
Eliminación de impurezas volátiles
La aplicación más común es la purificación. El proceso elimina sustancias volátiles, que son componentes que se convierten fácilmente en gas cuando se calientan.
Esto incluye agua ligada físicamente (secado), agua ligada químicamente en hidratos (deshidratación) y dióxido de carbono de los minerales de carbonato (descarbonatación). El resultado es una versión más concentrada y purificada del material base.
Inducción de transiciones de fase
A veces, el objetivo no es eliminar nada, sino cambiar la forma interna del material.
La calcinación puede inducir una transición de fase, que altera la estructura cristalina del material. Esto puede cambiar sus propiedades, como la dureza, la densidad o la reactividad, haciéndolo adecuado para una aplicación específica como un catalizador o un pigmento.
Preparación de materiales para procesamiento posterior
A menudo, la calcinación es un paso preparatorio. Al eliminar impurezas y crear una sustancia más reactiva (como un óxido), el material se prepara para un proceso posterior.
Por ejemplo, calcinar un mineral puede hacer que la extracción posterior del metal final mediante fundición sea más eficiente y menos intensiva en energía.
Comprensión de las compensaciones y distinciones
La calcinación a menudo se confunde con otros procesos térmicos. Comprender las diferencias es clave para entender su función específica.
Calcinación vs. Tostación
La tostación es otro proceso térmico, pero se realiza con un exceso de aire. Su objetivo es causar intencionalmente la oxidación. Por ejemplo, convertir un mineral de sulfuro metálico en un óxido metálico. La calcinación, por el contrario, evita activamente la oxidación.
Calcinación vs. Sinterización
La sinterización también utiliza calor por debajo del punto de fusión, pero su objetivo es completamente diferente. La sinterización busca fusionar pequeñas partículas para aumentar la densidad y la resistencia del material. La calcinación purifica y descompone; la sinterización consolida. En muchos flujos de trabajo industriales, la calcinación se realiza primero, seguida de la sinterización.
El riesgo de sobrecalentamiento
Controlar la temperatura es primordial. Si el material se calienta más allá de su punto de fusión, el proceso ya no es calcinación. Se convierte en fusión o sinterización, lo que puede ser indeseable y conducir a un producto final completamente diferente y, a menudo, inutilizable.
Tomar la decisión correcta para su objetivo
La calcinación es una herramienta precisa utilizada para lograr transformaciones específicas de materiales. Su objetivo dicta su aplicación.
- Si su enfoque principal es purificar un mineral: Utilice la calcinación para eliminar agua y carbonatos, creando un óxido más concentrado antes de la fundición.
- Si su enfoque principal es producir cemento: La calcinación de la piedra caliza para producir cal es el primer paso fundamental e innegociable del proceso.
- Si su enfoque principal es activar un catalizador: Utilice la calcinación para lograr la estructura cristalina y el área superficial ideales necesarios para una alta reactividad química.
En última instancia, la calcinación es una técnica fundamental en la ciencia de los materiales para modificar deliberadamente la composición química y la estructura de un sólido mediante el calor.
Tabla resumen:
| Aspecto clave | Descripción |
|---|---|
| Objetivo principal | Descomposición térmica y purificación sin fusión |
| Temperatura | Calentado por debajo del punto de fusión del material |
| Atmósfera | Aire/oxígeno limitado o nulo para evitar la oxidación |
| Insumos comunes | Piedra caliza (CaCO₃), minerales, hidratos |
| Productos comunes | Cal (CaO), óxidos purificados, catalizadores activados |
| Aplicaciones clave | Producción de cemento, procesamiento de minerales metálicos, activación de catalizadores |
¿Listo para transformar sus materiales con precisión?
El proceso de calcinación es fundamental para purificar minerales, producir cemento y activar catalizadores. KINTEK se especializa en equipos de laboratorio de alta temperatura necesarios para lograr estas transformaciones térmicas precisas de manera confiable y eficiente.
Ya sea que esté procesando minerales o desarrollando materiales avanzados, nuestra experiencia en hornos de laboratorio y consumibles garantiza que tenga las herramientas adecuadas para la descomposición controlada y las transiciones de fase.
Contacte hoy mismo a nuestros expertos en procesamiento térmico para discutir cómo las soluciones de KINTEK pueden optimizar su flujo de trabajo de calcinación y mejorar los resultados de sus materiales.
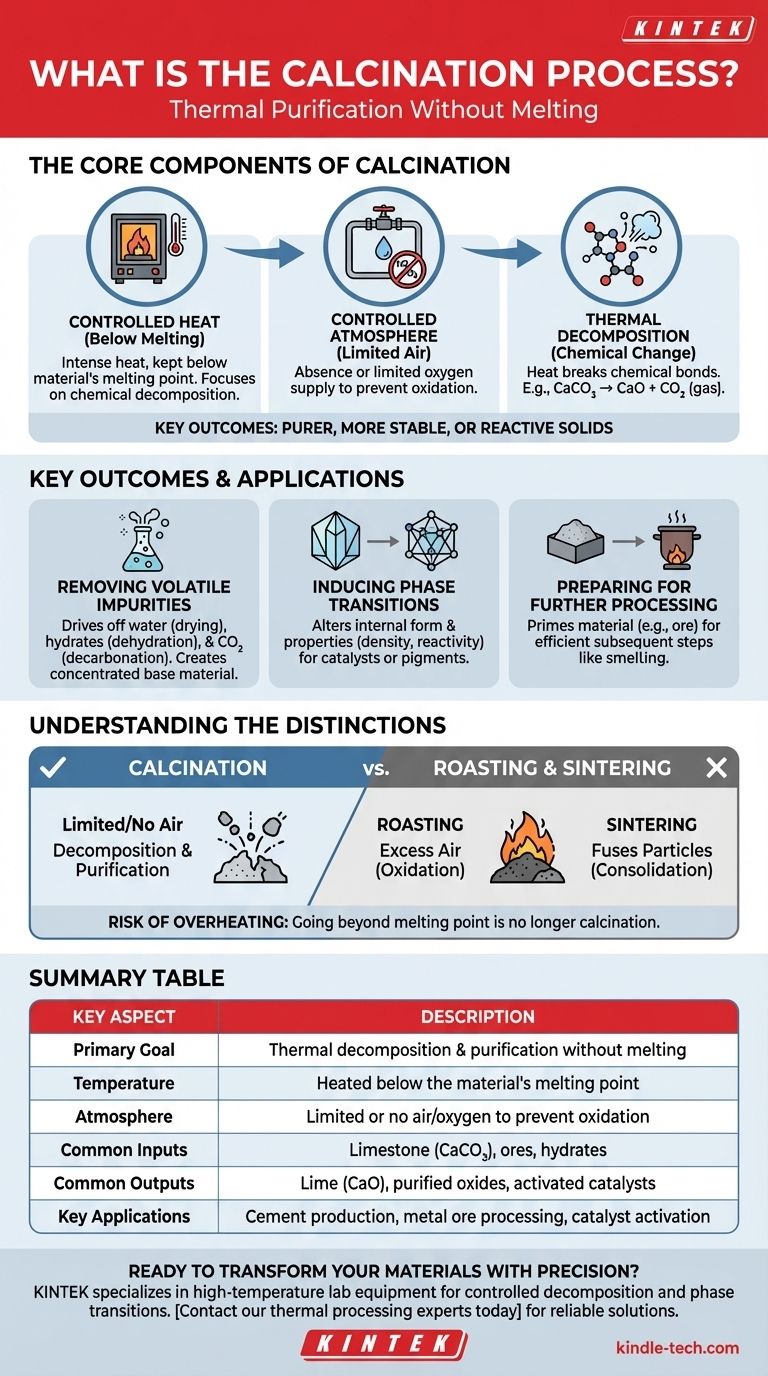
Guía Visual
Productos relacionados
- Planta de Horno de Pirólisis de Horno Rotatorio Eléctrico Máquina Calcinadora Horno Rotatorio Pequeño Horno Giratorio
- Horno Rotatorio Eléctrico de Trabajo Continuo, Pequeña Planta de Pirólisis con Calefacción de Horno Rotatorio
- Horno Vertical de Vacío de Grafito de Alta Temperatura para Grafización
- Horno de Grafización de Película de Alta Conductividad Térmica de Vacío de Grafito
- Horno de grafización al vacío a ultra alta temperatura de grafito
La gente también pregunta
- ¿A qué temperatura ocurre la pirólisis? Una guía para controlar la producción de su producto
- ¿Qué es un horno eléctrico de cuba rotatoria? Consiga un calentamiento uniforme superior para sus materiales
- ¿Cuál es la temperatura de un horno rotatorio? Depende de su material y objetivo de proceso
- ¿Cuáles son las desventajas de un horno rotatorio? Altos costos y desafíos operativos
- ¿Cuáles son las características de los modos de movimiento de lecho de deslizamiento, colapso y rodadura? Optimice su proceso rotatorio



















