En resumen, las atmósferas protectoras son necesarias en la sinterización para prevenir reacciones químicas destructivas, principalmente la oxidación, que ocurren a altas temperaturas. Este ambiente controlado asegura que las partículas de polvo metálico puedan unirse eficazmente, lo cual es el objetivo principal del proceso.
La sinterización requiere un calor inmenso para fusionar las partículas de material, pero ese mismo calor hace que esas partículas sean altamente vulnerables al ataque químico del aire circundante. Una atmósfera protectora reemplaza el aire reactivo con un gas controlado, actuando como un escudo químico que previene estas reacciones o las guía hacia un resultado deseado.

El desafío fundamental: Reactividad a altas temperaturas
La sinterización opera bajo un principio simple: calentar un polvo compactado hasta que las partículas se unan y se densifiquen. Sin embargo, las altas temperaturas requeridas también aceleran drásticamente las reacciones químicas, creando un desafío de ingeniería significativo.
El enemigo principal: La oxidación
La mayoría de la sinterización industrial involucra polvos metálicos. Cuando se calientan, estos metales reaccionarán fácilmente con cualquier oxígeno presente en la atmósfera.
Esta reacción, llamada oxidación, forma una capa delgada, dura y similar a la cerámica (un óxido) en la superficie de cada partícula de polvo.
Esta capa de óxido actúa como una barrera, impidiendo físicamente que las superficies metálicas hagan contacto directo y se fusionen. El resultado es una pieza débil y quebradiza que no se ha sinterizado correctamente.
Más allá del oxígeno: Otros contaminantes
Aunque el oxígeno es la principal preocupación, otros componentes del aire también pueden ser perjudiciales. El vapor de agua (humedad) y el dióxido de carbono son potentes agentes oxidantes a temperaturas de sinterización y deben eliminarse o desplazarse para proteger el material.
Cómo las atmósferas protectoras resuelven el problema
Una atmósfera protectora funciona reemplazando el aire ambiente reactivo en el horno con un gas o una mezcla de gases que es inerte o tiene una reactividad específica y deseable.
El principio de la inercia: Creando un escudo
El enfoque más simple es usar un gas inerte, más comúnmente Nitrógeno (N₂) o Argón (Ar).
Estos gases no reaccionan químicamente con el material que se está sinterizando, incluso a altas temperaturas. Funcionan simplemente desplazando el oxígeno y la humedad, creando un "escudo" neutral alrededor de las piezas.
El principio de la reducción: Limpieza activa de superficies
Un enfoque más potente implica una atmósfera reductora, que típicamente contiene Hidrógeno (H₂).
El hidrógeno no solo previene la nueva oxidación, sino que también puede revertirla activamente. Químicamente elimina los átomos de oxígeno de cualquier capa de óxido existente en las superficies del polvo, convirtiéndolos en vapor de agua (H₂O) que luego se expulsa del horno.
Esta acción de "limpieza" asegura una superficie metálica prístina, lo cual es crítico para lograr la máxima densidad y resistencia en la pieza final, especialmente con materiales que se oxidan fácilmente.
Reacciones deliberadas: Modificación de la superficie
A veces, el objetivo no es solo proteger la superficie, sino cambiarla intencionalmente. Se pueden usar mezclas de gases específicas para difundir elementos en la superficie del material.
Por ejemplo, una atmósfera rica en carbono (una atmósfera de carburación) puede usarse para crear una superficie de acero dura y resistente al desgaste en una pieza. De manera similar, una atmósfera rica en nitrógeno puede usarse para la nitruración. En estos casos, la atmósfera se convierte en una parte clave del diseño del material.
Comprendiendo las compensaciones
Elegir la atmósfera adecuada es un equilibrio entre los requisitos técnicos, la seguridad y el costo. No existe una única atmósfera "mejor" para todas las aplicaciones.
Atmósferas inertes vs. reductoras
Una atmósfera inerte como el Nitrógeno puro es segura, relativamente económica y eficaz para prevenir la oxidación en materiales menos sensibles.
Una atmósfera reductora que contiene Hidrógeno es más eficaz para crear piezas de alta pureza y alta densidad, pero introduce la complejidad de costo y seguridad del manejo de un gas inflamable.
El papel crítico de la pureza y el punto de rocío
La eficacia de cualquier atmósfera protectora depende de su pureza. Incluso una atmósfera de Nitrógeno puede volverse oxidante si contiene demasiada humedad o trazas de oxígeno.
El punto de rocío del gas es una medida crítica de su contenido de humedad. Un punto de rocío bajo indica un gas muy seco, lo cual es esencial para prevenir reacciones no deseadas durante el ciclo de sinterización a alta temperatura.
Costo y complejidad del sistema
El Argón puro proporciona el escudo más inerte, pero es significativamente más caro que el Nitrógeno. Los sistemas de Hidrógeno requieren controles de flujo sofisticados, interbloqueos de seguridad y sistemas de combustión, lo que aumenta la inversión inicial y la complejidad operativa del horno.
Selección de la atmósfera adecuada para su objetivo
Su elección de atmósfera depende directamente del material con el que esté trabajando y de las propiedades finales que necesite lograr.
- Si su enfoque principal es la prevención básica de la oxidación para materiales robustos (como algunas aleaciones de cobre): Una atmósfera inerte de Nitrógeno suele ser la opción más rentable y suficiente.
- Si su enfoque principal es la máxima densidad y resistencia para materiales sensibles (como aceros inoxidables o tungsteno): Es necesaria una atmósfera reductora que contenga Hidrógeno para limpiar los óxidos superficiales y asegurar una fuerte unión metálica.
- Si su enfoque principal es mejorar la dureza superficial y la resistencia al desgaste: Se requiere una atmósfera reactiva diseñada para la carburación o nitruración para lograr la química superficial deseada.
En última instancia, controlar la atmósfera del horno equivale a controlar la química fundamental de su proceso, lo que le da un control directo sobre la calidad final del componente sinterizado.
Tabla resumen:
| Función | Gases comunes utilizados | Beneficio clave |
|---|---|---|
| Blindaje inerte | Nitrógeno (N₂), Argón (Ar) | Previene la oxidación, rentable |
| Reducción activa | Mezclas de Hidrógeno (H₂) | Elimina óxidos existentes para máxima resistencia |
| Modificación de superficie | Gases ricos en carbono/nitrógeno | Mejora la dureza mediante carburación/nitruración |
Logre un control preciso sobre los resultados de su sinterización. La atmósfera protectora adecuada es fundamental para la densidad, resistencia y propiedades superficiales de las piezas. KINTEK se especializa en equipos y consumibles de laboratorio, proporcionando soluciones para todas sus necesidades de sinterización en laboratorio. Deje que nuestros expertos le ayuden a seleccionar la atmósfera ideal para su material y objetivos. Contáctenos hoy para discutir cómo podemos mejorar su proceso y asegurar resultados de alta calidad.
Guía Visual
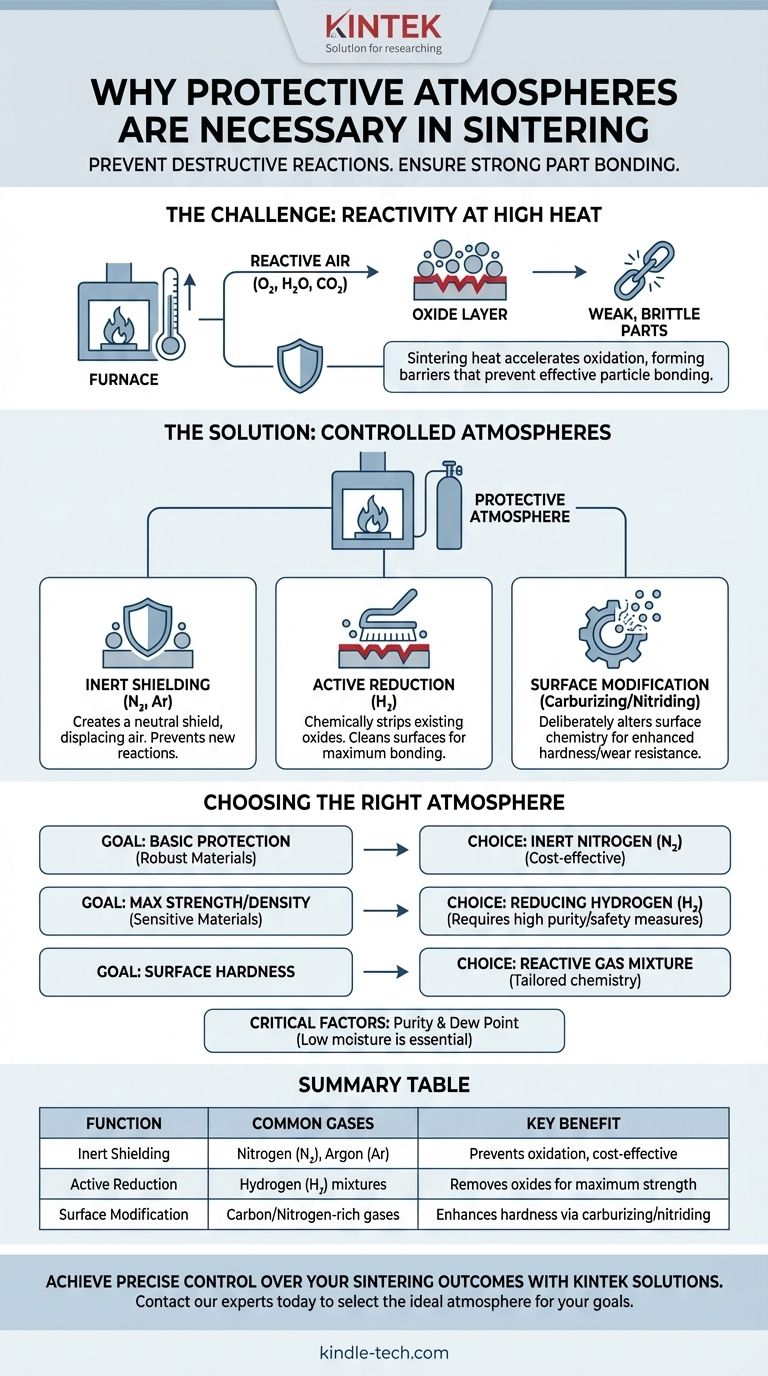
Productos relacionados
- Horno de atmósfera controlada con cinta de malla
- Horno de Atmósfera de Hidrógeno y Nitrógeno Controlado
- Horno de atmósfera controlada de 1200℃, horno de atmósfera inerte de nitrógeno
- Horno de Atmósfera Controlada de 1700 ℃ Horno de Atmósfera Inerte de Nitrógeno
- Horno de atmósfera controlada de 1400 ℃ con nitrógeno y atmósfera inerte
La gente también pregunta
- ¿Por qué es deseable un horno de atmósfera controlada en la sinterización? Lograr pureza y densidad superiores
- ¿Cuál es la función de un horno de control atmosférico en la producción de carburo de tungsteno? Lograr síntesis de alta pureza
- ¿Cuál es la necesidad de hornos de atmósfera controlada para la corrosión por gas? Asegure un modelado preciso de fallas de materiales
- ¿Qué gases se utilizan comúnmente en atmósferas controladas? Una guía de gases inertes y reactivos
- ¿Por qué es necesario un horno de atmósfera controlada para la preparación de catalizadores de metales activos?



















